

突破界限。点燃变革。 纳斯达克:IOBT 2024 年 1 月公司简报附录 99.1

免责声明 | 前瞻性 陈述本演示文稿中包含的某些信息包括经修订的1933年《证券法》第27A条和经修订的 1934年《证券交易法》第21E条所指的 “前瞻性陈述”,与我们的业务计划、临床试验和监管文件有关。在某些情况下,我们可能会使用 “可能”、“应该”、“将”、“期望”、“计划”、 “预期”、“可能”、“打算”、“目标”、“项目”、“考虑”、“相信”、“估计”、“预测”、“潜在” 或 “继续” 之类的术语或其他向他们传达未来事件或结果的不确定性的词语识别这些前瞻性陈述。我们的前瞻性陈述基于管理团队当前的信念和期望, 涉及风险、环境的潜在变化、假设和不确定性。任何或全部前瞻性陈述可能被证明是错误的,或者受到我们可能做出的不准确假设或已知或未知的风险和 不确定性的影响。这些前瞻性陈述受风险和不确定性的影响,包括与我们的业务计划的执行、临床试验或其他研究的成功和时机相关的风险,以及我们在向美国证券交易委员会提交的 文件中列出的其他风险。出于所有这些原因,实际业绩和发展可能与我们的前瞻性陈述中表达或暗示的业绩和发展存在重大差异。提醒您不要过分依赖这些前瞻性陈述,这些陈述仅在本演示之日作出。我们没有义务公开更新此类前瞻性陈述以反映随后的事件或情况。

适应症:黑色素瘤 SCCHN NSCLC 3 T-win 癌症疫苗技术平台 1 3 管道项目 17 专利家族专注于在不增加全身毒性的情况下改善临床效果 50% 80% * 1/2 期 MM1636 黑色素瘤结果 25.5 个月 MPFs* 提供快速持久的 反应亮点 | 打破界限。Ignite Change。24 年第 3 季度第 3 期中期分析结果 IO102-IO103 第 3 期晚期黑色素瘤关键试验已全部入组 2025 年潜在美国市场准入 ORR* CRR*

患者和市场视角 1 我们的 独特的价值主张 2 我们的产品线及其背后的科学 3 增长战略和展望 4 IO 生物技术团队 5 内容
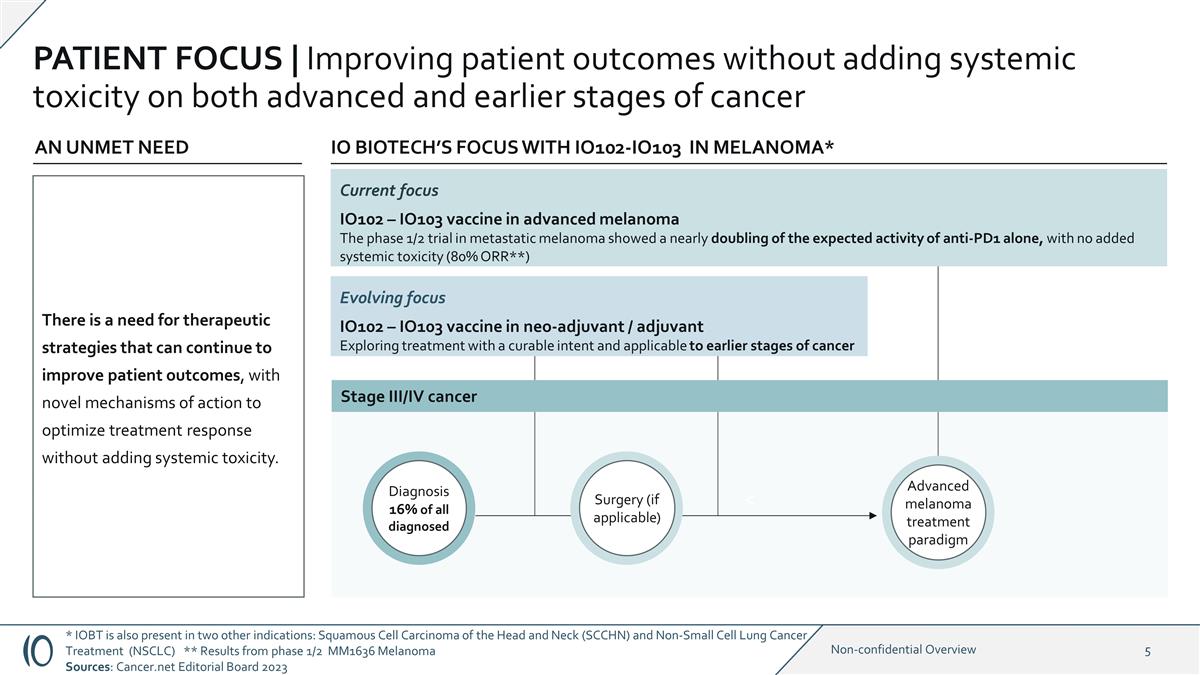
患者焦点 | 在不增加癌症晚期和早期阶段全身毒性的前提下改善患者 预后 * IOBT 还存在于另外两个适应症中:头颈部鳞状细胞癌 (SCCHN) 和非小细胞肺癌治疗 (NSCLC) ** 1/2 期 MM1636 黑色素瘤结果 来源:Cancer.net 编辑委员会 2023 不断演变的焦点 IO102 — IO103 新辅助剂疫苗/辅助药物 IO BIOTECH 以可治愈的目的探索适用于癌症早期阶段的治疗方法* Currenoma* Current IO102-IO103焦点 IO102 — 用于晚期黑色素瘤的 IO103 疫苗转移性黑色素瘤的 1/2 期试验显示,单独使用抗 PD1 的预期活性几乎翻了一番,没有增加全身毒性 (80% ORR**) 未满足的需求

市场 | IO Biotech 旨在解决 3种大型且不断增长的适应症中未得到满足的需求:头颈部鳞状细胞癌*(SCCHN)非小细胞肺癌治疗**(NSCLC)黑色素瘤新病例、全球死亡病例、全球新发病例、 全球死亡人数,2020年全球估计 2040 ~510 000 ~325,000 ~57,000 ~57,000 ~57,000 ~744,000 1,109,000 ~364,000 ~1,875,000 ~3,084,000 ~1,526,000 ~556,000 ~2,557,000 +57% +68% +49% +52% +64% +68% *此处显示的数据是唇部、口腔、喉部的发病率总和下咽癌和口咽癌**此处显示的数据相当于气管、支气管和肺部发病率的85%。来源:国际癌症研究机构
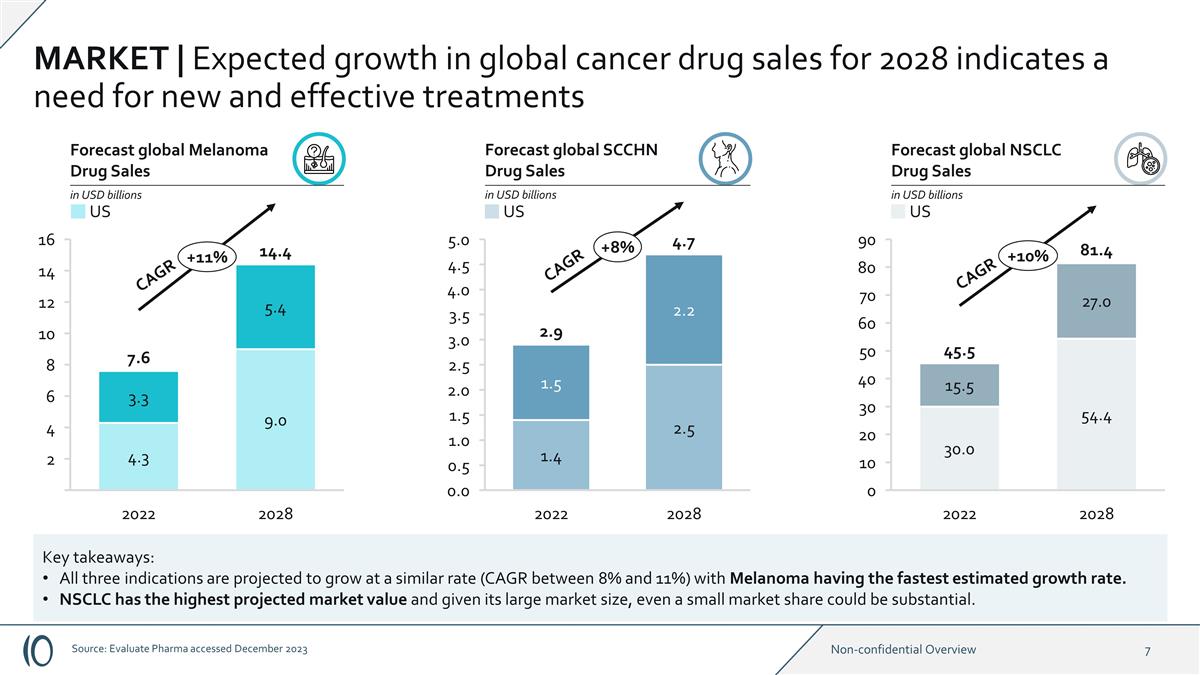
2028 2022 16 14 12 10 8 6 4 2 +11% 2028 2028 2028 2022年预测全球黑色素瘤药物销售额十亿美元预测全球非小细胞肺癌药物销售额十亿美元预测全球非小细胞肺癌药物销售额以十亿美元计 0.0 4.0 5.0 4.5 3.5 3.5 2.5 1.0 1.0 1.0 0.5 +8% 0 90 80 70 60 40 4.0 9.0 5.3 10 +10% 复合年增长率 30.0 54.0 27.0 15.5 14.4 7.6 2.9 4.7 CAGR 45.5 81.4 CAGR 市场 | 2028年全球抗癌药物销售的预期增长表明需要新的有效疗法关键要点:预计所有三种适应症都将以类似的速度(CAGR)增长介于8%至11%之间),其中黑色素瘤的估计生长速度最快。NSCLC的预计市场价值最高,鉴于其庞大的市场规模,即使很小的市场份额也可能很大。美国美国美国来源: Evaluate Pharma 于 2023 年 12 月访问
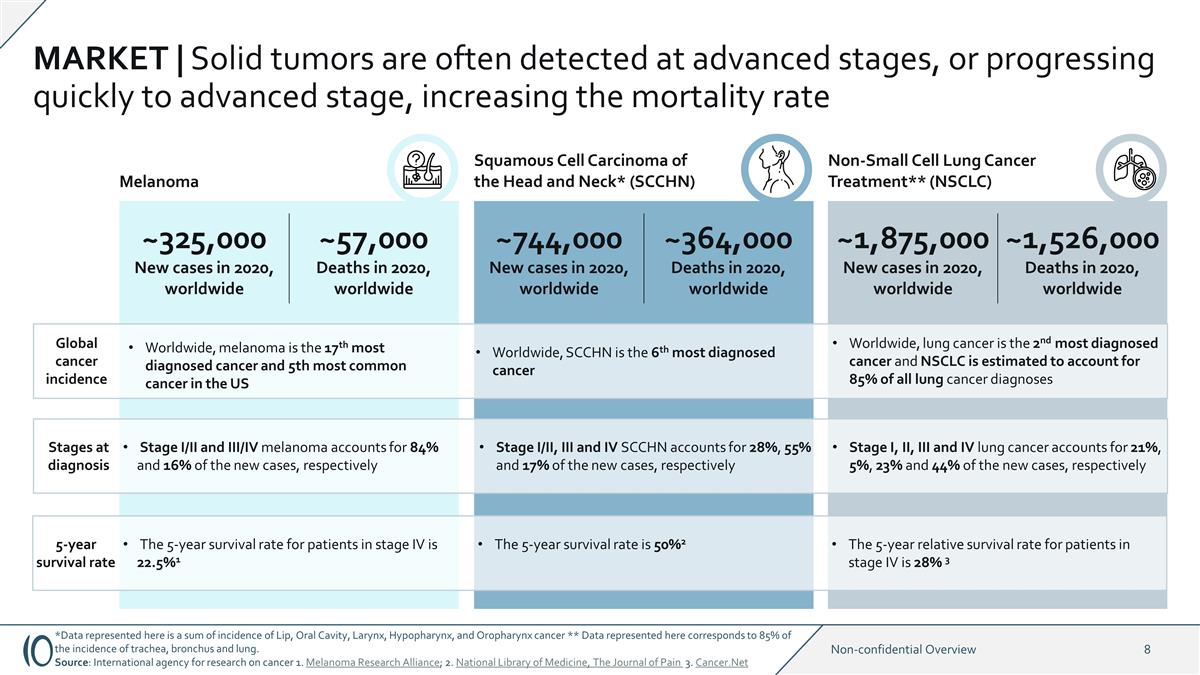
市场 | 实体瘤通常在晚期检测到 ,或迅速发展到晚期,使死亡率增加约32.5万例新发病例,2020年全球约57,000例死亡,2020年全球约74.4万例新发病例,2020年全球约36.4万例死亡,全球 黑色素瘤非小细胞肺癌治疗**(NSCLC)头颈部鳞状细胞癌*(SCCH* N) 2020 年新增约 1,875,000 例新发病例,2020 年全球约 1,526,000 例死亡,全球癌症发病率在全球范围内,肺癌是诊断率第二高的癌症,NSCLC 是估计占所有肺癌诊断的85% 5年存活率IV期患者的5年存活率为22.5% 1 5年存活率为50% 2 IV期患者 的5年相对存活率为28% 3个诊断阶段的I/III和III/IV阶段黑色素瘤分别占新发病例的84%和16%,SCCHN占28%,新发病例的55%和17%,分别是I、II、III和IV期肺癌 分别占新发病例的21%、5%、23%和44%,在全球范围内,SCCHN是6个黑色素瘤是全球诊断最多的癌症,是美国第17大最常见的癌症和第5大最常见的癌症。*此处显示的数据是唇癌、口腔癌、喉癌、下咽癌和口咽癌发病率的总和 ** 此处显示的数据对应气管、支气管和肺部发病率的85%。资料来源:国际癌症研究机构 1.黑色素瘤研究联盟; 2.国家医学图书馆,《疼痛杂志》3.Cancer.net
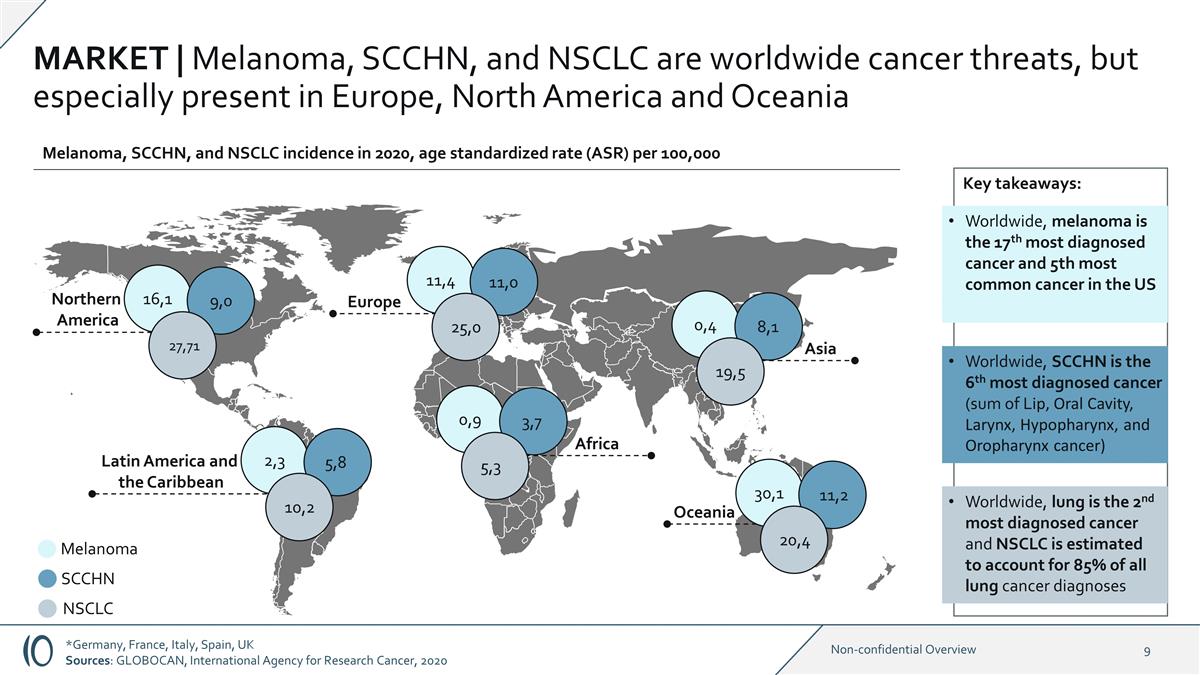
市场 | 黑色素瘤、SCCHN 和 NSCLC 是全球性的癌症威胁,但尤其存在于欧洲、北美和大洋洲 16,1 北美大洋洲欧洲 9,0 黑色素瘤 SCCHN NSCLC 27,71 11,0 25,0 30,1 11,2 20,4 亚洲 0,4 8,1 19,5 黑色素瘤、SCCHN 和 NSCLC 发病率 2020,每 100,000 人的年龄标准化率 (ASR) 关键要点:在全球范围内,黑色素瘤是美国全球诊断率第 17 位的癌症和第 5 位最常见的癌症,SCCHN 是诊断率排名第 6 的癌症(唇癌、口腔癌、喉癌、下咽癌、 和口咽癌之和)在全球范围内,肺是诊断率第二高的癌症,据估计,非小细胞肺癌占所有肺癌诊断的85% 拉丁美洲和加勒比地区 2,3 5,8 10,2 非洲 0,9 3,7 5,3 *德国、法国、意大利、西班牙、英国 来源:GLOBOCAN,国际癌症研究机构,2020

患者和市场视角 1 我们独特的价值主张 2 我们的产品线及其背后的科学 3 增长战略和展望 4 IO生物技术团队 5 内容
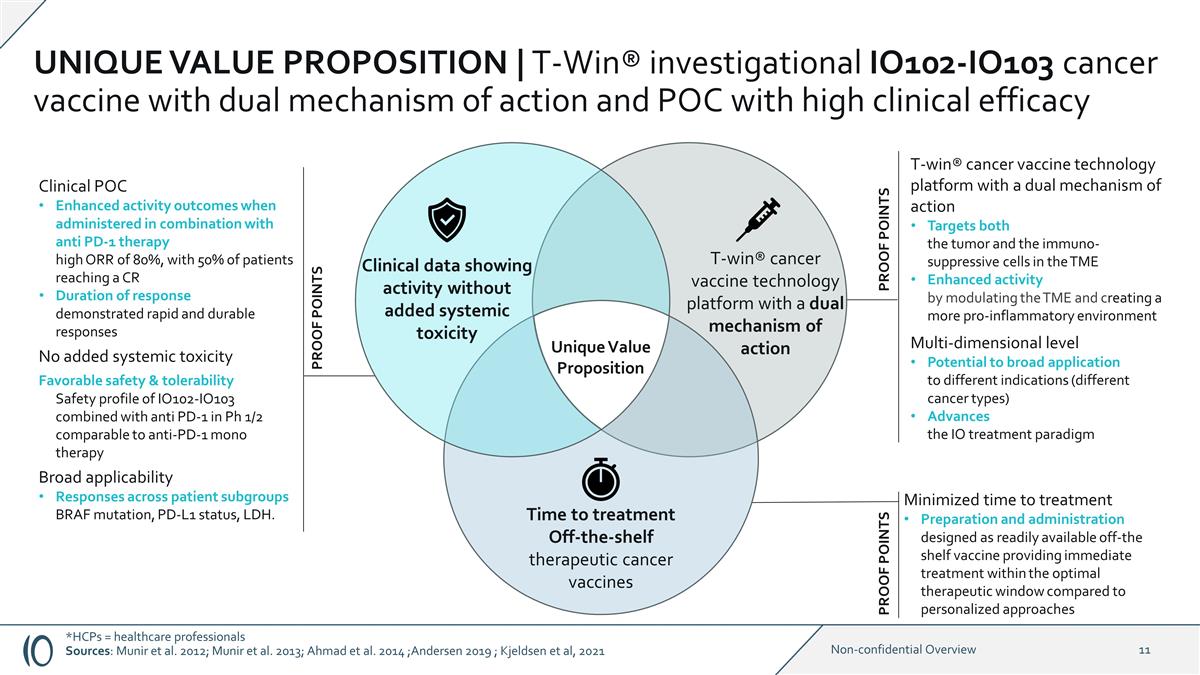
临床 POC 与抗 PD-1 疗法联合使用时活性增强 结果高达 80%,50% 的患者达到 CR 反应持续时间表现出快速而持久的反应没有增加全身毒性良好的安全性和耐受性 IO102-IO103 在 pH 1/2 中联合抗PD-1的安全特征与抗 PD-1 单一疗法相似的广泛适用性对患者亚组的反应 BRAF 突变、PD-L1 状态、LDH。最大限度地缩短了治疗时间准备和 给药设计为现成疫苗,与个性化方法相比,可在最佳治疗窗口内立即进行治疗具有双重作用机制的 T-win® 癌症疫苗技术平台 同时靶向 TME 中的肿瘤和免疫抑制细胞通过调节 TME 和创造更具促炎性的环境增强活性多维水平广泛应用于不同适应症(不同 癌症)类型)进度IO 治疗模式临床数据显示活性不增加全身毒性 T-win® 癌症疫苗技术平台具有双重作用机制治疗时间现成治疗性癌症 疫苗独特的价值主张证明点证明点 *HCPs = 医疗保健专业人员来源:穆尼尔等人。2012 年;穆尼尔等人。2013 年;安徒生 2019 年;Kjeldsen 等人,2021 年独特的价值主张 | T-Win® 正在研究的 IO102-IO103 癌症疫苗具有双重作用机制和具有高度临床意义的 POC功效

独特的价值主张 | 来自市场研究的初步医生反馈凸显了 IO Biotech 疫苗 IO102-IO103 的潜力 MoS 是提供的最令人印象深刻的数据 —— 法国 KOL(如果)ORR 优于 ipi + nivo,该产品将成为新的护理标准 — 美国 KOL 无论是 BRAF 或 PD-L1 状态如何,我都可能会将其用于所有患者 — 美国 KOL 很高兴能提供更多帮助患者看看从长远来看会有什么好处- KOL 鼓励AE和AE之间没有权衡利弊功效-KOL 它可以广泛扩展到更大的患者群体,并具有出色的疗效-KOL 来源:医师市场研究,2023 年第四季度;脑外科和 IO 生物技术(2023 年); 对 Ph1/2 数据和目标产品概况的反应
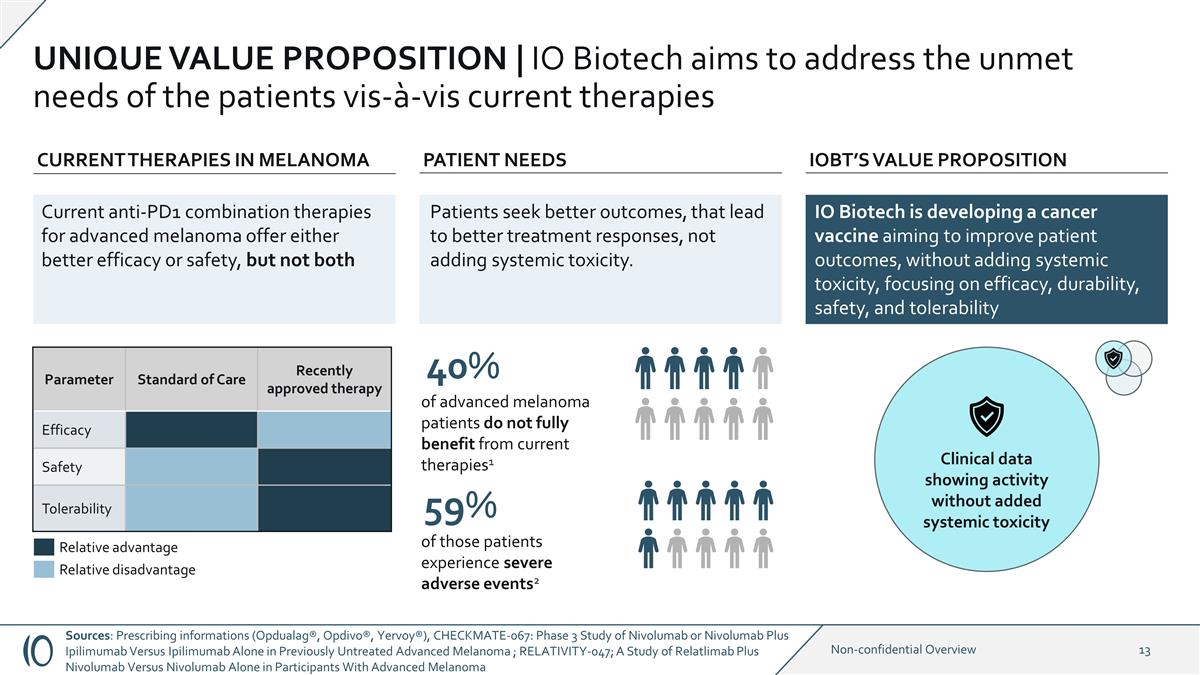
IO Biotech正在开发一种癌症 疫苗,目的是在不增加全身毒性的情况下改善患者的预后,重点关注疗效、耐久性、安全性和耐受性独特的价值主张 | IO Biotech旨在解决患者相对于当前 疗法未满足的需求参数护理标准最近批准的疗法疗效安全性耐受性黑色素瘤的当前疗法 IOBT 的价值主张缩写:这些患者中有59%出现严重不良事件 2 40% 的晚期 黑色素瘤患者无法完全受益当前疗法1 临床数据显示活性不增加全身毒性当前针对晚期黑色素瘤的抗 PD1 联合疗法具有更好的疗效或安全性,但并非两者都需要 1/10 2/10 3/10 5/10 6/10 7/10 7/10 8/10 9/10 9/10 10/10 10/10 2/10 3/10 7/10 7/10 8/10 9/10 10/10 相对劣势相对优势患者寻求更好的治疗反应,而不是增加全身毒性。来源: 处方信息(Opdualag®、Opdivo®、Yervoy®),CHECKMATE-067:Nivolumab 或 Nivolumab Plus Ipilimumab 对比单独使用伊匹木单抗对比单独治疗的晚期黑色素瘤的三期研究;RELATIVITY-047;对晚期黑色素瘤参与者的 Relatlimab Plus Nivolumab 对比单独使用 Nivolumab 的研究

患者和市场视角 1 我们独特的价值主张 2 我们的产品线及其背后的科学 3 增长战略和展望 4 IO生物技术团队 5 内容
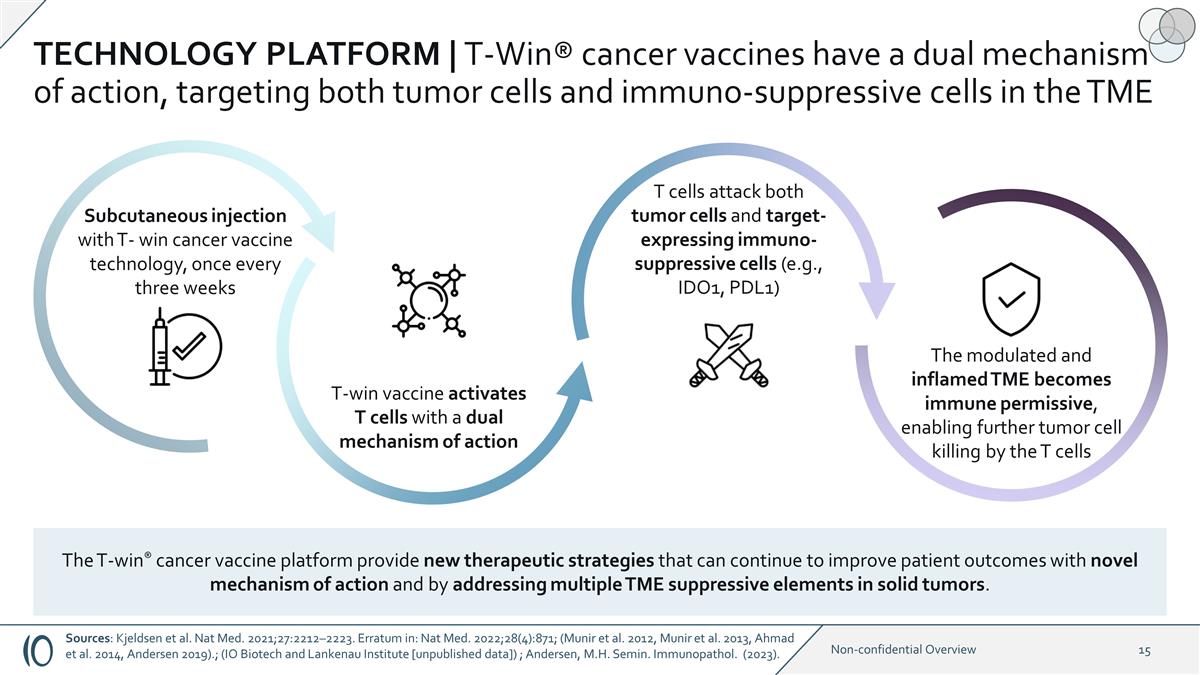
技术平台 | T-Win® 癌症疫苗具有双重作用机制,靶向 TME 中的肿瘤细胞和免疫抑制细胞 T 细胞同时攻击肿瘤细胞和靶向表达免疫抑制细胞(例如 IDO1、PDL1)。调制和发炎的 TME 成为允许免疫的,允许T细胞进一步杀死肿瘤细胞 T-win 疫苗使用双重激活T细胞作用机制 T-win 癌症疫苗技术皮下注射,每三周一次 T-win® cancer 疫苗平台提供新的治疗方法这些策略可以通过新的作用机制和解决实体瘤中的多种TME抑制因素来继续改善患者预后。资料来源:Kjeldsen等人。Nat 2021 年中学;27:2212 —2223。勘误表:Nat Med. 2022;28 (4): 871;(穆尼尔等人,2012 年,穆尼尔等人,2013 年,艾哈迈德等人,2014 年,安德森 2019)。(IO 生物技术和兰克瑙研究所)。 [未发布的数据]); 安徒生,M.H. Semin。免疫疗法。(2023)。
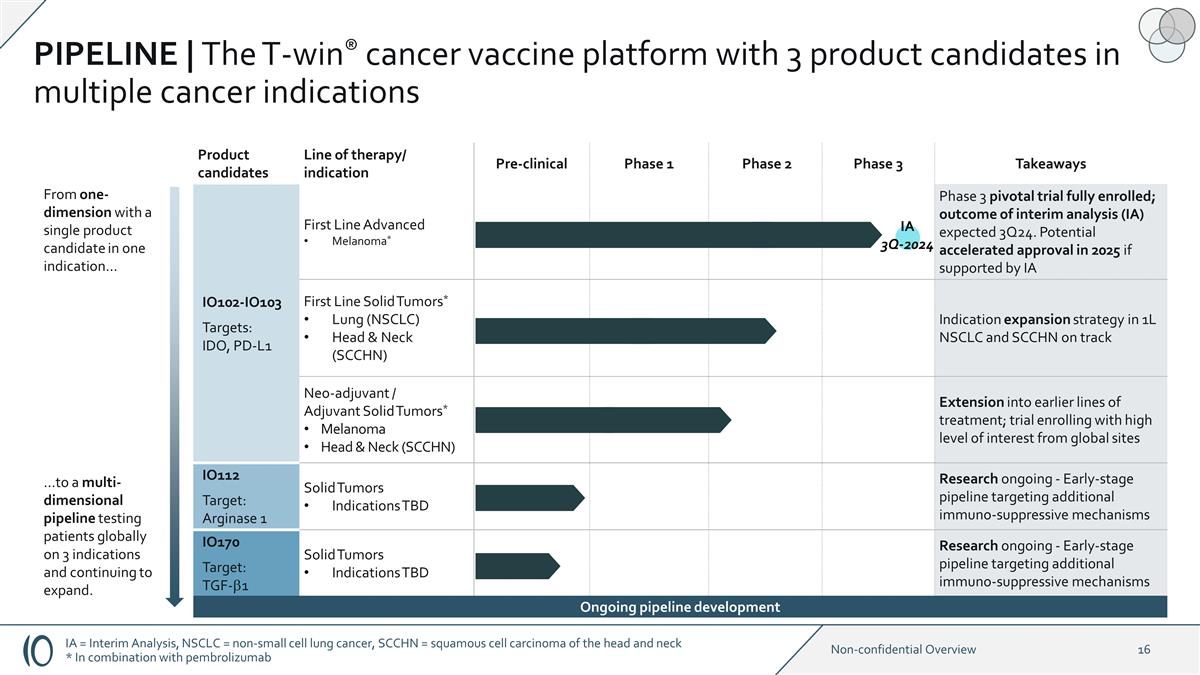
IA 3Q-2024 候选产品系列 疗法/适应症临床前 1 期 2 期 3 期要点 IO102-IO103 目标:IDO、PD-L1 一线晚期黑色素瘤* 3 期关键试验已全部入组;中期分析 (IA) 的结果预计在 24 年第 3 季度。如果 IA IO102—IO103 一线实体瘤*肺部 (NSCLC) 头颈部 (SCCHN) 1L NSCLC 和 SCCHN 的适应症扩展策略有望在 2025 年加快批准速度* 头部和 颈部黑色素瘤 (SCCHN) 扩展到早期治疗系列;备受关注的试验来自全球站点 IO112 目标:精氨酸酶 1 实体瘤适应症待定研究正在进行中-针对其他 免疫抑制机制的早期产品线 IO170 靶标:TGF-b1 实体瘤适应症待定研究正在进行——针对其他免疫抑制机制的早期产品线从单一适应症中使用单一候选产品的一维度... ... 到针对3种适应症在全球范围内对患者进行测试并持续扩大的多维管线。正在进行的研发管道 | T-win® 癌症疫苗平台在多种癌症适应症中有3种候选产品 IA = 中期分析,NSCLC = 非小细胞肺癌,SCCHN = 头颈部鳞状细胞癌 * 与pembrolizumab联合使用

临床试验 | IO102-IO103 的所有 临床数据令人鼓舞,黑色素瘤 (MM1636) 的 Ph1/2,结果令人鼓舞,推动了一线晚期黑色素瘤 (IOB-013/KN-D18) 的持续临床开发。实体瘤篮子 (IOB-022/KN-D38) 的 pH2 持续 pH2,初步疗效数据令人鼓舞;未观察到新的安全信号 1/2 期转移性黑色素瘤结果 (MM1636):80% ORR*,50% CR 状态:目前处于第 3 阶段,有 380 名患者第一线非小细胞肺癌 2 期结果 ORR 56% > 基准 ORR 39% ** 状态令人鼓舞的初步数据(n=18)在ESMO 2023 FIRST LINE SCCHN上公布的第二阶段结果 ORR 3/6 > 基准 ORR 23% **状态令人鼓舞的初步数据在ESMO 2023年上公布的令人鼓舞的初步数据从一维度,在一个适应症中包含 单一产品候选药物的单维度... 到对全球患者进行3种适应症的多维度测试,并持续扩展。*24 名出现反应的患者中有两名在随后的放射学 确认之前取得了进展(如先前在《自然医学》RECIST1.1= 73.3% ORR 中所报道的那样)**KEYNOTE-042(1L NSCLC PD-L1 ≥ 50%):ORR 39%;KEYNOTE-048(在 1L SCCHN CPS 中单独使用 pembro ≥ 20%):ORR 23%
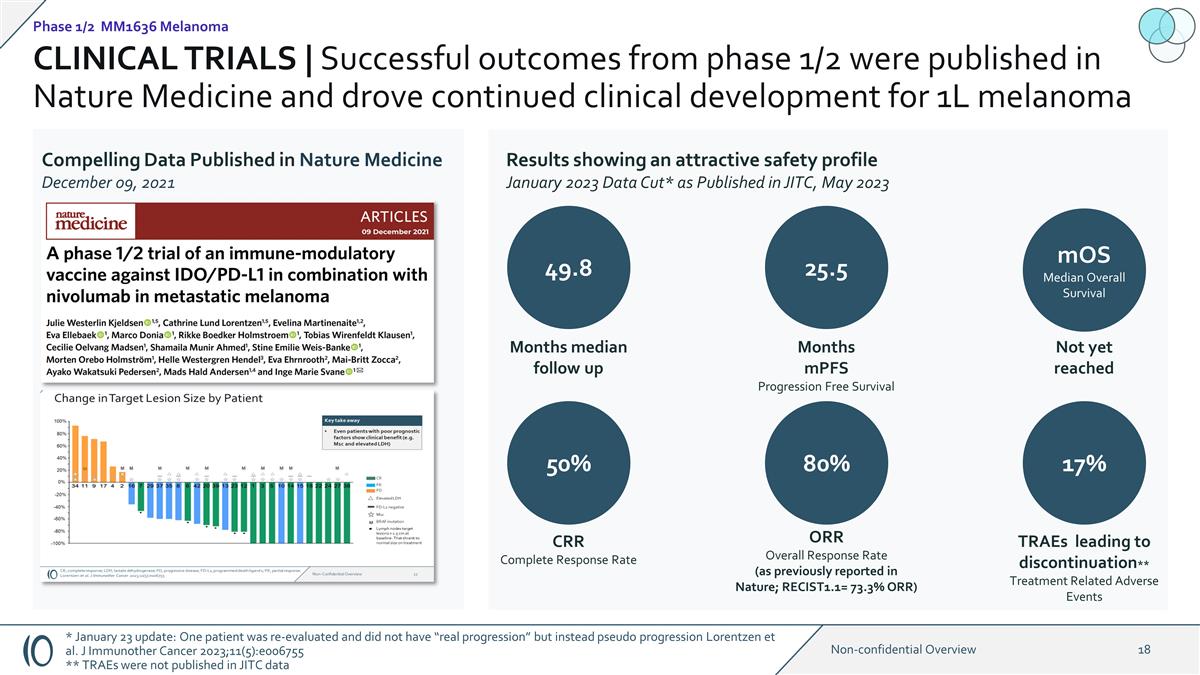
临床试验 | 1/2 期成功的 结果发表在《自然医学》杂志上,推动了 1L 黑色素瘤的持续临床开发 2021 年 12 月 9 日发表在《自然医学》上的令人信服的数据 2023 年 1 月 发布于 JITC 的数据截图* 49.8 个月随访中位数 25.5 MoS 总体存活率尚未达到 50% 80% 17% CRR 完全缓解率 ORR 总体缓解率 ORR 总缓解率(如先前在《自然》杂志上报道)RECIST1.1= 73.3% ORR) TRAE 导致 停药**治疗相关不良事件月份 mpfs 无进展生存期 1/2 期 MM1636 黑色素瘤 * 1 月 23 日更新:一名患者接受了重新评估,并没有 “实际进展”,而是假进展 Lorentzen 等人J Immunother Cancer 2023; 11 (5): e006755 ** TRAE 未在 JITC 数据中公布
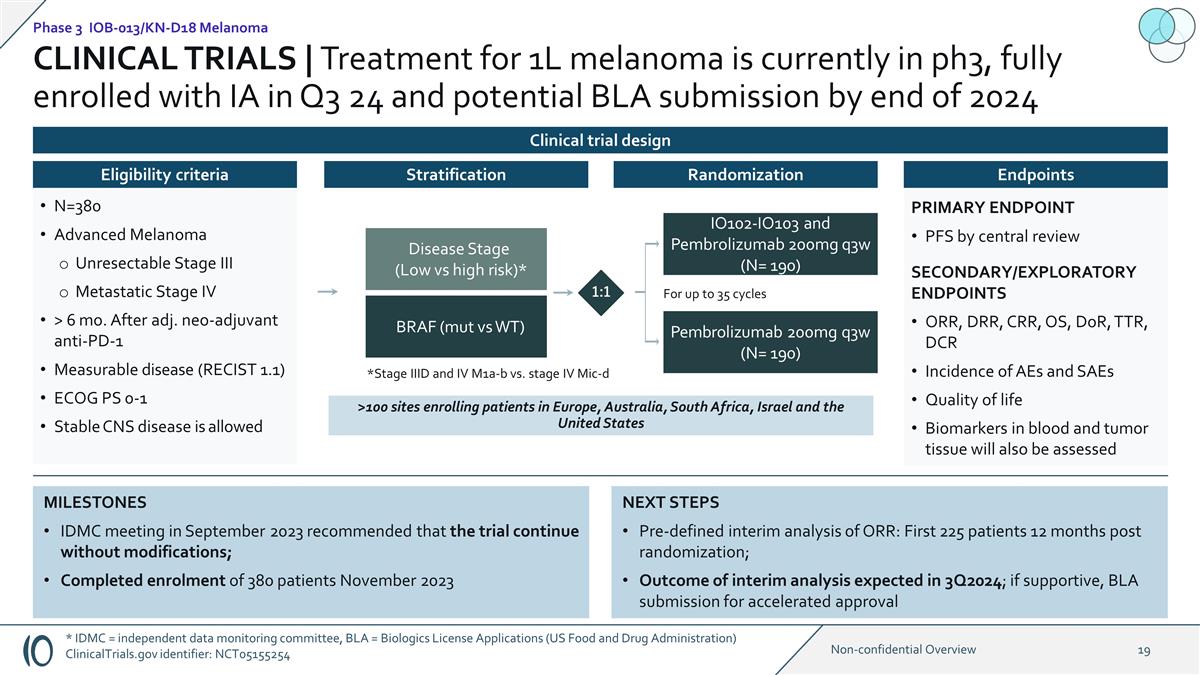
后续步骤预先定义的 ORR 中期 分析:随机分组 12 个月后的前 225 名患者;3Q2024 预计中期分析结果;如果支持,BLA 于 2023 年 9 月提交加速批准里程碑 IDMC 会议建议在不进行修改的情况下继续试验 ;2023 年 11 月完成了 380 名患者的入组 >100 个研究中心按中心审查二级/探索性终点在欧洲、澳大利亚、南非、以色列和美国注册患者的主要终点 PFS ORR、 DRR、CRR、OS、DoR、TTR、DCR 发生率血液和肿瘤组织中的生命质量生物标志物还将评估疾病阶段(低风险与高风险)* BRAF(mut vs WT)IO102-IO103 和 Pembrolizumab 200mg q3w(N= 190)Pembrolizumab 200mg q3w(N= 190)最多 35 个周期 1:1 *III 期和 IV 期 m1a-b 与 IV 期 mic-D 分层终点随机分层 N=380 晚期黑色素瘤不可切除的 III 期转移期 IV 期 > 6 mo。调整后。新辅助抗PD-1可衡量 疾病(RECIST 1.1)允许使用 ECOG PS 0-1 稳定的中枢神经系统疾病资格标准临床试验 | 1L 黑色素瘤的治疗目前处于第 3 阶段,24 年第三季度已完全入组 IA,并可能在 2024 年底前提交 BLA 第 3 阶段 IOB-013/KN-D18 黑色素瘤临床试验设计 * IDMC = 独立数据监测委员会,BLA,2024 年底前可能提交 BLA 第 3 阶段 IOB-013/KN-D18 黑色素瘤临床试验设计 * IDMC = 独立数据监测委员会,BLA = 生物制剂许可证申请(美国食品药品监督管理局)ClinicalTrials.gov 标识符:NCT05155254
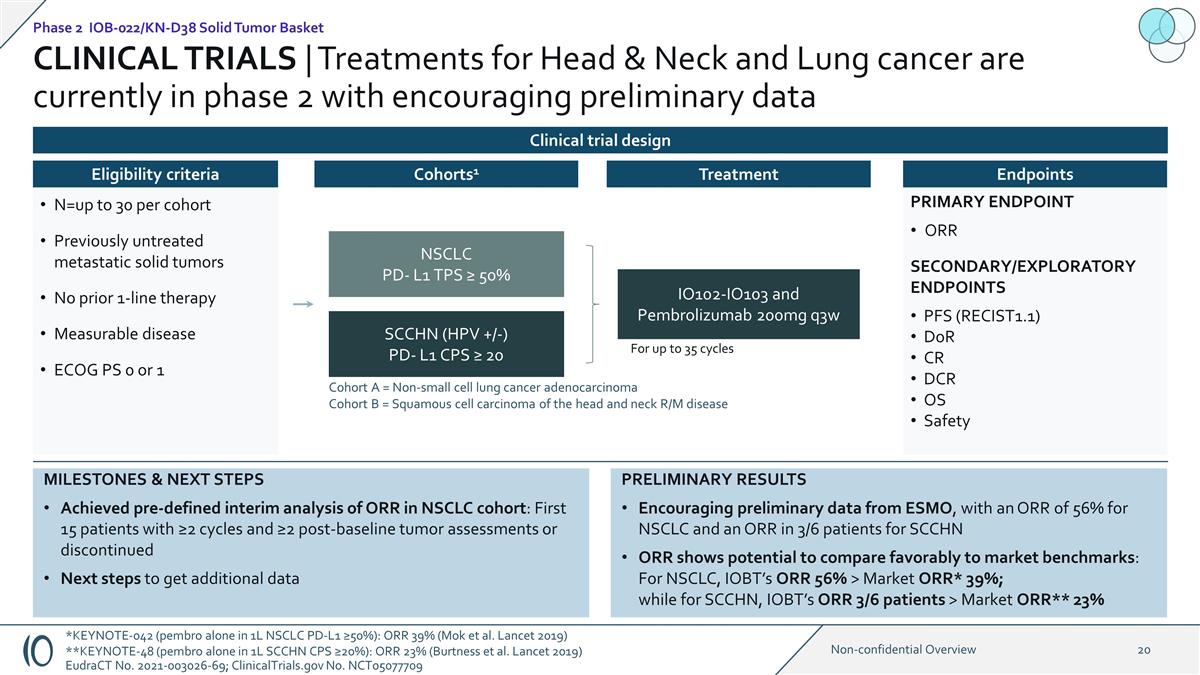
主要终点 ORR 次要/探索性终点 PFS (RECIST1.1) DoR CR DCR OS 安全性临床试验 | 头颈部和肺癌的治疗目前处于第 2 阶段,初步数据令人鼓舞 1:1 IO102-IO103 和 Pembrolizumab 200mg q3w NSCLC PD-L1 TPS ≥ 50% SCCHN (HPV +/-) PD-L1 CPS ≥ 20 队列 A = 非小细胞肺癌腺癌队列 B = 头颈部鳞状细胞癌 R/M 疾病长达 35 个周期 n=每个队列最多 30 个先前未经治疗的转移性 实体瘤此前未经治疗的转移性 实体瘤此前没有单线疗法可衡量的疾病 ECOGPS 0 或 1 资格标准 Cohorts1 治疗终点初步结果来自ESMO的初步数据令人鼓舞,非小细胞肺癌的ORR为56%,SCCHN ORR的3/6名患者显示有可能与市场基准相提并论:对于非小细胞肺癌,IOBT的ORR 56%>市场ORR* 39%;而对于SCCHN,IOBT的ORR 3/6患者>市场ORR** 23% 里程碑和后续步骤对非小细胞肺癌队列中的ORR进行了预定义的中期 分析:前15名周期≥2个且超过2次基线后肿瘤评估的患者或已停止的下一步获取更多数据第 2 阶段 IOB-022/KN-D38 实体瘤篮临床试验设计 *KEYNOTE-042(pembro 单独用于 1L NSCLC PD-L1 ≥ 50%):ORR 39%(Mok 等人Lancet 2019)**KEYNOTE-48(在 1L SCCHN CPS 中单独使用 pembro ≥ 20%):ORR 23%(Burtness 等人《柳叶刀》(2019)欧盟法案第 2021-003026-69 号;ClinicalTrials.gov No.NCT05077709
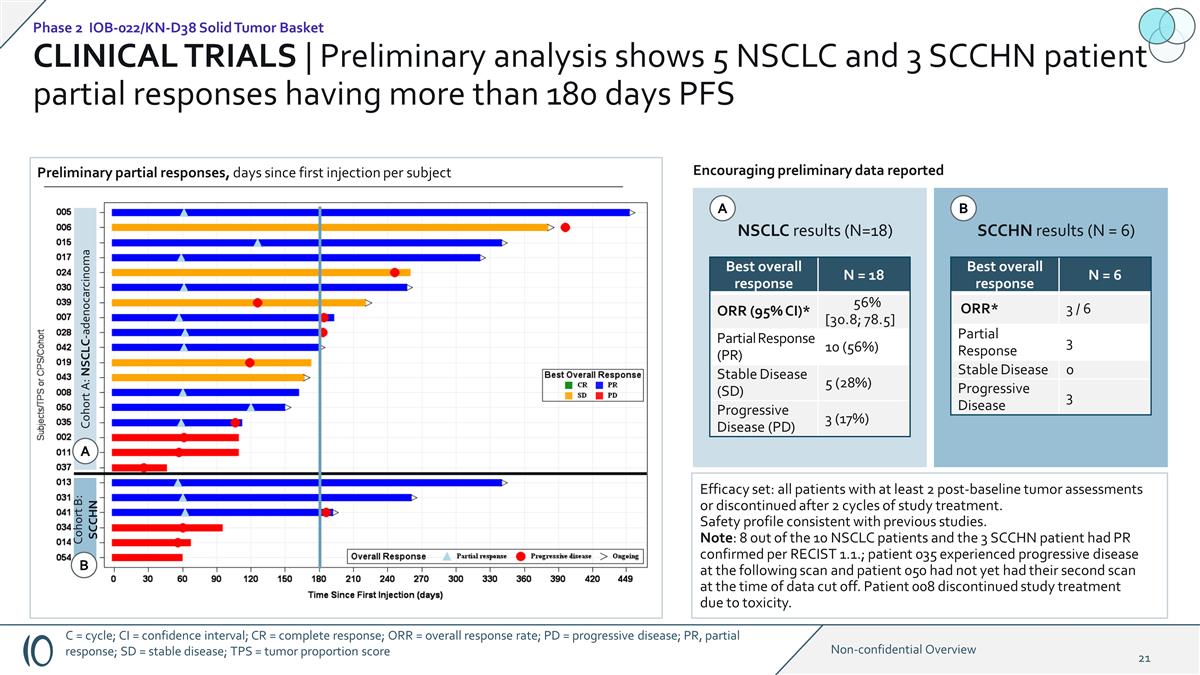
临床试验 | 初步 分析显示 5 名非小细胞肺癌和 3 名 SCCHN 患者部分反应超过 180 天 PFS 队列 A:NSCLC-腺癌队列 B:SCCHN NSCLC 结果(N=18)SCCHN 结果(N = 6)令人鼓舞的初步数据报告了最佳总体反应 N = 18 ORR(95% 置信区间)* 56% [30.8; 78.5]部分反应(PR)10(56%)稳定疾病(SD)5(28%)进行性疾病(PD)3(17%)疗效组合:所有接受过至少2次基线后肿瘤评估或在两个研究周期后停止治疗的患者。 安全概况与先前的研究一致。注意:根据RECIST 1.1,10名非小细胞肺癌患者中有8名和3名SCCHN患者已确认PR;035名患者在接下来的扫描中出现进展性疾病,而050名患者在数据截断时尚未进行第二次扫描。由于毒性,008号患者停止了研究治疗。最佳总体反应 N = 6 ORR* 3/6 部分反应 3 稳定疾病 0 进展性疾病 3 初步部分反应,自每个受试者首次注射 后的天数 A A B B 第 2 期 IOB-022/KN-D38 实体瘤篮子 C = 周期;CI = 置信区间;CR = 完全反应;PD = 进展性疾病;PR,部分反应;SD = 稳定疾病;TPS = 肿瘤 比例分数
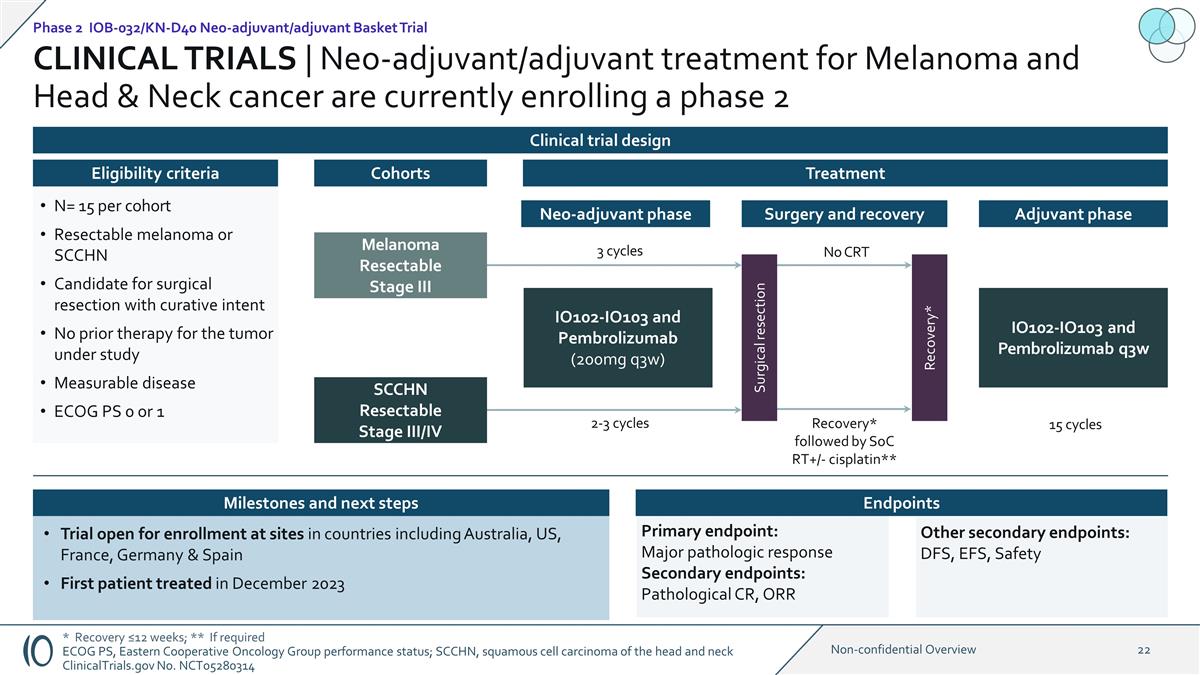
临床试验 | 黑色素瘤和头颈癌的新辅助/辅助治疗目前正在注册第二期 1:1 IO102-IO103 和 Pembrolizumab(200mg q3w)黑色素瘤可切除三期 SCCHN 可切除三期 SCCHN 可切除三期 N= 15 个可切除黑色素瘤 或 SCCHN 候选疗法意图之前没有对研究中的肿瘤进行任何治疗可衡量的疾病 ECOG PS 0 或 1 资格标准队列治疗试验在 澳大利亚、美国、法国、德国和西班牙等国家的研究中心开放招募首位患者接受治疗2023 年 12 月 2 期 IOB-032/KN-D40 新辅助/辅助篮子试验临床试验设计新辅助阶段 2-3 周期手术切除手术和康复 康复* IO102-IO103 和 Pembrolizumab q3w 15 个周期辅助第 3 期周期 * 恢复 ≤12 周;** 如果需要 ECOG PS,东部合作肿瘤学小组的表现状态;SCCHN,鳞状头部和颈部细胞癌 ClinicalTrials.gov No.NCT05280314 恢复* 其次是 SoC RT+/-cisplatin** 无 CRT 主要终点:主要病理反应次要终点:病理 CR、ORR 其他次要终点:DFS、EFS、安全里程碑和后续步骤 终点
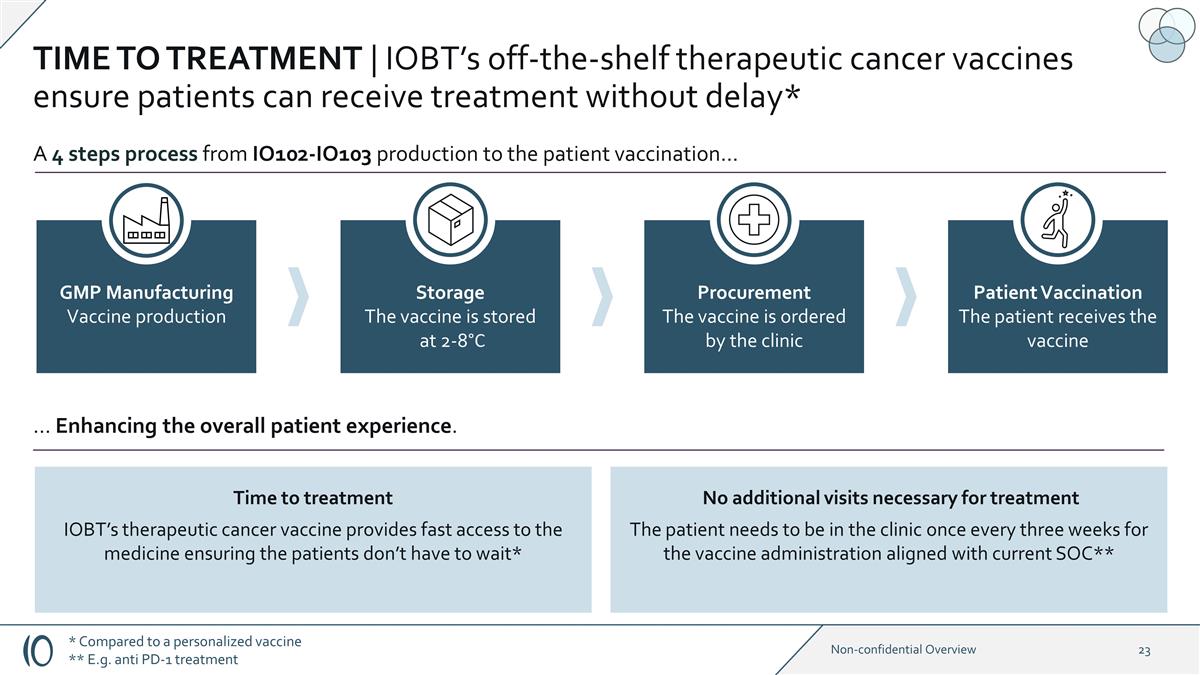
治疗时间 | IOBT 现成的治疗性癌症疫苗确保患者能够毫不拖延地接受治疗* GMP 制造疫苗生产存储疫苗储存在 2-8°C 采购疫苗由诊所订购患者疫苗接种 患者接种疫苗 A 从 IO102-IO103 生产到患者疫苗接种的四个步骤... 治疗时间 IOBT 的治疗性癌症疫苗可快速获得药物,确保患者不必这样做 等等*... 增强整体患者体验。无需额外就诊治疗患者需要每三周就诊一次,以便疫苗接种符合当前 SOC** * 与个性化 疫苗相比 ** 例如抗 PD-1 治疗
患者和市场视角 1 我们独特的价值主张 2 我们的产品线及其背后的科学 3 增长战略和展望 4 IO生物技术团队 5 内容
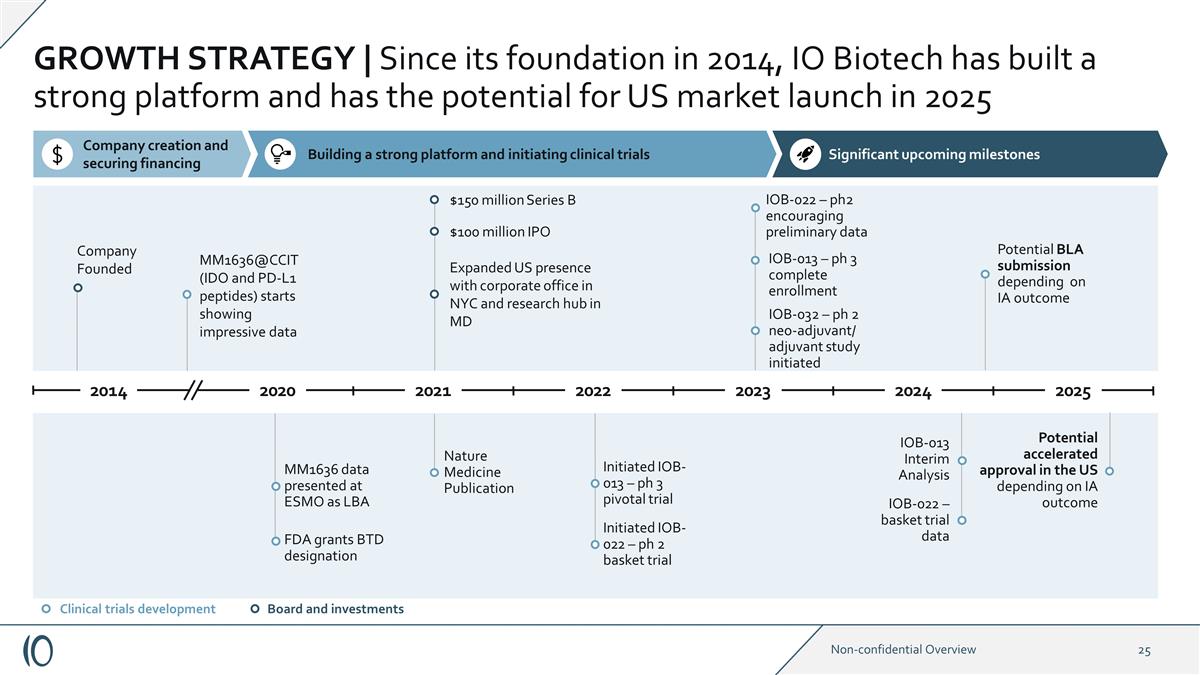
IOB-022 — 一揽子试验数据 增长战略 | 自2014年成立以来,IO Biotech已经建立了一个强大的平台,有可能在2025年在美国上市。公司创立的 MM1636 @CCIT(IDO 和 PD-L1 肽)开始显示令人印象深刻的数据 FDA 授予 BTD 称号 MM1636 数据作为 LBA 自然医学出版物 1.5 亿美元 B 轮融资 1 亿美元首次公开募股扩大了美国的影响力,在纽约设立了公司办公室,马里兰州启动了研究中心 IOB-022 — ph 2 篮子试验已启动 IOB-013 — ph 3 关键试验 IOB-022 — ph2 令人鼓舞初步数据董事会和投资临床试验开发 IOB-013 中期分析 IOB-013 — ph 3 完成注册根据 IA 的结果可能提交 BLA 提交 美国的批准可能性加快 即将到来的重要里程碑建立强大的平台并启动临床试验 2021 年 2020 年 2014 2023 2024 2024 IOB-032 — ph 2 新辅助/辅助研究已启动
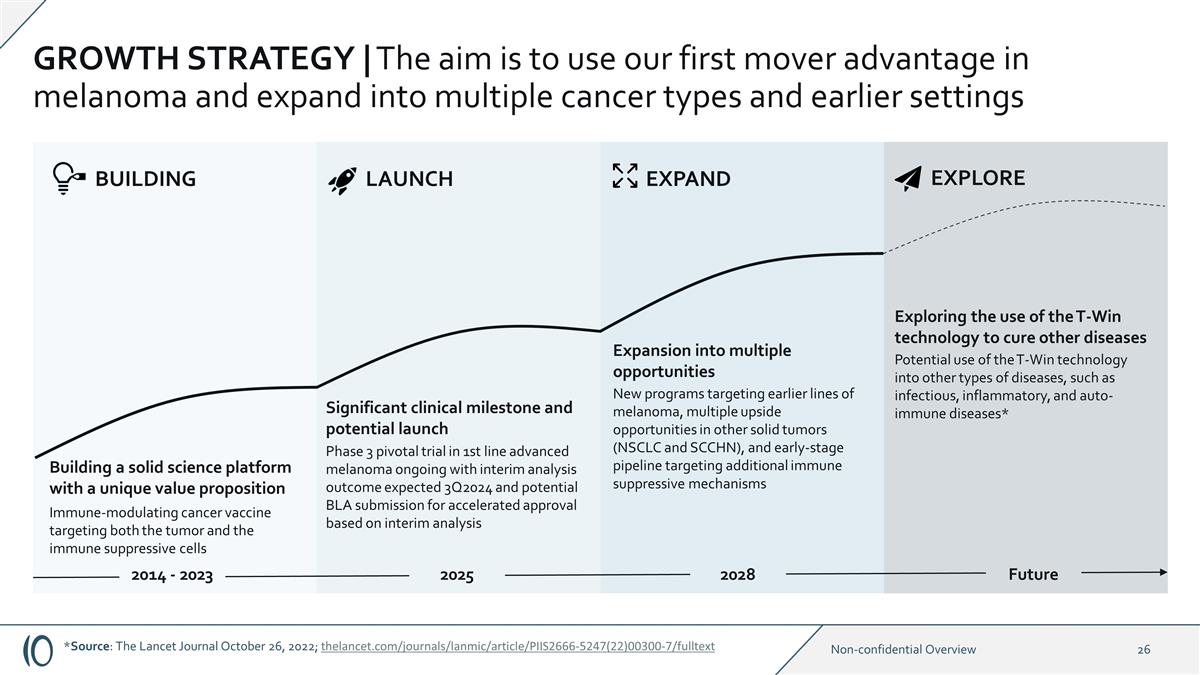
增长战略 | 目标是利用我们在黑色素瘤领域的先发优势,扩展到多种癌症类型和早期环境建立一个具有独特价值主张的坚实科学平台免疫调节癌症疫苗同时靶向肿瘤和免疫抑制性 细胞的重大临床里程碑和潜在的启动一线晚期黑色素瘤的3期关键试验正在进行中,中期分析结果预计 3Q2024,并可能根据中期分析提交 BLA 加速审批之前针对的新 程序黑色素瘤系、其他实体瘤(NSCLC 和 SCCHN)的多种上行机会,以及针对其他免疫抑制机制的早期产品线扩展到多种机会 2025 2028 扩展 BUILDING LAUNCH 2014-2023 年 T-Win 技术在其他类型的疾病中的潜在用途,例如传染性、炎症和自身免疫性疾病* 探索使用 T-Win 技术治疗其他疾病未来探索 *来源: 《柳叶刀日报》2022年10月26日;thelancet.com/journals/LANMIC/article/piis2666-5247 (22) 00300-7/全文

展望 | 预计未来两年将出现重要的临床 里程碑,这得益于 4Q2025 项目阶段适应症治疗系列 IO102-IO103 目标:IDO、PD-L1 三期黑色素瘤一线晚期 IO102—IO103 Basket 试验肺部 (NSCLC) 头颈部 (SCCHN) 一线转移性二期篮子试验黑色素瘤头颈部 (SCCHN) NEO-BR} 辅助/辅助 IO112 靶点:精氨酸酶 1 1/2 期实体瘤 IO170 靶标:TGF-b1 实体瘤到 2024 年的里程碑到 2025 年的里程碑到 2025 年的里程碑 2023 年 6 月入组 225 名患者在 2023 年年底前完成入组中期分析 (IA) 2Q2024,结果在 IA 支持下,美国可能加快批准速度 预计将在 25 年下半年达到无进展存活率的主要终点 附加数据启动第 2 阶段 2H2023 初始数据 IND 就绪 IND 申报;启动 IST 研究临床前研究基于 IA 的潜在的 BLA 提交 * 截至 2023 年 9 月 30 日。

患者和市场视角 1 我们独特的价值主张 2 我们的产品线及其背后的科学 3 增长战略和展望 4 IO生物技术团队 5 内容

团队 | 我们拥有一支强大的 管理团队,具有丰富的生物制药和生物技术经验 Mai-Britt Zocca,博士首席执行官卡西姆·艾哈迈德,医学博士首席医学官艾米·沙利文,工商管理硕士首席财务官埃里克·福克纳,工商管理硕士首席技术官德文·史密斯 总法律顾问丹·曼尼克斯博士,监管高级副总裁

董事会团队 | 我们的 管理团队得到董事会和科学顾问委员会的支持 Peter Hirth 博士主席 Kathleen Sereda Glaub,工商管理硕士成员 Christian Elling,博士成员 — Lundbeckfonden Hunter 成员 Jack B. Nielsen,M.Sc 成员 — Vivo Capital 大卫·史密斯,工商管理硕士 Mai-Britt Zocca Ca,博士科学顾问委员会主席兼首席执行官英格·玛丽·斯瓦恩,医学博士,博士创始人,临床顾问亚历山大·埃杰蒙特,医学博士,高级临床顾问卡皮尔·丁格拉, 医学博士战略研发顾问马兹·哈尔德安德森,医学博士,博士创始人,科学顾问海伦·柯林斯,医学博士成员

适应症:黑色素瘤 SCCHN NSCLC 3 T-win 癌症疫苗技术平台 1 3 管道项目 17 专利家族专注于在不增加全身毒性的情况下改善临床效果 50% 80% * 1/2 期 MM1636 黑色素瘤结果 25.5 个月 MPFs* 提供快速持久的 反应亮点 | 打破界限。Ignite Change。24 年第 3 季度第 3 期中期分析结果 IO102-IO103 第 3 期晚期黑色素瘤关键试验已全部入组 2025 年潜在美国市场准入 ORR* CRR*