

附录 99.1 企业概述 2024 年 1 月 8 日 © 2024 Invivyd, Inc.Invivyd 和 Invivyd 徽标是 Invivyd, Inc.的商标。本演示文稿中的所有商标均为其各自所有者的财产。

关于前瞻性陈述的警示说明本演示文稿 包含1995年《美国私人证券诉讼改革法》所指的前瞻性陈述。本演示文稿中非历史事实陈述的陈述均为前瞻性陈述。诸如 “可能”、“将”、“应该”、“期望”、“计划”、“预期”、“寻求”、“打算”、“目标”、“目标”、 “项目”、“设计用于”、“估计”、“相信”、“潜在” 或 “继续” 之类的词语或这些术语或其他类似表述的否定词意在 识别前瞻性陈述,尽管并非所有前瞻性陈述都包含这些识别词。前瞻性陈述包括以下方面的陈述:我们认为 Invivyd 有望进入 转型期,以及如果我们的紧急使用授权 (EUA) 申请获得批准,我们将为 VYD222 的潜在商业化发布做准备;如果获得批准,VYD222 EUA 的潜在范围,包括疾病状态和患者 人群;我们的使命是快速提供保护弱势群体免受病毒威胁的抗体;COVID 的未来-19 景观;我们对目标规模的期望患者群体和候选产品的潜在市场机会 以及我们的市场地位;我们对抗 SARS-CoV-2 单克隆抗体 (mAB) 临床用途的信念;公司 INVYMAB™ 平台方法在快速、 串行产生新抗体以应对病毒威胁方面的潜力;VYD222 的预期广泛活性和长期效用;我们正在进行的研究和临床的进展和时机开发活动,包括与 VYD222 相关的开发活动; CANOPY 临床试验设计,包括我们计划使用免疫桥接方法将CANOPY临床试验中获得的数据与阿丁特雷维单抗的某些历史数据进行比较;我们预计来自这家 公司EVADE临床试验的历史阿丁曲单抗数据可能会加速 VYD222 的开发;根据CANOPY临床试验中观察到的早期信号,VYD222 有可能对有症状的 COVID-19 提供强有力的临床保护;如果有 VYD222 能够迅速在美国上市 EUA 被授予;我们的候选产品渠道的潜力,如果经授权或批准,可用于预防或治疗严重的病毒性疾病,从 COVID-19 和 开始扩展到流感和其他急需适应症;以及其他非历史事实的声明。实际上,我们可能无法实现前瞻性陈述中披露的计划、意图或预期,您不应过分 依赖我们的前瞻性陈述。这些前瞻性陈述涉及风险和不确定性,可能导致我们的实际结果与前瞻性陈述中描述或暗示的结果存在重大差异, 包括但不限于:我们的发现、临床前和临床开发活动的时间和进展;我们从CANOPY临床试验中生成支持 VYD222 潜在EUA所需的临床数据的能力;我们在EUA申请 VYD222 结果方面与美国食品药品管理局的互动;美国提交的 VYD222 和其时机;VYD222 或其他候选产品的授权或批准的开发和监管途径; 在临床前研究或临床试验中观察到的意外安全性或有效性数据;基于临床前研究中和活性的 VYD222 或其他候选产品临床成功的可预测性; 临床前研究或临床试验的结果可能无法预测与当前或未来临床试验相关的未来结果的风险;我们在以下方面依赖第三方病毒检测创建和候选产品测试以及 我们的临床试验;用于预测针对关注的 SARS-CoV-2 变种活性的模型结果的差异性;预期或现有竞争的变化;监管环境的变化;监管 授权或批准程序的不确定性和时机;我们的平台方法是否使我们能够快速、串行地生成新的抗体以应对病毒威胁;VYD222 或任何其他候选产品是否能够证明并维持中和活性 针对相关、主要或占主导地位的 SARS-CoV-2 变体,尤其是在病毒进化的情况下;在 EUA 或批准(如果获得批准)后,VYD222 或任何其他候选产品的持续保持可接受的安全性、耐受性和有效性的能力;我们未来能否成功为任何其他候选产品提交 EUA,以及任何此类欧盟申请的结果和时间;我们生产足够商业数量的 VYD222 的能力; 制造单抗疗法的复杂性以及我们对它的依赖与制造商签订合同;我们建立销售、营销和分销基础设施以将 VYD222 或我们可能 获得监管批准或 EUA 的任何其他候选产品商业化的能力;我们能否为 VYD222 或任何其他候选产品获得和维持第三方保险和充足的报销;我们的研发工作是否会为除 COVID-19 以外的传染病确定和产生安全和 有效的治疗选择;我们继续作为持续经营企业的能力;以及我们是否有充足的资金以满足未来的运营费用和资本支出需求。 可能导致我们的实际业绩与本演示文稿中前瞻性陈述中明示或暗示的业绩存在重大差异的其他因素在我们向美国证券交易委员会(SEC)提交的最新10-K表年度报告、我们向美国证券交易委员会(SEC)提交的其他文件以及我们向美国证券交易委员会提交并可在www.sec.sec上查阅的最新报告中,在 “风险因素” 标题下进行了描述 gov。 本演示文稿中包含的前瞻性陈述自该日起作出,除非适用法律要求,否则我们没有义务更新此类信息,无论是由于新信息、未来事件还是其他原因。© 2024 Invivyd, Inc.Invivyd、Invymab 和 Invivyd 徽标是 Invivyd, Inc.的商标。本演示文稿中的所有商标均为其各自所有者的财产。2

INVIVYD 有望进入转型期,短期 有机会提供急需的治疗药物 • 2024 年 1 月,Invivyd 宣布向美国食品药品管理局提交 VYD222 紧急使用授权 (EUA) 申请,用于免疫功能低下 成人和青少年 COVID-19 的暴露前预防 • VYD222 EUA 的提交基于正在进行的关键 CANOPY 3 期临床试验的积极初步结果对包括 JN.1 公司在内的主要 SARS-CoV-2 变种的体外中和活性 如果获得 EUA,将继续为 VYD222 的潜在商业发射做准备 3
INVIVYD 的使命是快速提供保护 弱势人群免受病毒威胁的抗体,从 COVID-19 开始,短期机会 >900 万欧元 EUA 途径为获得授权或批准的潜在免疫功能低下的人群提供了在美国单独引进可能不能 单克隆抗体 VYD222(一种单克隆抗体)以充分反应 1 COVID-19 疫苗预防有症状免疫功能低下的成年人和青少年的机会 COVID-19 的暴露前 COVID-19 预防参考:1. 根据 Invivyd 赞助的市场研究和内部分析估算的市场机会 4
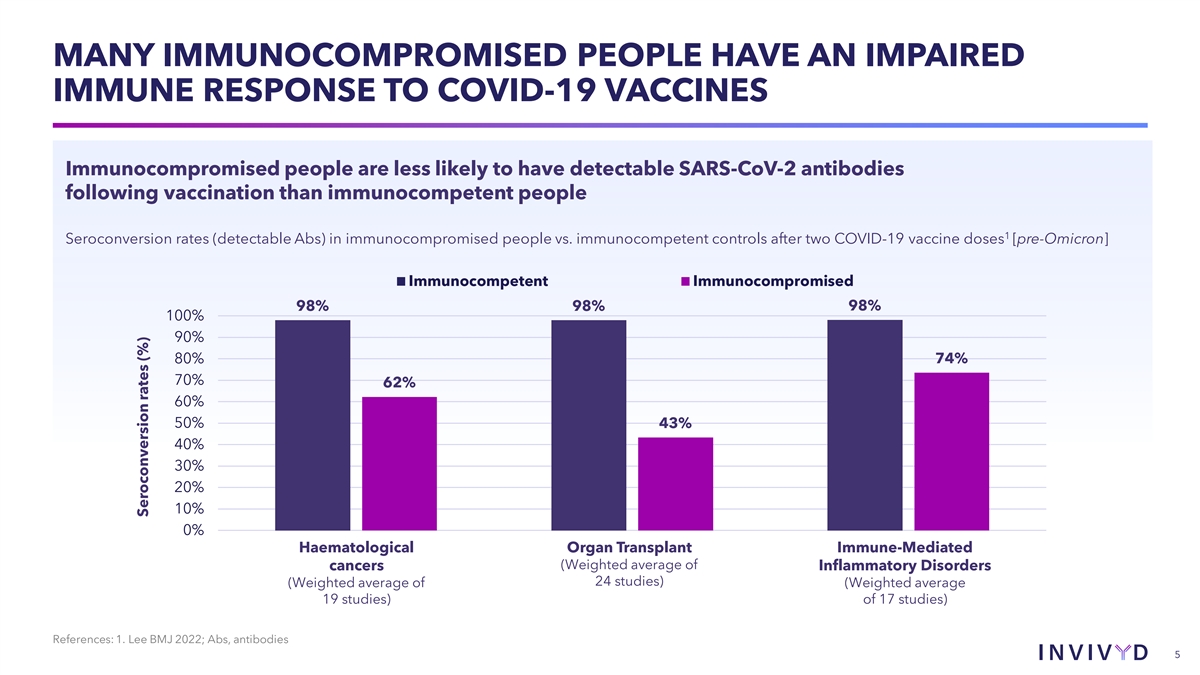
许多免疫功能低下的人对 COVID-19 疫苗的免疫反应受损与免疫功能正常的人相比,免疫功能低下的人在接种疫苗后获得可检测到的 SARS-CoV-2 抗体的可能性较小 1 免疫功能低下人群的血清转化率(可检测到 Abs)与免疫功能正常对照组 接种两剂 COVID-19 疫苗后的血清转化率(可检测到 Abs) [在 Omicron 之前]免疫正常免疫功能低下 98% 98% 98% 100% 90% 74% 70% 62% 60% 50% 43% 30% 20% 0% 0% 血液器官移植免疫介导癌症(炎症性疾病 24 项研究的加权平均值)(17 项研究(19 项研究的加权平均值)参考文献:1.Lee BMJ 2022;Abs、抗体 5 血清转化率 (%)
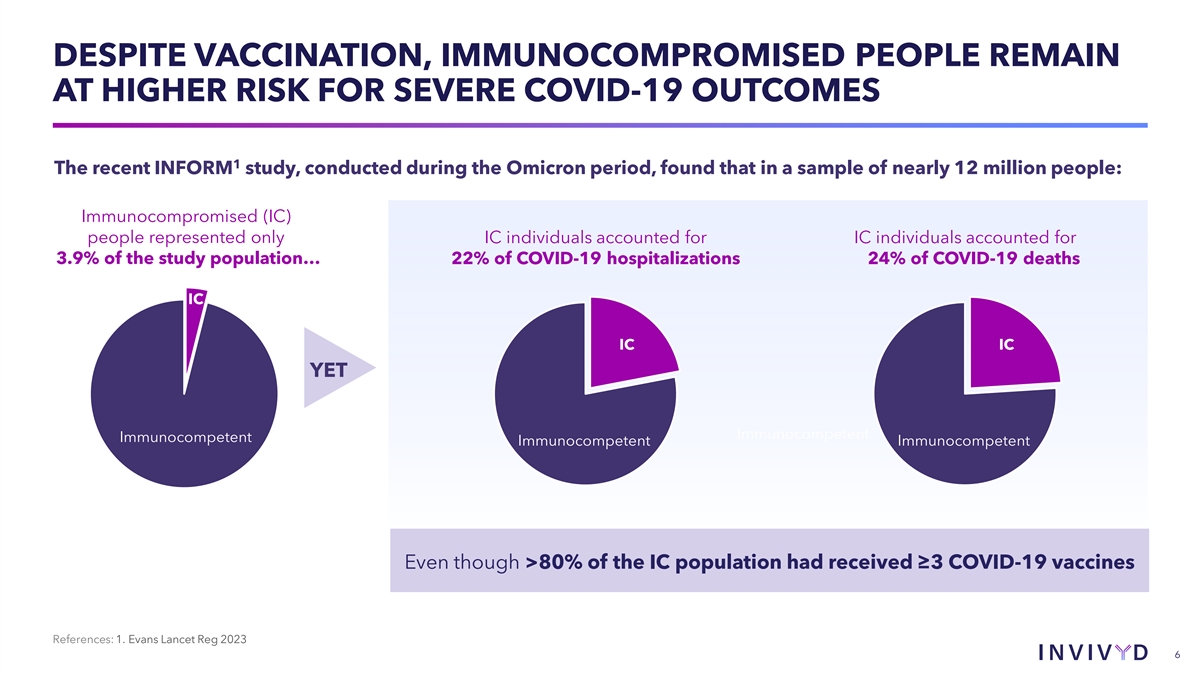
尽管接种了疫苗,但免疫功能低下的人出现 严重 COVID-19 结果的风险仍然更高 1 最近在 Omicron 时期进行的 INFORM 研究发现,在近 1200 万人的样本中:只有免疫功能低下 (IC) 的人占研究人群的 3.9%... COVID-19 住院人数占研究人群的 22% IC IC IC 但免疫功能正常的免疫功能正常即使 80% 的 IC 人群接种了 ≥3 支 COVID-19 疫苗 COVID-19参考文献:1.Evans Lancet Reg 2023 6
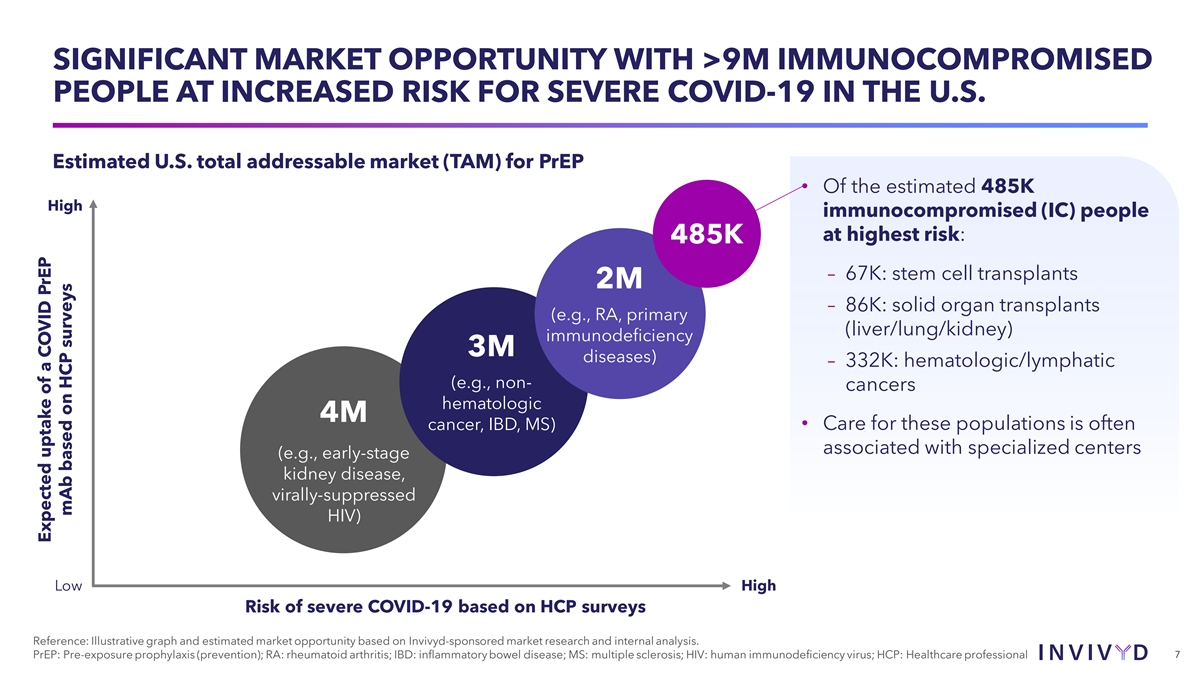
巨大的市场机会,美国超过900万免疫功能低下人群患重症 COVID-19 的风险增加。估计美国PrEP的总潜在市场(TAM)• 在估计的48.5万高免疫功能低下(IC)人群中:485K — 67K:干细胞移植 2M — 86K:固体 器官移植(例如 RA、原发性(肝/肺/肾)免疫缺陷 3M 疾病)— 33K 2K:血液学/淋巴系统(例如,非癌症血液学 4M 癌、IBD、MS)• 对这些人群的护理通常与专门的 中心(例如,早期阶段)有关肾脏疾病,病毒抑制的 HIV)重度 COVID-19 的低高风险根据 HCP 的调查参考文献:根据 Invivyd 赞助的市场研究和内部分析得出的说明性图表和估计的市场机会。 PrEP:暴露前预防(预防);RA:类风湿性关节炎;IBD:炎症性肠病;MS:多发性硬化症;HIV:人类免疫缺陷病毒;HCP:医疗保健专业人员 7 根据HCP 的调查,COVID PrEP 单抗的预期摄取量
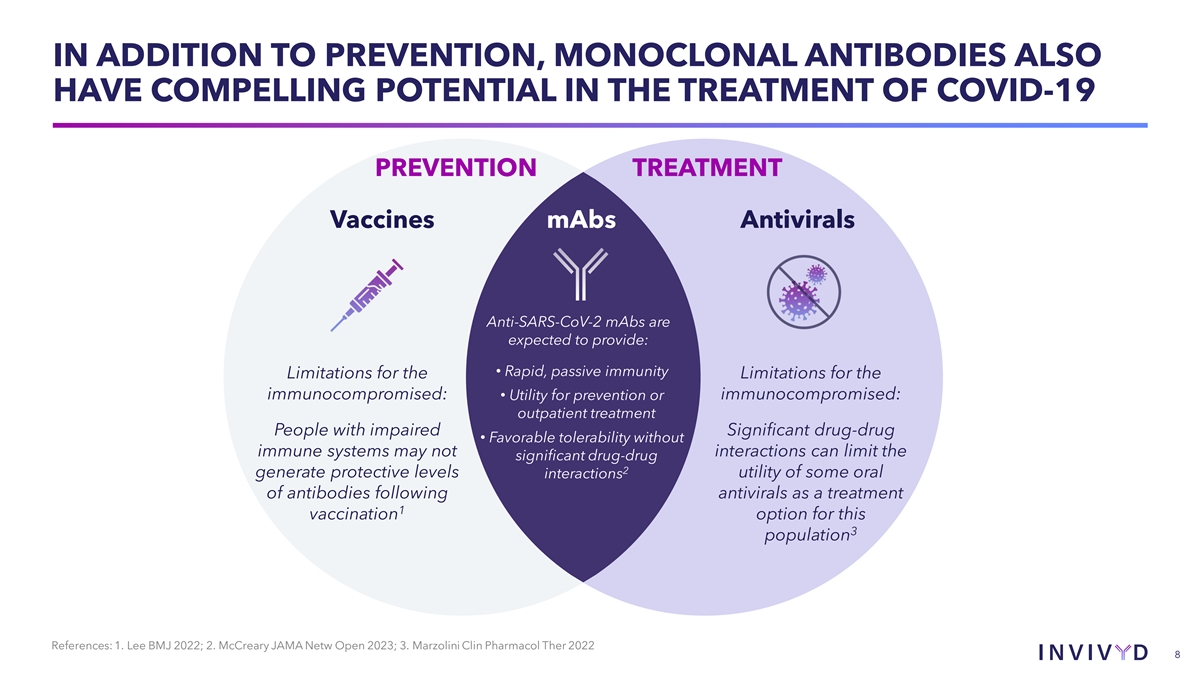
除预防外,单克隆抗体在 COVID-19 预防治疗疫苗的治疗中也具有令人信服的 潜力,抗SARS-CoV-2 单克隆抗体预计将提供:• 免疫功能低下者局限性的快速被动免疫局限性:• 预防或免疫功能低下的用途:门诊治疗受损患者重要药物 • 没有免疫系统的良好耐受性可能无法限制药物 2 的生成 一些口服的保护水平效用抗病毒药物作为治疗后的抗体相互作用这3种人群的1种疫苗接种选择参考文献:1.Lee BMJ 2022;2.McCreary JAMA 网络公开赛 2023;3.Marzolini Clin Pharmacol Ther 2022 8

我们的平台和 VYD222 © 2024 Invivyd, Inc. Invivyd 和 Invivyd 徽标是 Invivyd, Inc. 的商标。本演示文稿中的所有商标均为其各自所有者的财产。
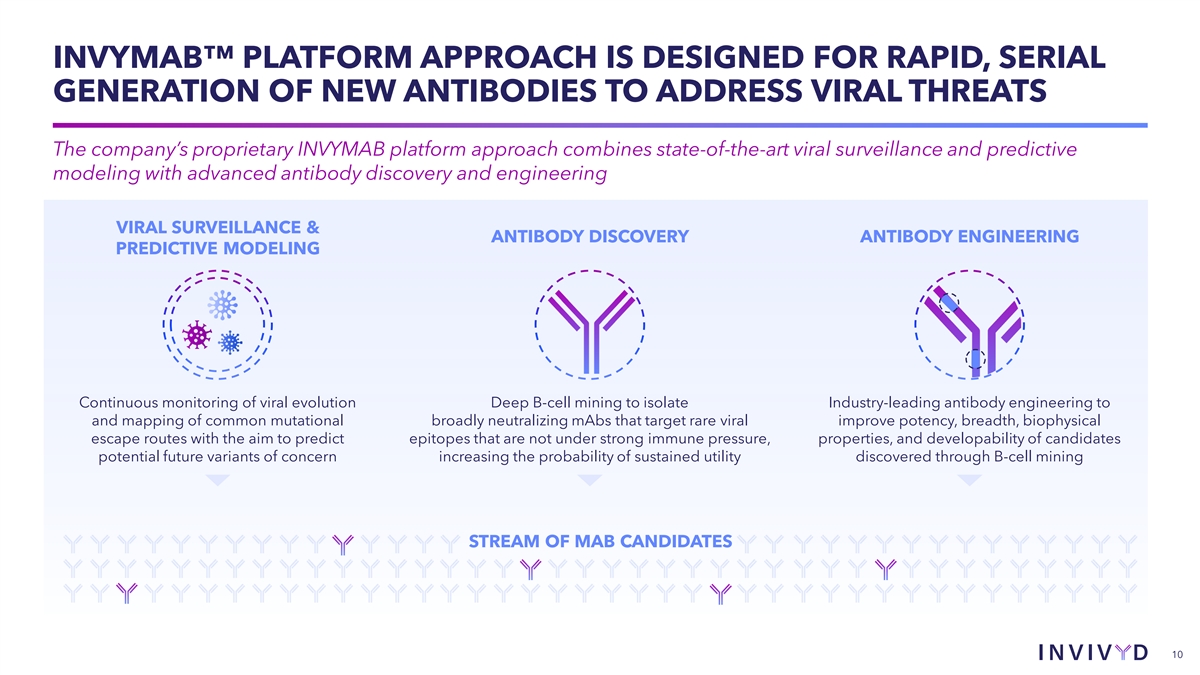
INVYMAB™ 平台方法专为快速、串行 生成新抗体以应对病毒威胁而设计。该公司专有的INVYMAB平台方法将最先进的病毒监测和预测建模与先进的抗体发现和工程病毒监测 和抗体发现抗体工程预测建模持续监测病毒进化深度B细胞挖掘,将行业领先的抗体工程分离到靶向 稀有病毒的常见突变广泛中和单抗体的映射改善效力、广度、生物物理逃生路线,目的是预测不受强免疫压力的表位、特性和候选人的可发育性,潜在的未来值得关注的变种增加了通过B细胞挖掘发现持续效用的可能性 STREAM OF MAB CANDIDATIES 10

VYD222:在 免疫功能低下的成人和青少年中预防 COVID-19 的候选药物 ph 2/3 预防 COVID-19 的 ADG20 临床试验 RBD Spike ACE2 Ph 2/3 对用于 COVID-19 治疗的 ADG20 的临床试验广泛中和、延长半衰期与刺突蛋白受体 结合 由正在开发的用于SARS-CoV-2结合域(RBD)的候选药物阿丁单抗制成,(ADG20),一种单抗候选药物,Invivyd 在暴露前预防 COVID-19 干扰病毒的感染能力,此前 在 2 中进行了研究针对免疫功能低下的成人和人体细胞临床终点的临床试验;来自 EVADE 青少年试验的数据有望加速 VYD222 的开发参考资料:Saxena SK VirusDis 2020(SARS-CoV-2 图)11

VYD222 已显示出对 各种前 OMICRON 和 OMICRON 变体 1 变体亚系 VYD222 WT (D614G) WT (D614G) ✓ Delta B.1.617.2 ✓ BA.4.6 ✓ BF.7 ✓ XBB.1 ✓ XBB.1.5 ✓ XBB.1.16 ✓ 欧密克隆 XBB.1.5.10/EG.5 ✓ HK.3 ✓ BA.2.86 ✓ HV.1 ✓ JN.1 目前是美国占主导地位的 2 SARS-CoV-2 变体。JN.1 ✓ 参考文献:1.CRO 使用伪病毒 SARS-CoV-2 中和 ✓ 中和活性在 体外伪病毒测定抗体分析中使用伪病毒 SARS-CoV-2 中和活性生成的 VYD222 数据;2. https://covid.cdc.gov/covid-data-tracker/#variant-proportions(2024 年 1 月 5 日访问)12
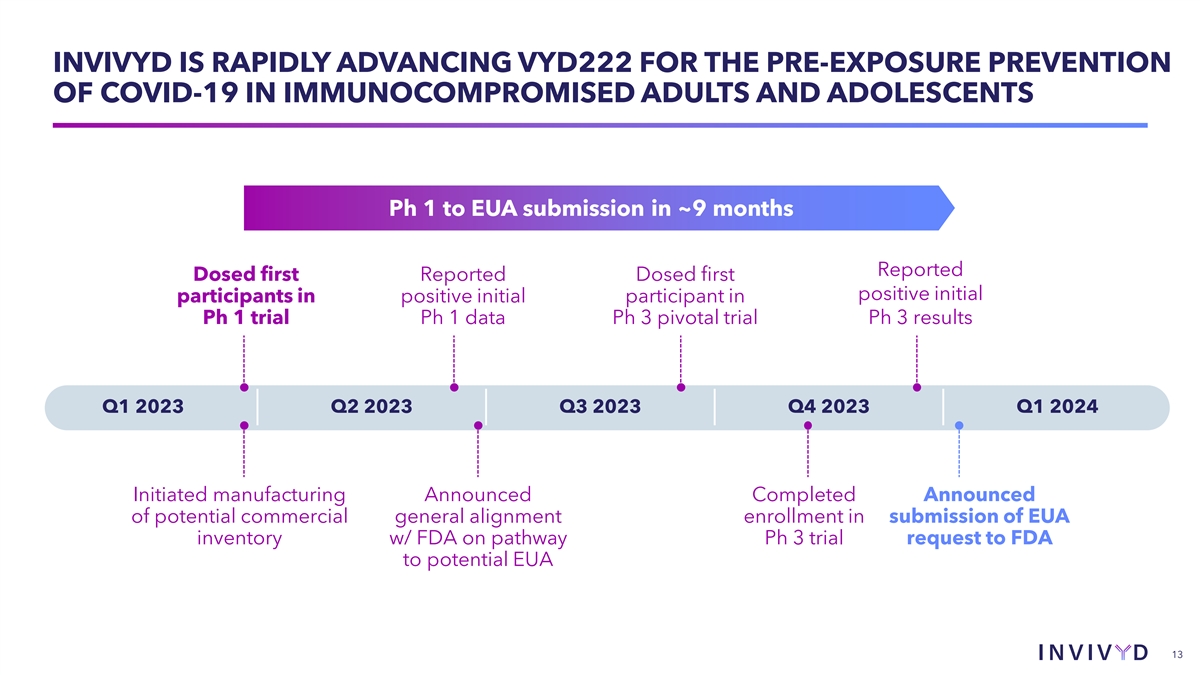
INVIVYD 正在大约 9 个月内快速推进免疫功能低下成人和青少年 COVID-19 的暴露前预防 Ph 1 至 EUA 的预防 Ph 1 试验阳性初始参与者的剂量 Ph 1 数据第 3 阶段关键试验 Ph 3 结果 2023 年第一季度第三季度2023 年第四季度启动制造业宣布欧盟提交的潜在商业通用校准注册已完成美国食品和药物管理局关于向美国食品和药物管理局提出的 Ph 3 试验申请的清单(潜在的美国 13)VYD222
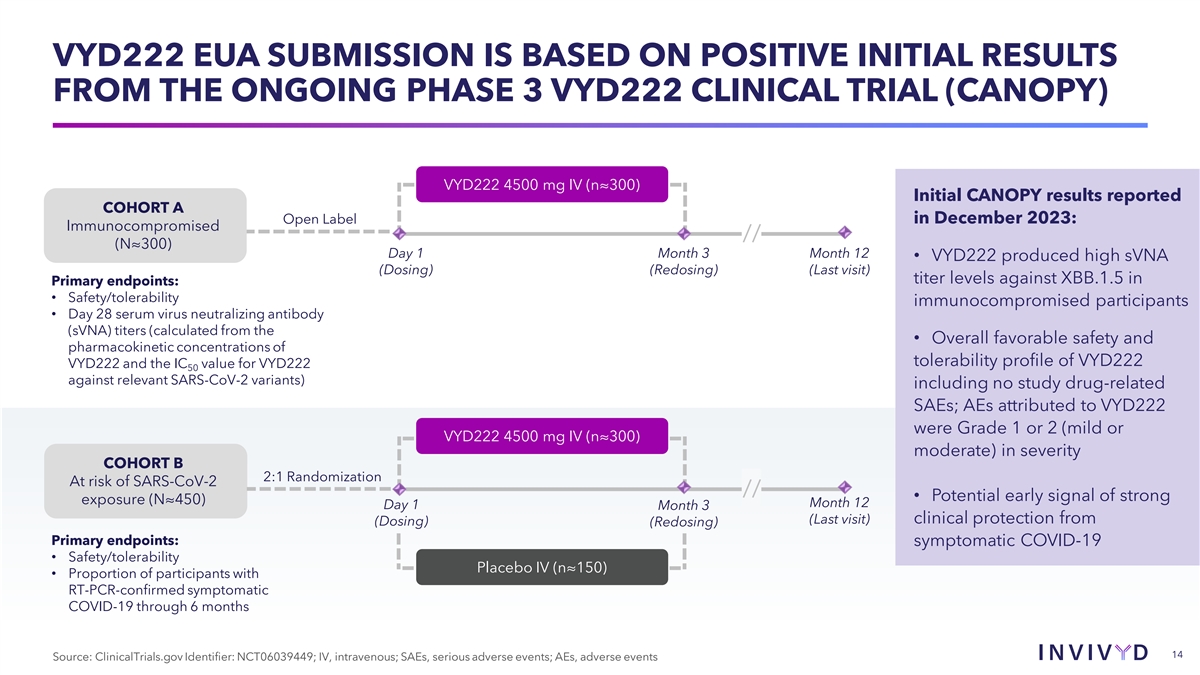
VYD222 EUA 提交的依据是 正在进行的第 3 期 VYD222 临床试验 (CANOPY) VYD222 4500 mg IV (n√300) CANOPY 的初步结果报告了 2023 年 12 月的 A Open Label 队列:免疫功能低下//(N√300) 第 1 天 3 个月 12 • VYD222 产生了较高的 svNA(剂量) (再给药)(上次访问)滴度水平,而初级组 XBB.1.5 终点:• 安全性/耐受性免疫受损的参与者 • 第 28 天血清病毒中和抗体 (svNA) 滴度(根据 • 总体良好 安全性和药代动力学计算得出VYD222(VYD222 耐受性浓度,对照相关 SARS-CoV-2 变体)和 VYD222 50 的 IC 值(不包括研究药物相关的 SAE);归因于 VYD222 的 AE 的严重程度为 1 级或 2 级(轻度或 VYD222 4500 mg IV(n√300)中度)队列 B 2:1 随机分配 SARS-CoV-2 风险// • 潜在的强暴露早期信号(N√450)第 12 天 1 个月 3(上次访问)) 针对(剂量)(再给药)的临床保护 主要终点:有症状的 COVID-19 • 安全性/耐受性安慰剂 IV(n√150)• 使用 RT-的参与者比例PCR 证实在 6 个月内出现症状的 COVID-19 14 来源:ClinicalTrials.gov 标识符:NCT06039449;静脉注射, 静脉注射;SAE,严重不良事件;AE,不良事件

如果获得授权,INVIVYD 的目标是尽快将 VYD222 在美国上市。此后,商业准备工作由一支在传染病领域成功实现产品商业化经验的经验丰富的团队领导。准备工作已经完成或正在进行中:上市规划(例如, 市场研究、市场规模/细分、品牌战略、战地力量规模)市场准入活动(例如付款人/定价研究、分销渠道)制造初始商业库存建立必要的内部系统以及支持向商业阶段过渡的 技术 Invivyd 计划最初通过高度集中的现场销售组织专注于为风险最高的 IC 人群提供服务,如果 VYD222 获得批准,该组织可以随着时间的推移扩展到更多的 IC 成人和青少年 青少年 15
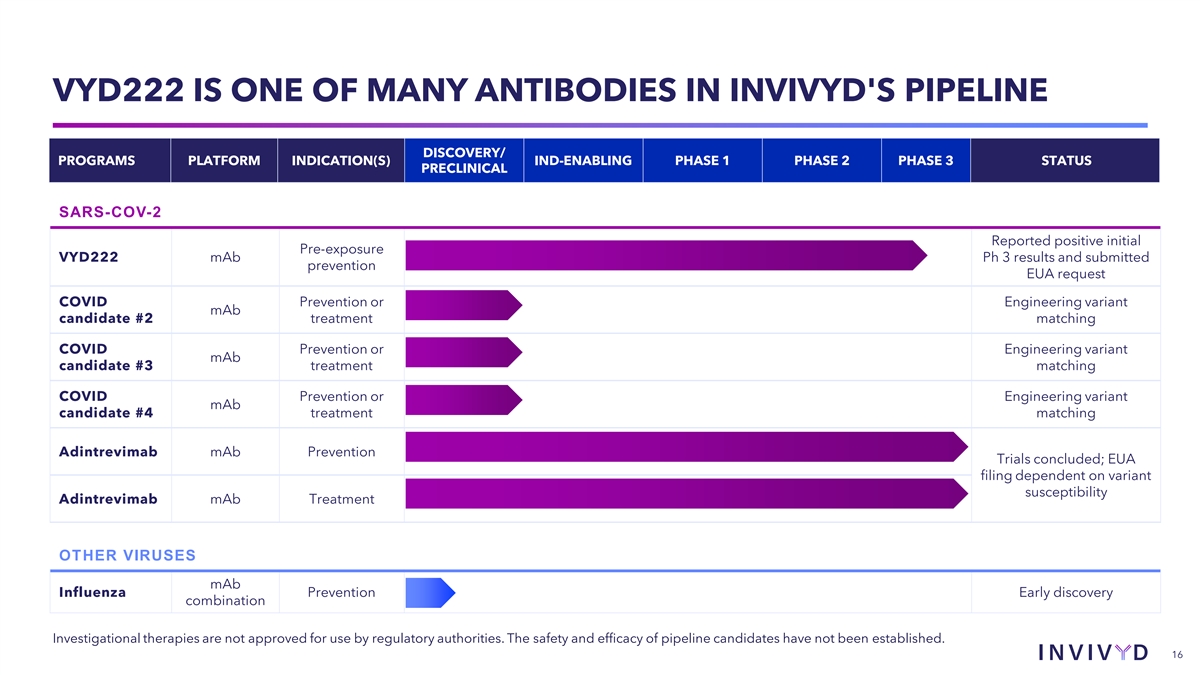
VYD222 是 INVIVYD 管道中的众多抗体之一 DISCOVERY/ 项目平台适应症(S)支持IND的第 1 阶段 2 期 3 期状态临床前 SARS-COV-2 报告了初始暴露前阳性 VYD222 maB Ph 3 结果并提交了预防 EUA 申请 COVID 预防或工程变体 maB 候选药物 #2 与 COVID 预防或工程变体单抗候选药物 #3 治疗匹配 Adintrevitrevity mab mAb 预防试验结束;EUA 申请 依赖性 #4关于变异易感性 Adintrevimab 单抗治疗其他病毒单抗流感预防早期发现组合研究疗法未获监管机构批准使用。管道 候选药物的安全性和有效性尚未确定。16

具有传染病专业知识和成功记录的管理团队 彼得·施密特,医学博士,斯泰西·普莱斯理学硕士,威廉·杜克女士,工商管理硕士戴夫·赫林,工商管理硕士首席医疗官首席技术和制造官首席财务官兼董事吉尔·安德森,法学博士 杰里米·高勒首席运营官兼公司秘书罗伯特·艾伦博士商务官首席科学官 17

谢谢!