目录
独立审查对IGNYTE-ESO中期分析的回应
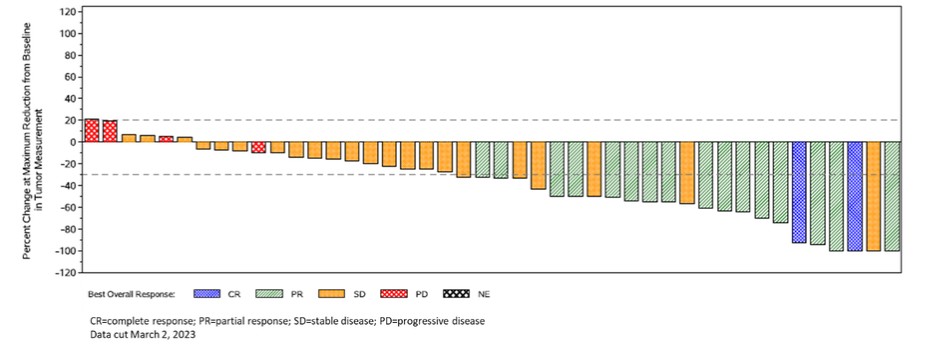
| ● | SURPASS-3 第 2 阶段试用 ADP-A2M4CD8 瞄准了 MAGE-A4。 针对耐铂卵巢癌患者的2期试验已经启动。我们已获得美国食品药品管理局颁发的 ADP-A2M4CD8 的 RMAT 称号(再生医学高级疗法称号),用于治疗该适应症。在SURPASS的1期试验中,欧洲肿瘤内科学会(“ESMO”)于2023年10月报告卵巢癌(6/15人接受治疗)的ORR为40%,有一项完全反应和5项部分反应。2 期试验将评估 ADP-A2M4CD8 在耐铂卵巢癌中的单一疗法和与检查点抑制剂 nivolumab 联合使用的情况。 |
我们的 MAGE-A4 靶向 TCR-T 细胞疗法 (ADP-A2M4CD8) 的早期临床试验正在进行中。
| ● | 使用 ADP 进行超越 1 期试验-A2M4CD8: ADP-A2M4CD8 的 1 期试验正在招募中,重点是治疗表达 MAGE-A4 抗原的头颈癌和尿路上皮癌患者,以及早期线路治疗环境中的患者。该试验的最新数据已于 2023 年 10 月在 ESMO 上公布。在所有适应症中,该试验报告的总体反应率为35%。在26名卵巢癌、尿路上皮癌和头颈癌患者中,反应率为50%,在先前接受3线或更少治疗的患者中,反应率提高到75%。该试验包括一个组合队列,参与者接受 ADP-A2M4CD8 和检查点抑制剂(nivolumab)的组合。组合队列的早期数据已于 2023 年 10 月在 ESMO 上公布,并且仍在不断变化。截至2023年8月14日,组合队列中有一位患者出现了确诊反应。在数据中断之后,又有一份已确认的回应。 |
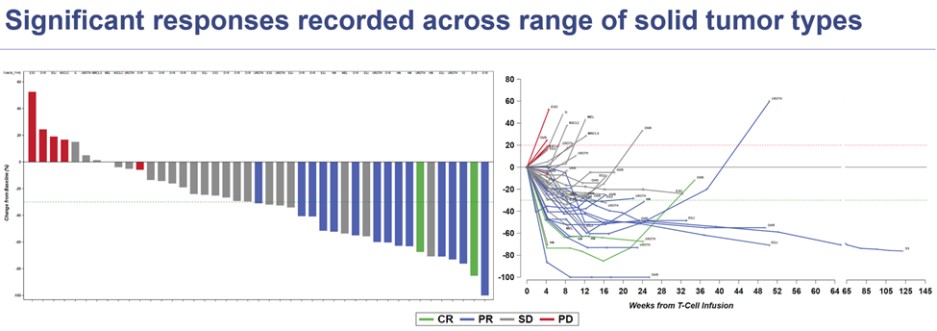
cr=完全反应;pr=部分反应;sd=稳定性疾病;pd=进行性疾病;ESMO 2023 年数据截止 8 月 1 日4, 2023
27