展品99.2

投资者介绍2023年1月

前瞻性陈述本演示文稿包含涉及重大风险和不确定因素的前瞻性陈述。根据1995年《私人证券诉讼改革法》对前瞻性陈述的定义,前瞻性陈述是指非历史事实的陈述,涉及大量风险和不确定因素。本文中的“可能”、“将”、“应该”、“可能”、“将”、“预期”、“计划”、“预期”、“相信”、“估计”、“项目”、“预测”、“打算”、“潜在”、“继续”、
和类似的表述(以及涉及未来事件、条件或情况的其他词语或表述)可能是前瞻性表述。本演示文稿中的前瞻性陈述基于公司当前的预期和信念,涉及已知和未知的风险、不确定因素和其他因素,这些因素可能会导致公司的实际结果、业绩和成就以及某些事件的时间与任何前瞻性陈述中讨论、预测、预期或表明的结果、业绩、成就或时间大不相同。此类风险、不确定性和其他因素包括但不限于以下因素:美国、欧洲或日本以外的Arikayce或公司在美国、欧洲、日本或其他市场的候选产品未能获得或延迟获得监管批准,包括每个市场和每种用途对Lamira®雾化系统和其他产品候选设备的单独监管批准;未能成功将公司唯一批准的产品Arikayce在美国商业化。, 欧洲或日本(分别为阿米卡星脂质体吸入剂、590毫克脂质体雾化器分散体和阿米卡星吸入药物制品),或维持美国、欧洲或日本对Arikayce的批准;灾难或其他事件造成的商业或经济中断,包括自然灾害或公共卫生危机;新冠肺炎大流行的影响和减少其对公司业务、员工(包括关键人员、患者、合作伙伴和供应商)的传播的努力;在正在进行的和未来的临床研究(包括Aspen研究)中,Brensocatib对患者没有被证明有效或安全的风险;在正在进行的和未来的临床研究中,TPIP被证明对患者没有有效或安全的风险;
医生、患者、第三方付款人和医疗保健社区中的其他人对Arikayce的市场接受程度的不确定性;公司无法获得美国食品和药物管理局对Arikayce的完全批准,包括公司无法成功或及时完成验证患者报告结果工具的研究和完全批准Arikayce所需的确认性上市后临床试验的风险;公司无法, Pari或公司其他第三方制造商未遵守与Arikayce或Lamira®雾化器系统相关的法规要求;公司无法从政府或第三方付款人处获得Arikayce的足够补偿或Arikayce的可接受价格;与Arikayce或公司的候选产品相关的意外安全或疗效问题;公司对Arikayce、Brensocatib、TPIP或公司其他候选产品的潜在市场规模的估计不准确,或公司用来确定医生、患者吸收预期比率、预期治疗持续时间或预期患者依从率或停用率的数据不准确;与我们由Pharmakon Advisors,LP管理的某些基金担保的优先贷款以及我们与OrbiMed Royalty&Credit Opportunities IV,LP进行的特许权使用费融资相关的风险和不确定性,以及预期的好处, 包括我们遵守优先担保贷款和特许权使用费融资协议中的约定的能力,以及根据这些协议对我们
运营的限制的感知影响;公司无法创建有效的直销和营销基础设施,或与提供此类基础设施的第三方合作,以便在未来分销Arikayce或任何经批准的公司候选产品;未能获得监管部门的批准,无法将Arikayce的适应症扩大到更广泛的患者群体;公司的竞争对手可能获得与公司为特定适应症开发的产品基本相同的产品的孤立药物独家经营权的风险;未能成功预测新基因疗法产品的开发、监管批准和商业化的时间和成本
;未能成功进行Arikayce、Brensocatib、TPIP和公司其他候选产品的未来临床试验,原因是公司在进行临床前开发活动和监管批准所需的临床试验方面的经验有限,以及可能无法招募或留住足够的患者来进行和完成试验或生成监管批准所需的数据等;公司的临床研究可能会被推迟或在药物开发期间发现严重的副作用;公司所依赖的第三方未能生产足够数量的Arikayce或公司用于商业或临床需求的候选产品,无法进行公司的临床试验, 或遵守影响公司业务或与公司的协议的公司协议或法律法规;公司无法吸引和留住关键人员或有效管理公司的增长;公司无法成功整合其最近的收购并适当管理管理层投入整合活动的时间和注意力;公司收购的技术、产品和候选产品在商业上不成功的风险;本公司无法适应其竞争激烈且不断变化的环境;本公司无法维持其重要客户的风险;政府医疗改革大幅增加本公司的成本并损害其财务状况的风险;本公司无法充分
保护其知识产权或阻止披露其商业秘密和其他专有信息,以及与此类事项相关的诉讼或其他诉讼程序的费用;与Arikayce或公司的候选产品相关的协议对公司施加的限制或其他义务,包括与Pari和阿斯利康AB的许可协议,以及公司未能履行此类协议规定的义务;
公司正在或可能成为其中一方的诉讼造成的成本和潜在的声誉损害, 包括产品责任索赔;公司运营在发生网络安全攻击或问题时受到重大中断的风险;与公司企业资源规划系统升级相关的业务中断或费用;公司有限的国际运营经验;适用于公司业务的法律法规的变化,包括任何定价改革,以及未能遵守此类法律法规;本公司的经营亏损历史,以及本公司可能永远无法实现或维持盈利的可能性;影响本公司经营业绩和财务状况的商誉减值费用;无力偿还本公司现有的债务以及与本公司获得未来资本的能力有关的不确定性;以及延迟执行经相关监管机构批准的额外第三方制造设施的计划,以及与该等计划相关的意外支出。公司可能无法实际实现公司的前瞻性陈述所表明的结果、计划、意图或预期,因为从本质上讲,前瞻性陈述涉及风险和不确定性,因为它们与事件有关,
取决于未来可能发生或可能不发生的情况。有关可能影响公司业务的风险和不确定因素的更多信息,请参阅公司截至12月31日的年度报告10-K表中第1A项“风险因素”中讨论的因素, 2021年和任何后续公司向美国证券交易委员会(美国证券交易委员会)提交的文件。本公司告诫读者不要过度依赖任何此类
前瞻性陈述,这些陈述仅在本演示文稿发表之日发表。除法律和美国证券交易委员会规则特别要求外,本公司不承担任何义务公开更新或修订任何此类陈述,以反映任何此类陈述可能基于的预期或事件、条件或情况的任何变化,或可能影响实际结果与前瞻性陈述中陈述的结果大相径庭的可能性
。

通过利用为经历重大健康问题的小患者群体提供的改变生活的疗法组合产生的收入
打造可持续发展的生物技术公司-5年愿景

未来18个月将是该公司…历史上最具变革性的一年现金>10亿美元用于支持近期拐点商业引擎有望在2022年实现30%的收入增长预计2023年收入将达到2.85亿至3亿美元到期PIPELIN我们每个计划的临床数据在2023-2024年期间
这是您希望在Insmed建立地位的一年。4.
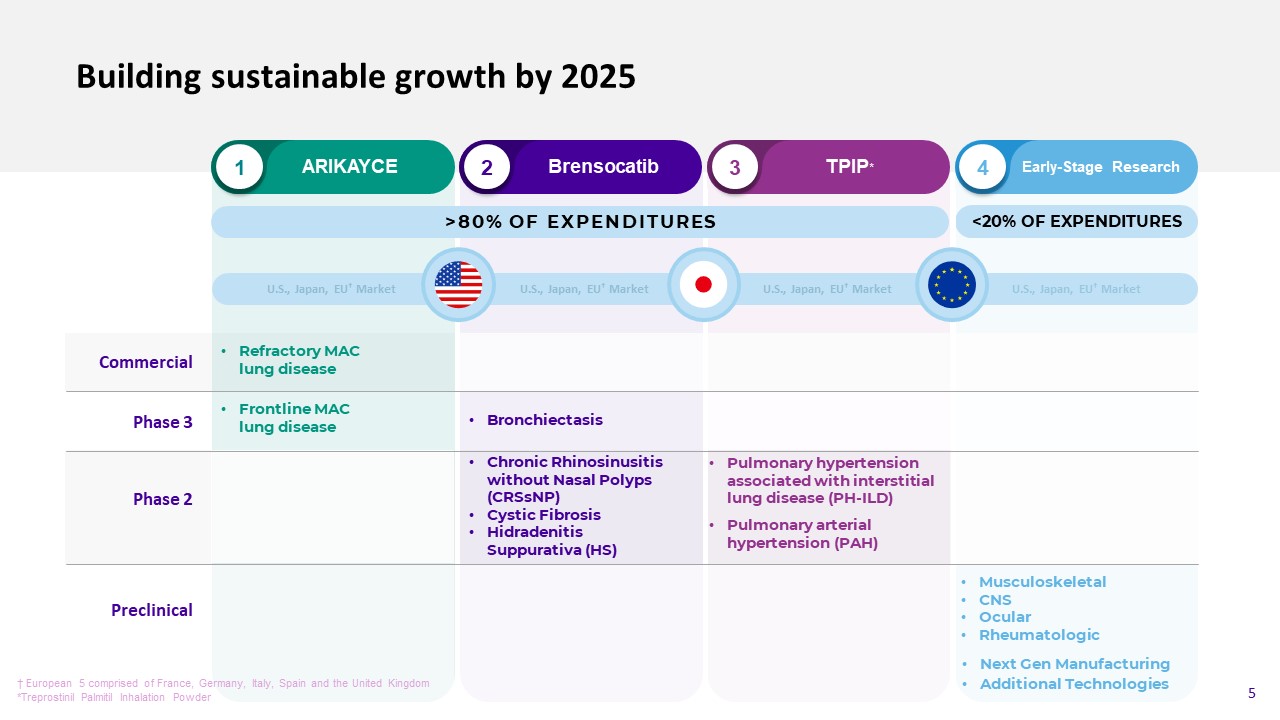
到2025年建立可持续增长商业1 2 3 4 Arikayce Brensocatib TPIP*早期研究难治性MAC肺病前线MAClung疾病下一代制造额外技术阶段3支出的80%无鼻息肉(CRSsNP)化脓性囊性纤维症(HS)美国、日本、欧盟†市场†欧洲5包括法国、德国、意大利、西班牙和英国*Treprostinil Palmil吸入粉5
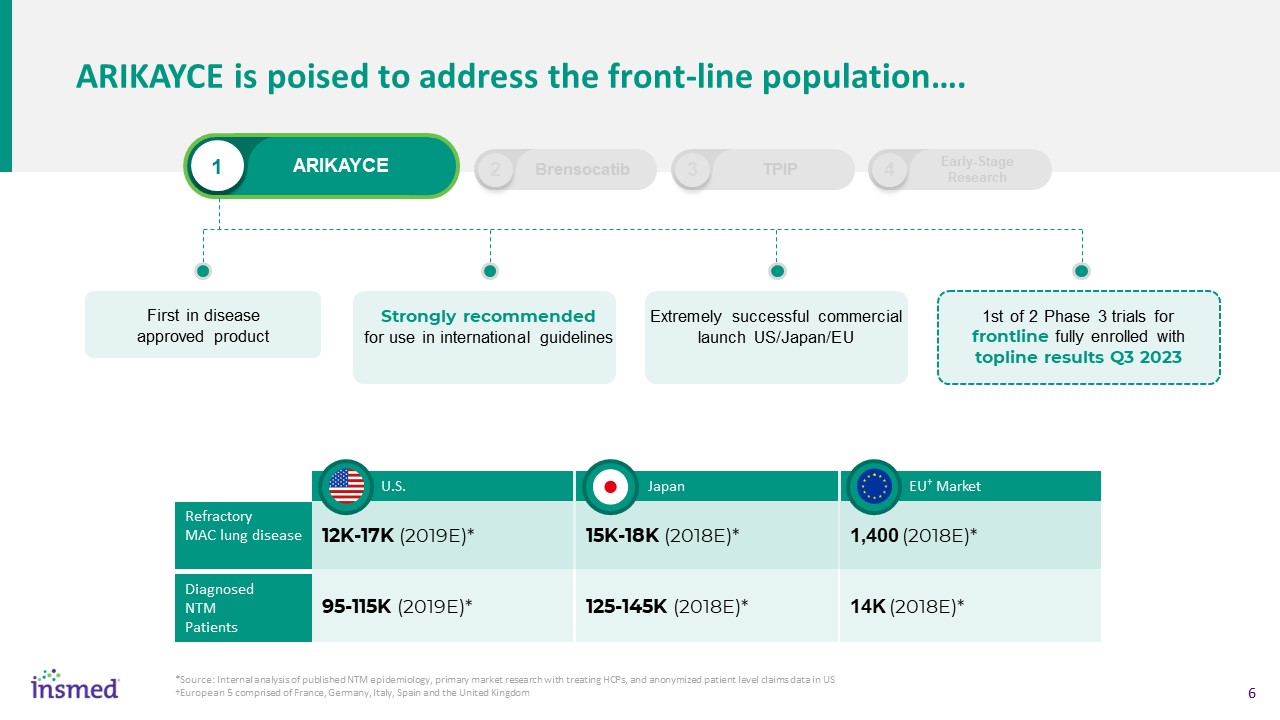
1 Arikayce Arikayce准备向一线人口…发表讲话。首个疾病批准产品强烈推荐用于国际指南非常成功的商业启动美国/日本/欧盟第一个完全纳入TOPLINE的2期3期试验结果Q3 2023 12K-17K(2019E)*95-115K(2019E)*美国难治性肺病诊断NTMPatients 15K-18K(2018E)*125-145K(2018E)*日本1,400(2018E)*14K(2018E)*欧盟†市场2 Brensocatib 3 TPIP 4早期-Stage Research*来源:
已发表的NTM流行病学内部分析,治疗HCP的主要市场研究,以及由法国、德国、意大利、西班牙和英国组成的美国†欧洲5国的匿名患者水平索赔数据
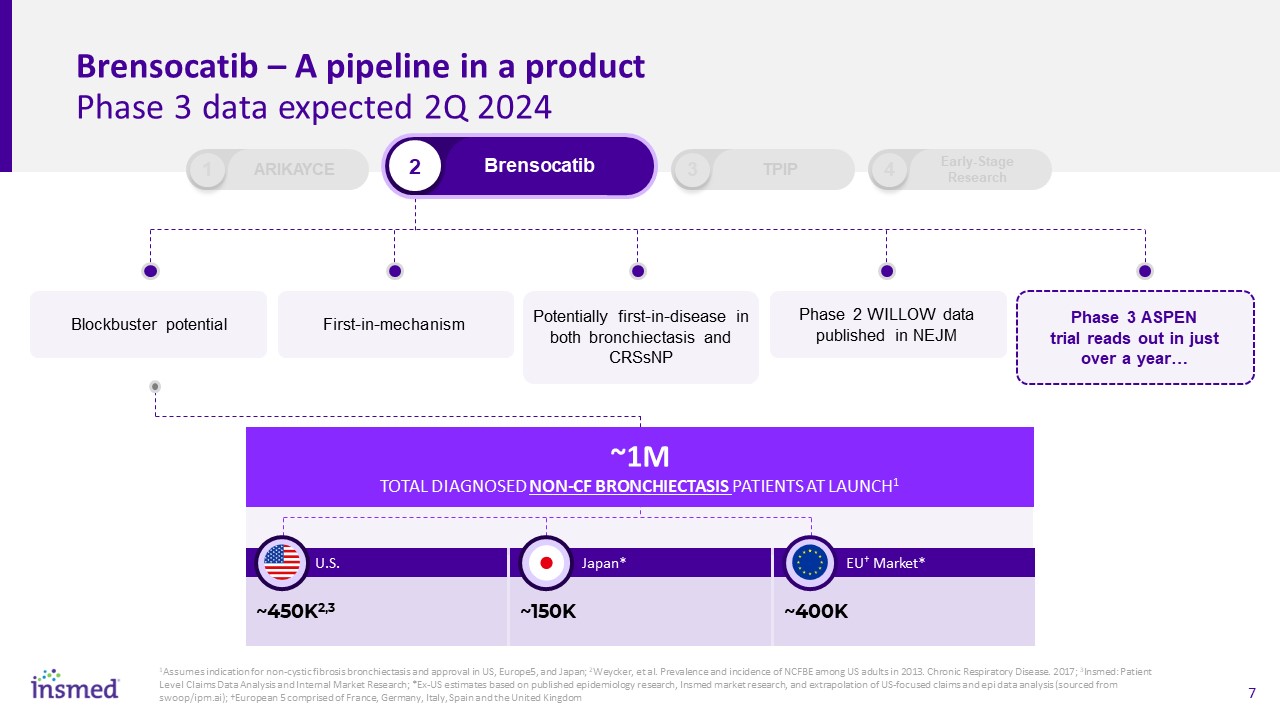
Brensocatib-产品第三阶段的流水线数据预计2024年第二季度
Blockbuster Potential 2 Brensocatib 1 Arikayce 3 TPIP 4早期机制研究第一机制潜在的CRSsNP第二阶段疾病在支气管扩张症和CRSsNP第二阶段数据发表在《新英格兰医学杂志》第三阶段Aspen试验
在一年多一点的时间里…1美国、欧洲和日本对非囊性纤维性支气管扩张症的适应症和批准;2Weycker等人。2013年美国成年人中NCFBE的患病率和发病率。慢性呼吸系统疾病:2017年;3调查:患者水平索赔数据分析和内部市场研究;*基于已发表的流行病学研究、深入的市场研究以及以美国为重点的索赔和EPI数据分析的外推的美国估计;†欧洲5由法国、德国、意大利、西班牙和英国组成†~450K2,3美国~150K日本*~400K欧盟†市场*~LAUNCH1诊断的总共100万名非CF型支气管扩张症患者
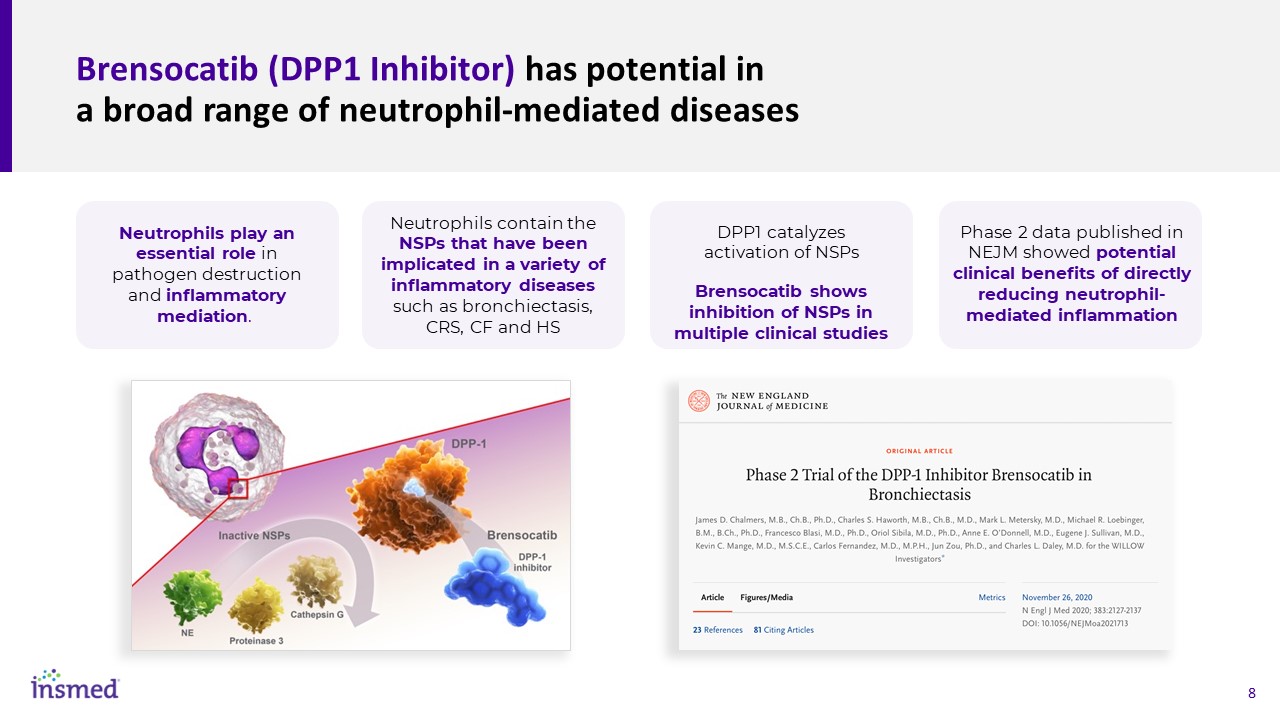
Brensocatib(DPP1抑制剂)在广泛的中性粒细胞介导的疾病中具有潜在的作用中性粒细胞在病原体破坏和炎症调节中发挥着重要作用。中性粒细胞含有与多种炎症性疾病有关的NSP,如支气管扩张、CRS、CF和HS DPP1催化NSP的激活。Brensocatib在多项临床研究中显示对NSP的抑制作用发表在《新英格兰医学杂志》上的第二阶段数据显示,直接减轻中性粒细胞介导的炎症具有潜在的临床益处
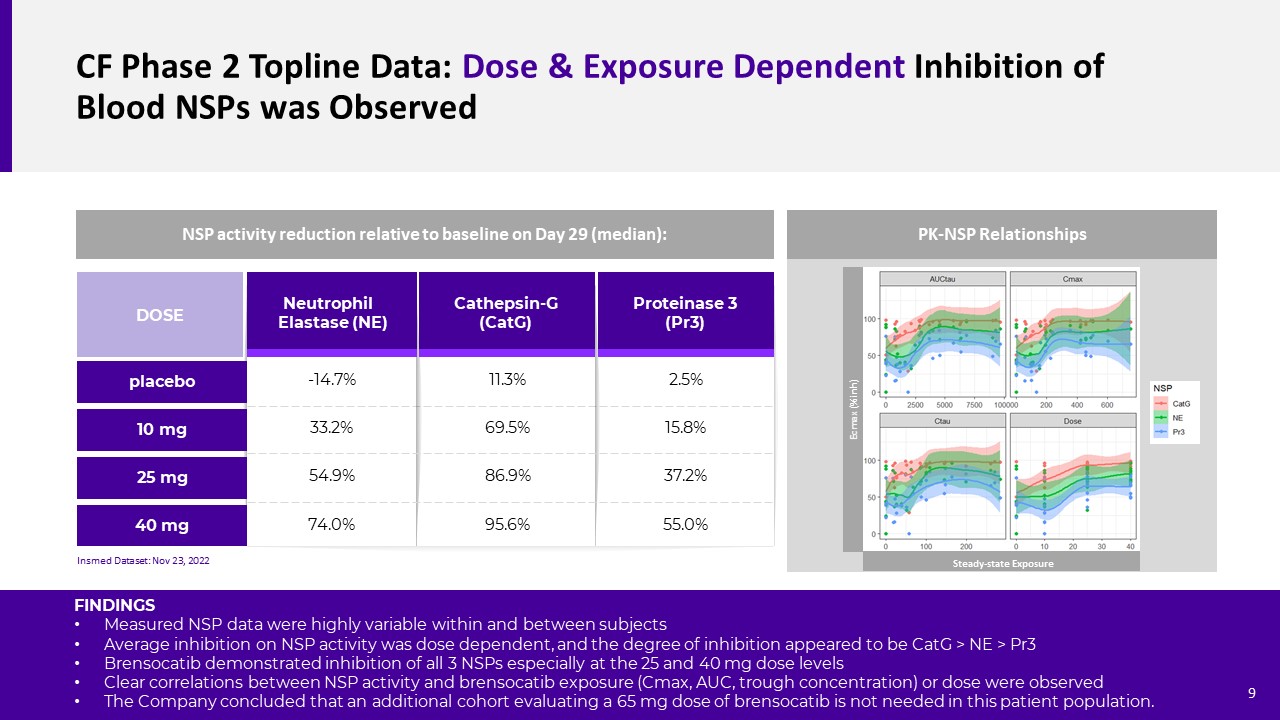
Cf第二阶段拓扑线数据:观察到血液中NSP受到剂量和暴露的抑制
组织蛋白酶-G(CATG)蛋白3(PR3)中性粒细胞弹性蛋白酶(NE)10 mg 25 mg剂量40 mg安慰剂-14.7%33.2%54.9%74.0%11.3%69.5%86.9%95.6%2.5%15.8%37.2%55.0%NSP活性相对降低
至第29天的基线(中位数):输入数据集:11月23日,2022年PK-NSP关系研究结果在受试者内部和受试者之间测量的NSP数据高度可变,对NSP活性的平均抑制程度似乎是CATG>NE>PR3。Brensocatib显示对所有3种NSP的抑制,特别是在25和40 mg剂量水平上。观察到NSP活性与Brensocatib暴露(Cmax、AUC、谷浓度)或剂量之间存在明显的相关性。该公司的结论是,在该患者群体中不需要额外评估65 mg剂量的Brensocatib。Ecmax(%inh)稳态暴露9
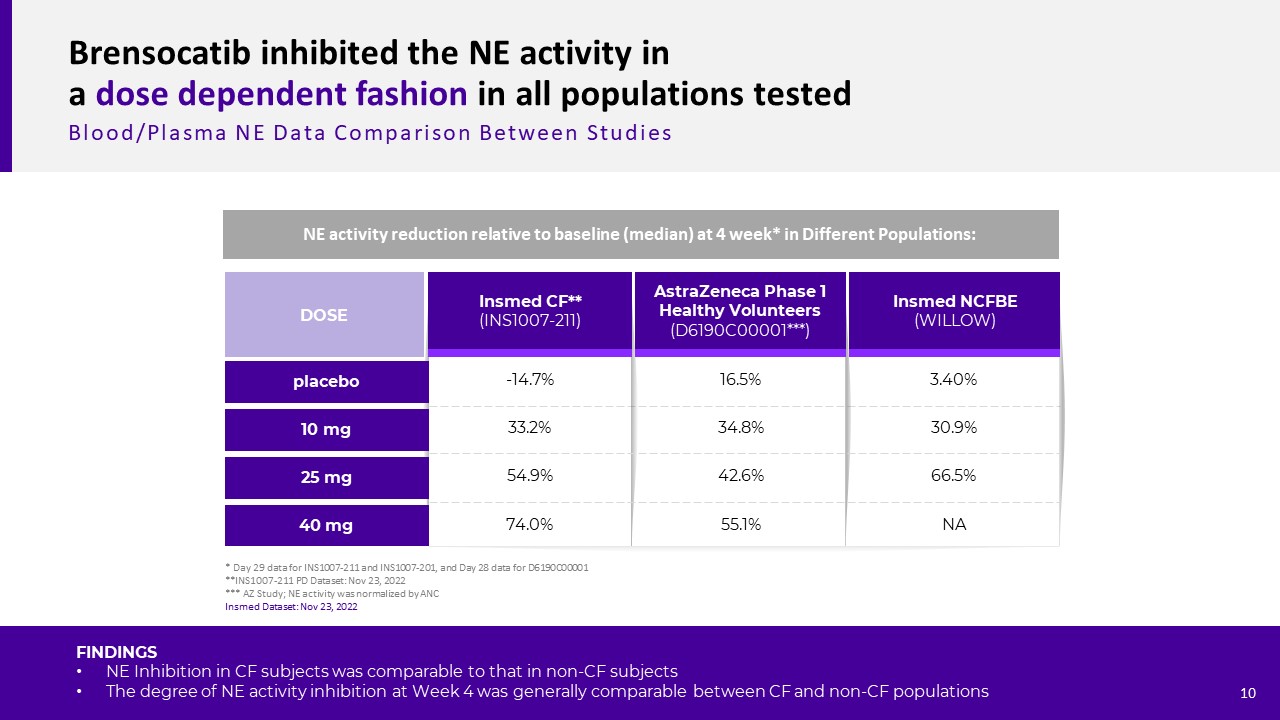
Brensocatib以剂量依赖的方式抑制所有受试人群的NE活性血液/血浆NE数据阿斯利康1期健康志愿者(D6190C00001*)注射NCFBE(Willow)CFF**(INS1007-211)10 mg 25 mg剂量40 mg安慰剂-14.7%33.2%54.9%74.0%16.5%34.8%42.6%55.1%3.40%30.9%66.5%NA不同人群在4周*的NE活性较基线(中位数)下降:*INS1007-211和INS1007-201的第29天数据,D6190C00001**INS1007-211 PD数据集的第
28天数据:2022年11月23日*AZ研究;NE活性通过ANC归一化。结果发现,慢性肺心病患者和非慢性肺心病患者的NE抑制程度相当。第4周的NE活性抑制程度在慢性肺心病和非慢性肺病人群中大致相似。10输入数据集:2022年11月23日
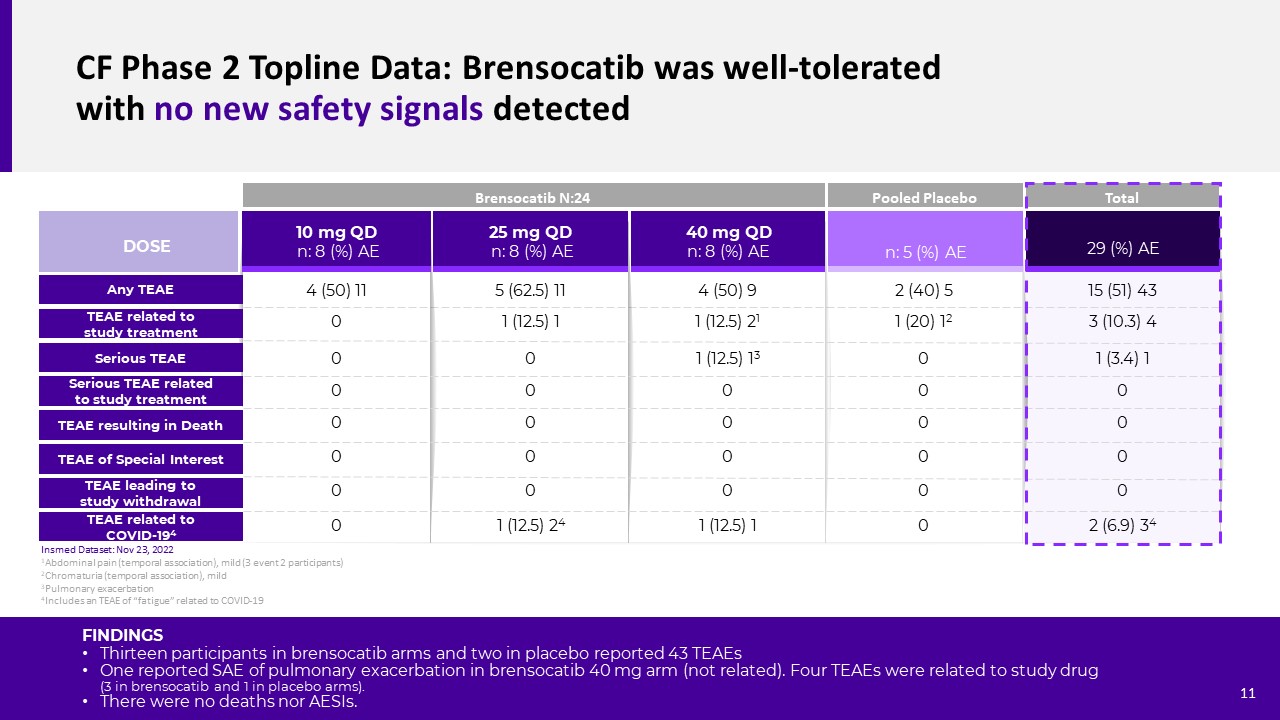
Cf第二阶段TOPLINE数据:Brensocatib耐受性良好,没有新的安全信号检测到
结果13名Brensocatib组和2名安慰剂组参与者报告了43个TEAE,一个报告了Brensocatib 40 mg组肺恶化的SAE(无关)。有4例TEAEs与研究药物有关(3例服用brensocatib,1例服用安慰剂)。没有死亡病例,也没有AESIs病例。25 mg QD n:8(%)AE 40 mg QD n:8(%)AE 10 mg QD n:8(%)AE TEAE与研究相关治疗严重TEAE剂量严重TEAE与研究相关
治疗任何TEAE n:5(%)AE 4(50)9 1(12.5)21 1(12.5)13 0 Brensocatib N:24与COVID-194 TEAE相关的混合安慰剂TEAE总TEAE与COVID-194 TEAE相关死亡00 1(12.51 TEAE导致研究退出5(62.5)11 1(12.5)1 00 00 01(12.5)24 4(50)11 00 00 00 2(40)51(20)12 00 00 00 15(51)43 3(10.3)4 1(3.4)1 00 00 2(6.9)34 1腹痛(暂时性联想),
轻度(3个事件2参与者)2色尿(时间关联),3轻度3肺恶化4包括与新冠肺炎11相关的TEAE“疲劳”INSMED数据集:2022年11月23日

通过MOA治疗的潜在潜在市场是:巨大的CRSsNP~400K4,5,6,7可寻址患者WW(严重人群)没有批准的治疗方法~7000万CRSsNP1患者,但许多患者对皮质类固醇和/或内窥镜鼻窦手术(ESS)囊性纤维化~70K8,9 WW诊断患者没有批准的针对中性粒细胞介导性炎症的抗炎治疗,中性粒细胞介导的炎症是恶化和疾病进展的关键驱动力HS~100K中到重度患者,对于需要多种治疗和/或手术来管理疾病的患者来说,目前的11种方法是沉重的负担多达670万名患者超出了启动的重点没有批准的治疗方法约170万名未诊断的患者/误诊为COPD或哮喘1、2+~230万至500万未诊断的BE患者/合并COPD2、31潜在的未诊断或误诊(COPD、哮喘)是根据医学专家驱动的见解估计的美国患者
使用先进的分析/统计方法应用于患者级别的索赔数据;2EX-US基于已发表的流行病学研究、Insmed市场研究以及对以美国为重点的索赔和EPI数据分析的推断(来自swoop/ipm.ai);3潜在的未诊断或(患有COPD)BE患者基于对16项EPI研究的内部荟萃分析得出的美国BE患者,这些研究着眼于COPD患者的BE患病率;4Cho et。无鼻息肉的慢性鼻窦炎J变态反应性Clin免疫实践。2016;4(4):575-582。DOI:10.1016/j.jaip.2016.04.015;5 Benjamin et.无鼻息肉的慢性鼻窦炎患者的临床特点学术环境中的J变态反应CLIN免疫练习卷7, 第3号,2019年3月;6患者级别索赔数据分析仅美国(科莫多健康),患者病史中没有Dx代码的积极管理的CRS患者的比例;外推到欧洲和日本5和日本;7仅美国患者级别索赔数据分析(科莫多健康),患有ESS的积极管理的CRSsNP患者的比例;推断到欧洲和日本;8CF基金会,https://www.cff.org/intro-cf/about-cystic-fibrosis;9囊性纤维化
杂志,https://www.cysticfibrosisjournal.com/action/showFullTableHTML?isHtml=true&tableId=t0015&pii=S1569-1993%2816%2930655-5;10Phan等人,化脓性汗腺炎的全球流行和地理变异-系统回顾和荟萃分析生物医学皮肤学(2020)4:2;11 Puri,Ajay:化脓性汗腺炎高管洞察,2019年11月*化脓性汗腺炎
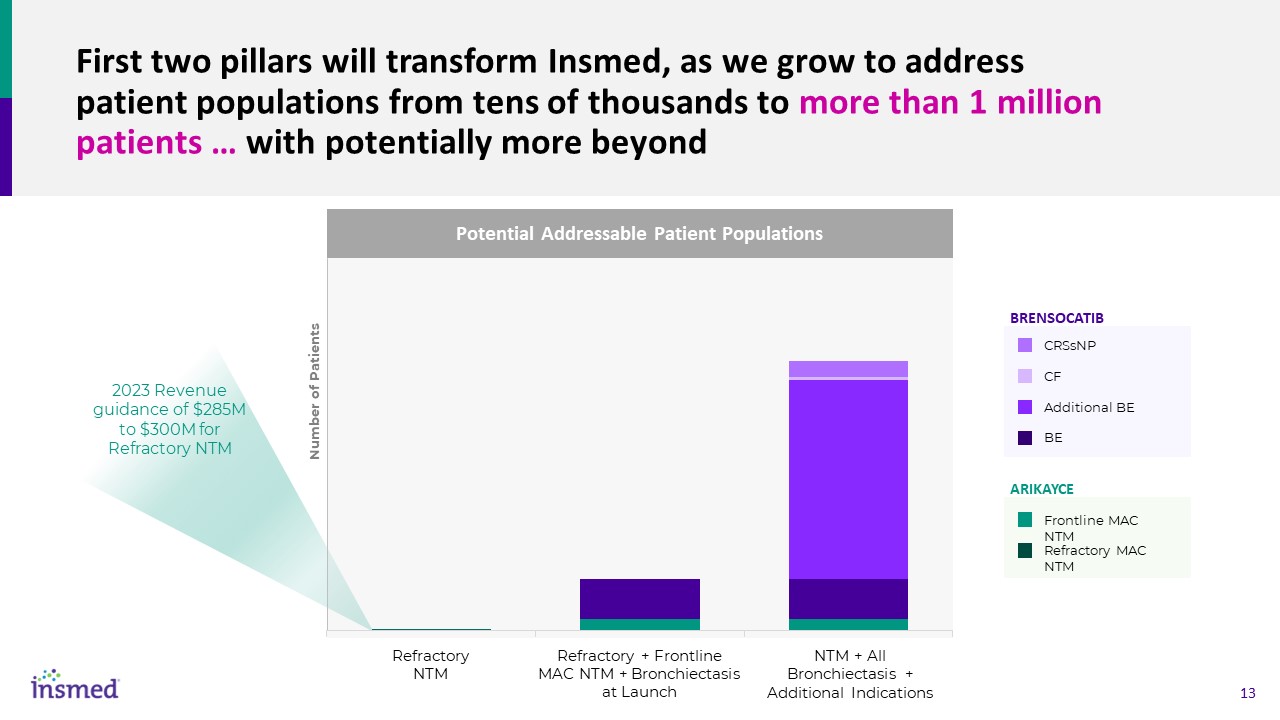
前两个支柱将改变Insmed,因为我们将满足患者
群体从数万到100多万患者…的需求除了潜在可寻址的患者群体外,可能还有更多难治性NTM+所有支扩+其他适应症难治性+前线MAC NTM
+推出时支扩BRENSOCATIB Arikayce CRSNP CF附加BE前线MAC NTM难治性MAC NTM 2023收入指导2.85亿至3亿美元用于难治性NTM患者数量
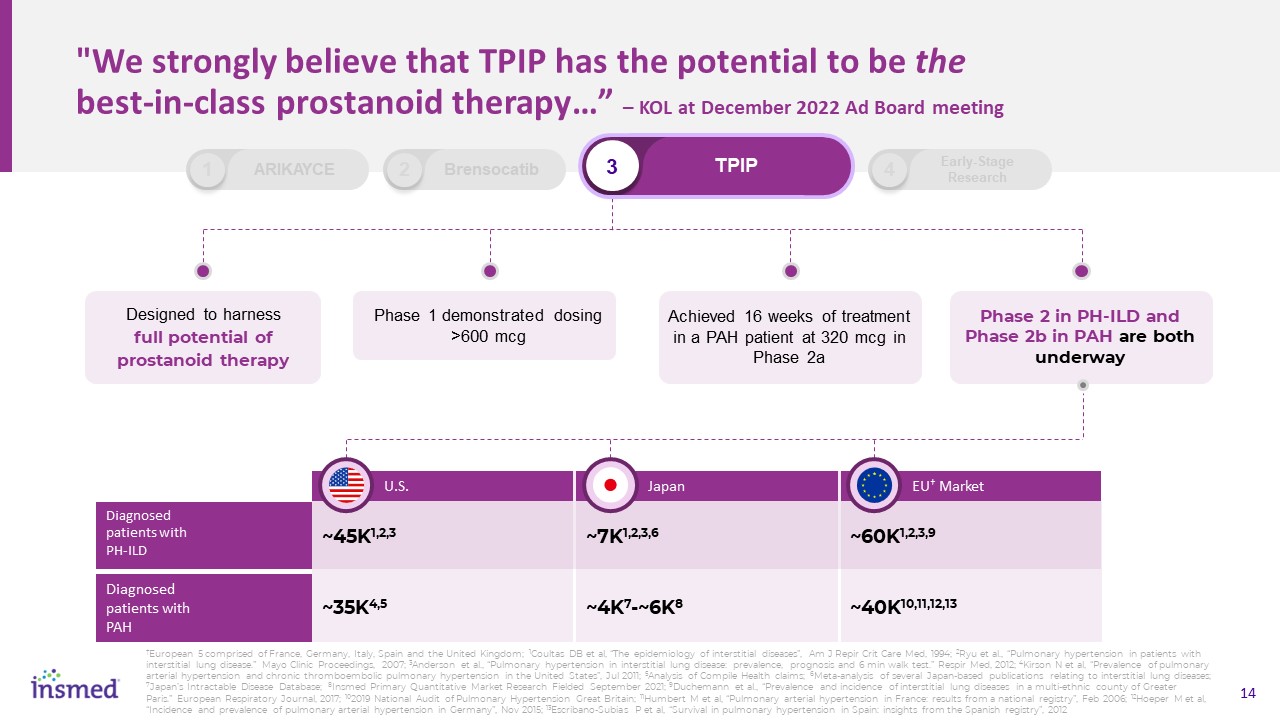
“我们坚信,TIP有可能成为同类最佳的前列腺素治疗…。”-KOL在2022年12月的广告委员会会议上充分利用前列腺素治疗的全部潜力第一阶段展示了剂量>600微克在一名PAH患者中实现了16周的治疗,剂量为320微克,在PH-ILD的2a阶段和PAH的2b阶段都在进行中。美国诊断的PH-ILD患者患有PAH~7K1,2,3,6~4K7-~6K8日本~45K1,2,3,9~40K10,11,12,13个欧盟†
市场2个Brensocatib 3个TPIP 1个Arikayce 4个早期研究†欧洲5个国家包括法国、德国、意大利、西班牙和英国;1 Coultas DB等人,“间质性疾病的流行病学”,Am J Repir Crit Care Med,
1994;2Ryu等人,“间质性肺病患者的肺动脉高压”。梅奥临床论文集,2007;3Anderson等人,“间质性肺疾病中的肺动脉高压:患病率、预后和6分钟步行试验
。Respir Med,2012;4 Kirson N等人,“美国的肺动脉高压和慢性血栓栓塞性肺动脉高压的流行率”,2011年7月;5对汇编的健康声明的分析;6关于间质性肺病的几种日本出版物的荟萃分析;7日本的顽固性疾病数据库;8引入的初级定量市场研究,2021年9月;9 Duchemann等人,“大巴黎一个多民族县间质性肺疾病的患病率和发病率”。《欧洲呼吸杂志》,2017年;《102019英国国家肺动脉高压审计》;11 Humbert M等人,《法国的肺动脉高压:来自国家登记的结果》, 2006年2月;12Hoeper M等人,“德国的肺动脉高压的发生率和流行率”,2015年11月;13Escribano-Subias P等人,“在西班牙的肺动脉高压中的生存:来自西班牙注册机构的见解”,2012年

我们设计了TPIP,以化学方式实现前列腺素的连续给药,并证明了其益处…雾化给药比静脉给药有更大的血管扩张作用。在最高剂量下,雾化吸入药物使肺血管阻力和肺动脉压恢复到基线水平…。正在进行的第二阶段试验旨在验证这一潜在益处15吸入前列腺素比全身给药更有效绵羊持续急性肺性高血压模型
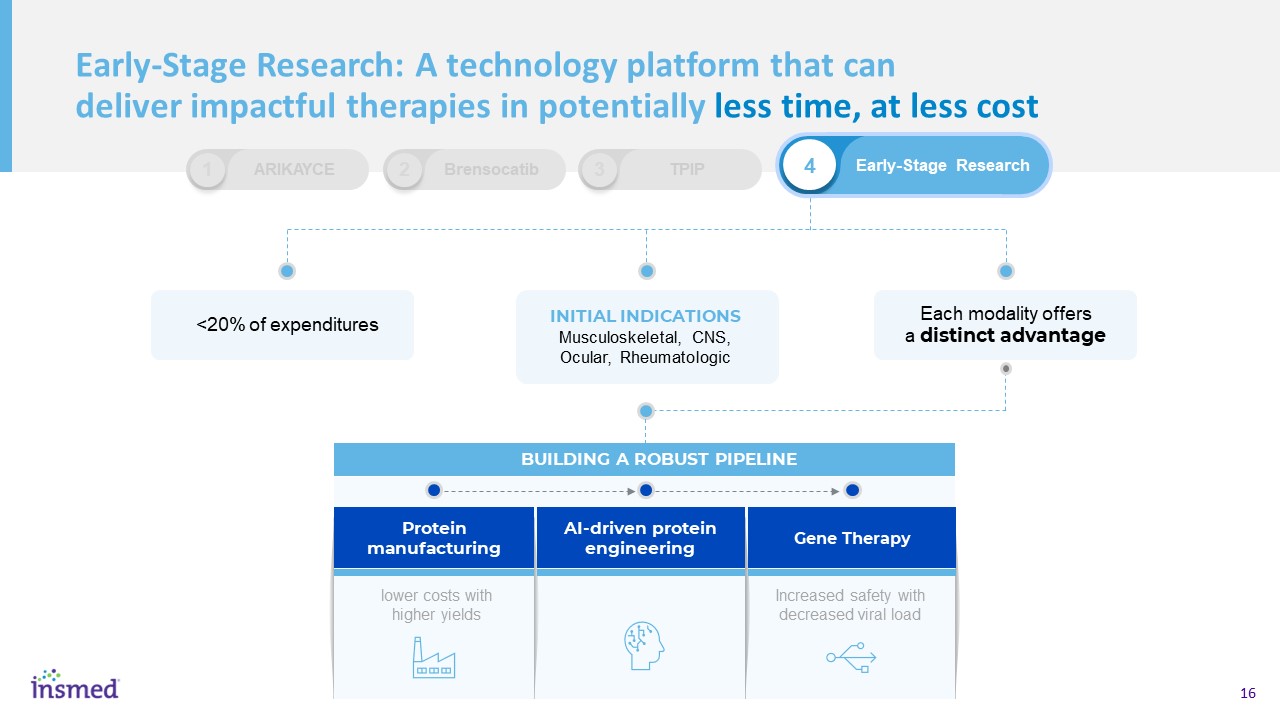

我们的三个不同的研究引擎预计将在2025年年底之前产生≥6 IND/第一阶段研究化学、配方和交付基因治疗,新型蛋白质制造人工智能驱动的蛋白质工程治疗靶点定位团队规模领导风湿学免疫学改进的病毒衣壳下一代DPP1抑制剂肌肉骨骼-1H23(IND)CNS-晚期‘23/早期’24(IND)新泽西州新泽西州加利福尼亚州N~40 N~15 N~35卡尔·格里斯沃尔德生物制品和NH站点负责人克里斯·贝利-凯洛格计算生物学Walter·珀金斯首席科学官布莱恩·卡斯帕

未来18个月的重要数据读数1H
2023 1 2 3 Arikayce Brensocatib TPIP 2H 2023 1H 2024肌肉骨骼临床前数据(2Q)CNS临床前数据(2Q)囊性纤维化PK/PD数据(1Q)TOPLINE结果(3Q)中期剂量滴定安全性和耐受性水平PH-ILD TOPLINE结果肌肉骨骼临床数据Aspen TOPLINE结果(2Q)4早期研究

我们的战略体现了我们对患者的承诺--提供改变生活的疗法,并迅速、创造性地工作,提供有意义的结果--改变生活的创新发生在突破性科学和协作文化的交汇处,在科学2022年生物医学雇主排行榜上排名第一(连续两年
)全球700多名员工19
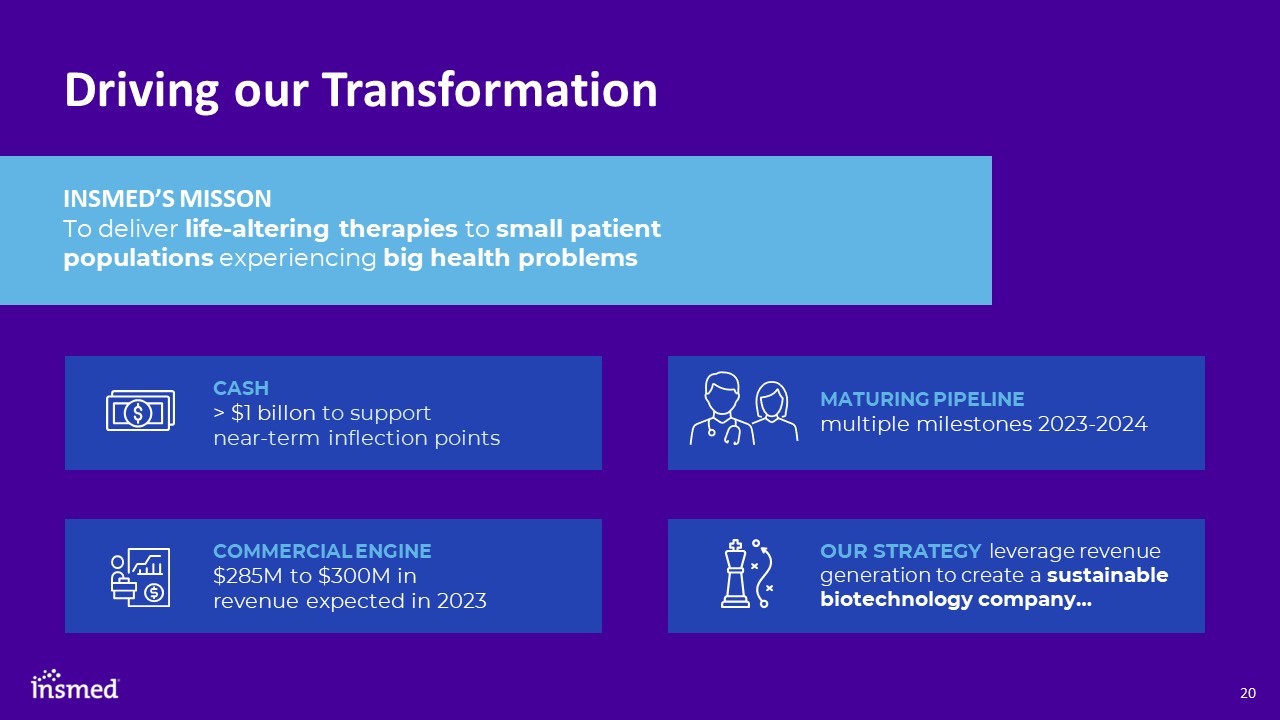
推动我们的转型Insmed的失败为经历重大健康问题的小患者群体提供改变生活的疗法
正在酝酿中的多个里程碑2023-2024我们的战略利用创收来创建可持续的生物技术公司…现金>10亿美元,用于支持近期拐点商业引擎,预计2023年收入将达到2.85亿至3亿美元