
ARV-471:2期VERITAC试验结果圣安东尼奥乳腺癌研讨会,2022年12月8日

安全港和前瞻性陈述2本陈述包含符合1995年“私人证券诉讼改革法”定义的前瞻性陈述,涉及重大风险和不确定性,包括有关ARV-471成为一种同类最佳雌激素受体靶向疗法的可能性的陈述,以及我们的ARV-471预期未来试验的时间,包括任何组合研究。“预期”、“相信”、“估计”、“预期”、“打算”、“可能”、“可能”、“计划”、“预测”、“项目”、“目标”、“潜在”、“将”、“可能”、“可能”、“应该”、“继续”以及类似的表述旨在识别前瞻性表述,尽管并不是所有前瞻性表述都包含这些识别词语。我们可能无法实际实现我们的前瞻性声明中披露的计划、意图或预期,您不应过度依赖我们的前瞻性声明。由于各种风险和不确定性因素,实际结果或事件可能与我们在前瞻性声明中披露的计划、意图和预期存在实质性差异,这些风险和不确定性包括但不限于:我们和辉瑞能否在预期的时间表内成功进行ARV-471临床开发并获得临床试验结果,或者根本不能;以及其他重要因素,这些因素可能会导致我们的实际结果与前瞻性声明中所述的结果大不相同,这些内容在提交给美国证券交易委员会的季度和年度报告中的“风险因素”部分进行了讨论。本演示文稿中包含的前瞻性陈述反映了截至本演示文稿发表之日我们对未来事件的当前看法, 除适用法律要求外,我们不承担更新任何前瞻性陈述的义务。这些前瞻性陈述不应被视为代表我们在本陈述之日之后的任何日期的观点。Arvinas的名称和标志是我们的商标。我们还拥有PROTAC®的服务商标和注册美国商标。本演示文稿中出现的商标、商号和服务标志均为其各自所有者的财产。我们省略了适用于本演示文稿中命名的商标的®和™名称。本演示文稿还包含独立各方和我们关于市场规模的估计和其他统计数据,以及关于我们行业的其他数据。这些数据涉及许多假设和限制,提醒您不要过度重视这些数据和估计。此外,对我们未来表现的预测、假设和估计,以及我们经营的市场的未来表现,必然受到高度不确定性和风险的影响。本演示文稿仅面向投资者群体。这并不是为了推广本文提到的产品或以其他方式影响医疗保健处方决策。交叉试验比较不是基于面对面的研究,也不能进行直接比较。

3简介
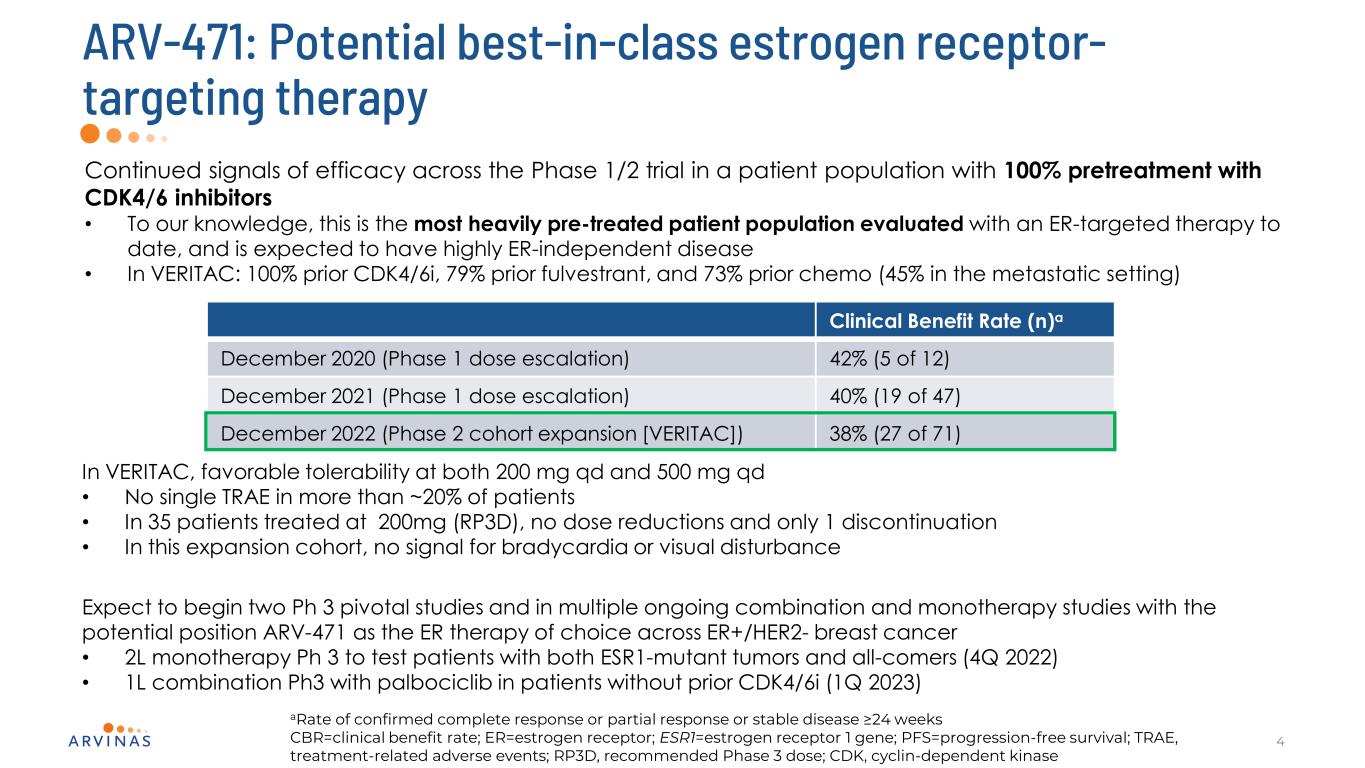
ARV-471:潜在的同类最佳雌激素受体靶向治疗4在1/2期试验中持续有效的信号,在使用CDK4/6抑制剂100%预治疗的患者群体中·据我们所知,这是迄今为止接受ER靶向治疗评估的最严重的预治疗患者群体,预计将有高度ER非依赖性疾病·在VERITAC:100%之前的CDK4/6i,79%的之前的fulvestrant,临床受益率(N)2020年12月(第一阶段剂量增加)42%(5/12)2021年12月(第一阶段剂量增加)40%(47/19)2022年12月(第二阶段队列扩大)[VERITAC])VERITAC中38%(27/71),对200 mg/d和500 mg/d都有良好的耐受性·在超过20%的患者中没有单一TRAE·在这个扩大队列中,在200 mg(RP3D)治疗的35例患者中,没有剂量减少和仅1例停药,没有心动过缓或视觉障碍的信号预计将开始两项Ph3关键研究和多项正在进行的联合和单一治疗研究,潜在的位置是ARV471作为ER+/HER2-乳腺癌的ER治疗的选择·2L单一治疗Ph3用于测试同时患有ESR1突变肿瘤和所有患者的患者(2022年4月)·1L与Palbociclib的联合Ph3在没有CDK4/6i(2023年1月)的患者中确认完全应答或部分应答或稳定疾病的比率≥24周CBR=临床受益率;ER=雌激素受体;ESR1=雌激素受体1基因;PFS=无进展生存期;TRAE,与治疗相关的不良事件;RP3D,推荐的3期剂量;CDK,细胞周期蛋白依赖性激酶

ARV-471:有可能成为ER+/HER2-乳腺癌治疗的内分泌骨干选择5潜在的未来美国ER+/HER2-乳腺癌治疗范例与ARV-471佐剂(手术后)乳腺癌(~160K)*转移性乳腺癌(~50K*)第二/第三线内分泌主干芳香酶抑制物(AI)Fulvestrant或伊西美坦附加疗法CDK4/6和其他靶向抑制剂mTOR抑制剂或PIK3抑制剂Fulvestrant*来自SEER数据库的美国人口每年事件CDK:细胞周期蛋白依赖性激酶,PI3K:磷酸肌醇3-激酶;MTOR:雷帕霉素的哺乳动物靶点ARV-471扩展潜力未来状态:ARV-471被设计为一种口服、高效的ER降解剂,近期具有良好的安全性

有SERDS或ARV471的研究包括一系列先前的治疗方法在关键研究中,VERITAC拥有大多数先前的治疗方法Paloma-31期3研究Palbociclib+fulvestrant与安慰剂+fulvestrant(N=521)0 0 34%‡acelERA2阶段2研究巨型消毒剂与SOC†(N=303)42%*19%*32%SERENA-23双亲诱导剂与Fulvestrant(N=2 4 0)50%0 19%Ameera-32期†(N=2 90)79*,‡10%*,‡11%VERONICA4联合富维斯特与富维斯特的‡11%‡VERONICA4期研究(N=103)100%0 EMERALD5 ELEACESTANT VS SOC†(N=477)100%30%22%VERITAC2期扩展队列的抗逆转录病毒-471(N=71)100%79%45%1Lancet Onol 2016。2022年ESMO。3 2022年圣安东尼奥乳腺癌研讨会。4临床癌症研究2022年.5J临床癌症2022年。*高级/转移设置。†医生对氟维斯特或芳香酶抑制剂的选择;他莫昔芬在AMEERA-3中也是允许的。SOC=标准护理‡公布的数据,手动计算总人口6预期耐药性预期疗效

7 ARV-471:VERITAC第二阶段详细结果
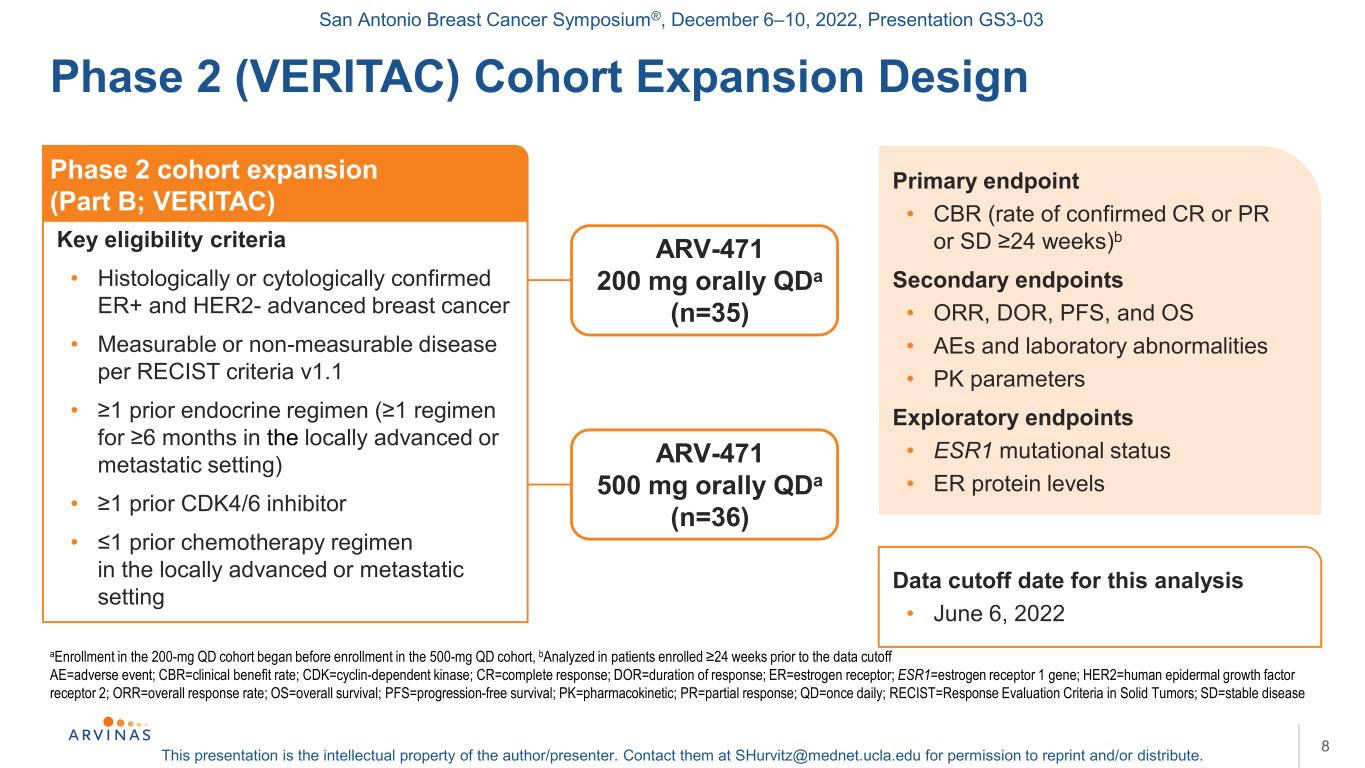
圣安东尼奥乳腺癌研讨会®,2022年12月6-10日,演示文稿GS3-03本演示文稿是作者/演讲者的知识产权。联系他们:shurvitz@mednet.ucla.edu,以获得转载和/或分发的许可。8a200mgQD队列中的登记在纳入500mgQD队列之前开始,b在数据截止前24周入选≥的患者中进行分析:AE=不良事件;CBR=临床受益率;CDK=细胞周期依赖性激酶;CR=完全应答;DOR=应答持续时间;ER=雌激素受体;ESR1=雌激素受体1基因;HER2=人类表皮生长因子受体2;ORR=总应答率;OS=总存活率;PFS=无进展存活率;PK=药代动力学;PR=部分应答;QD=每日一次;RECIST=实体肿瘤的疗效评价标准;SD=稳定期疾病2期(VERAC)队列扩大设计2期队列扩大(B部分;VERITAC)关键资格标准·组织学或细胞学证实的ER+和HER2-晚期乳腺癌·根据RECIST标准可测量或不可测量的疾病v1.1·≥1之前的内分泌方案(在局部晚期或转移的情况下,≥1方案为期6个月)·≥1之前的CDK4/6抑制剂·≥1之前的化疗方案在局部晚期或转移的情况下的主要终点·CBR(确诊CR或PR或SD≥24周的比率)b次要终点·ORR、DOR、PFS、和OS·AEs和实验室异常·PK参数探索终点·ESR1突变状态·ER蛋白水平ARV-471 200 mg口服QDA(n=35)ARV-471 500 mg口服QDA(n=36)本次分析的数据截止日期·2022年6月6日
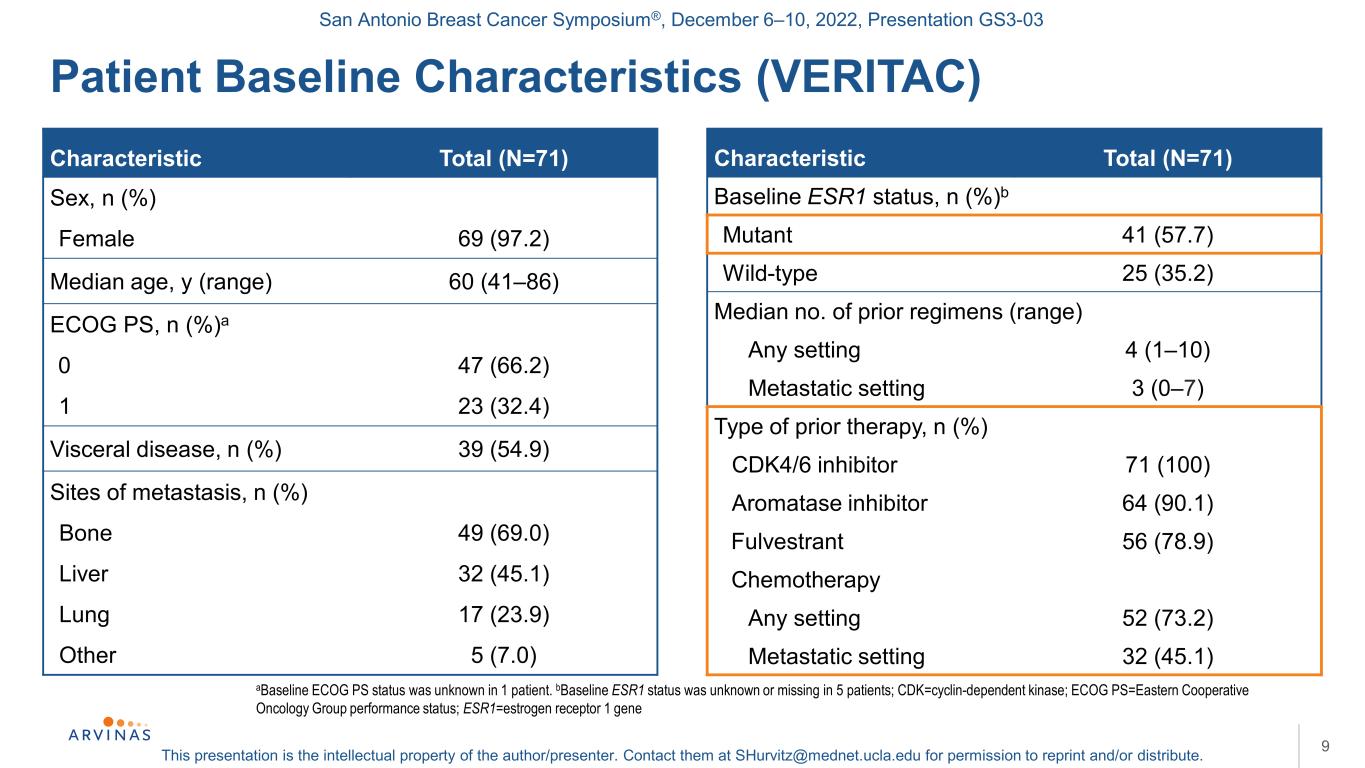
圣安东尼奥乳腺癌研讨会®,2022年12月6-10日,演示文稿GS3-03本演示文稿是作者/演讲者的知识产权。联系他们:shurvitz@mednet.ucla.edu,以获得转载和/或分发的许可。患者基线特征(VERITAC)9a基线ECOG PS状态未知1例.B基线ESR1状态未知或缺失5例;CDK=细胞周期蛋白依赖激酶;ECOG PS=东部合作肿瘤组表现状态;ESR1=雌激素受体1基因特征总数(N=71)性别,n(%)女性69(97.2)中位年龄,y(范围)60(41-86)ECOG PS,n(%)a 0 47(66.2)1 23(32.4)内脏疾病,n(%)39(54.9)转移部位,n(%)骨49(69.0)肝32(45.1)肺17(23.9)其他5(7.0)特征总(N=71)基线ESR1状态,N(%)b突变体41(57.7)野生型25(35.2)中位数之前的方案(范围)任何情况4(1-10)转移情况3(0-7)既往治疗类型n(%)CDK4/6抑制物71(100)芳香化酶抑制物64(90.1)Fulvestrant 56(78.9)化疗任何情况52(73.2)转移情况32(45.1)
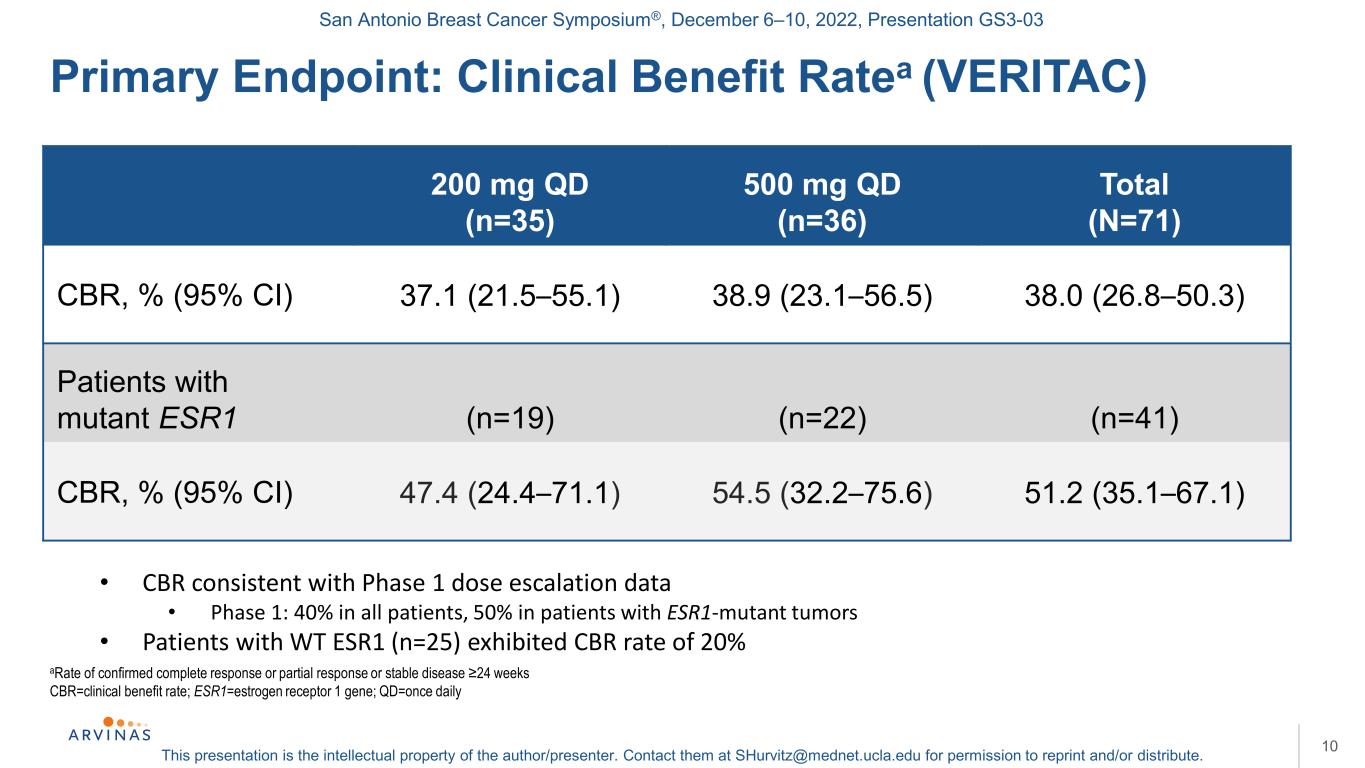
圣安东尼奥乳腺癌研讨会®,2022年12月6-10日,演示文稿GS3-03本演示文稿是作者/演讲者的知识产权。联系他们:shurvitz@mednet.ucla.edu,以获得转载和/或分发的许可。10确诊完全缓解或部分缓解或病情稳定的比率≥24周CBR=临床受益率;Qd=每日一次:临床受益率(VERITAC)200 mg qd(n=35)500 mg qd(n=36)总CBR(N=71)CBR,%(95%CI)37.1(21.5-55.1)38.9(23.1-56.5)38.0(26.8-50.3)突变ESR1患者(n=19)(n=22)(n=41)CBR,%(95%CI)47.4(24.4-71.1)54.5(32.2-75.6)51.2(35.1-67.1)·CBR与第一阶段剂量递增数据一致·第一阶段:所有患者40%,ESR1突变肿瘤患者50%·WT ESR1患者(n=25)CBR率为20%
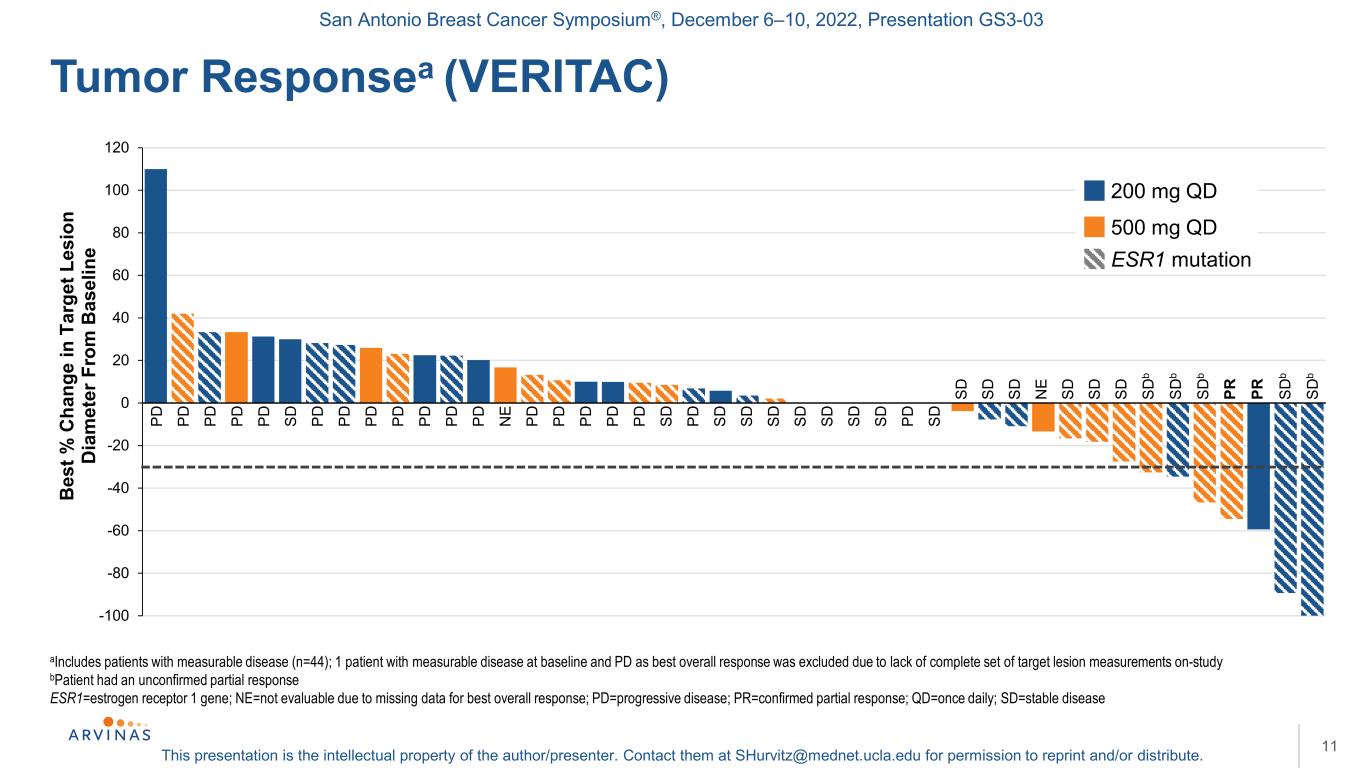
圣安东尼奥乳腺癌研讨会®,2022年12月6-10日,演示文稿GS3-03本演示文稿是作者/演讲者的知识产权。联系他们:shurvitz@mednet.ucla.edu,以获得转载和/或分发的许可。11a包括可测量疾病的患者(n=44);1名在基线可测量疾病和PD为最佳总体反应的患者因缺乏一套完整的靶点病变测量而被排除在研究中-研究b患者有未确认的部分反应ESR1=雌激素受体1基因;NE=由于缺少最佳总体反应的数据而不可评估;PD=进展性疾病;PR=确认的部分反应;QD=每天一次;SD=稳定型疾病肿瘤反应(VERITAC)-100-80-60-40-20 20 40 60 80 100 120 BES%C HANGE在E 200 mg QD 500 mg QD PD PD PDPD PDSD SDPD SD SDPD SD PD SD PD SD N E SD PR SD PR SD N E SD PR SD B PD SD b SD b SD b SD b ESR1突变
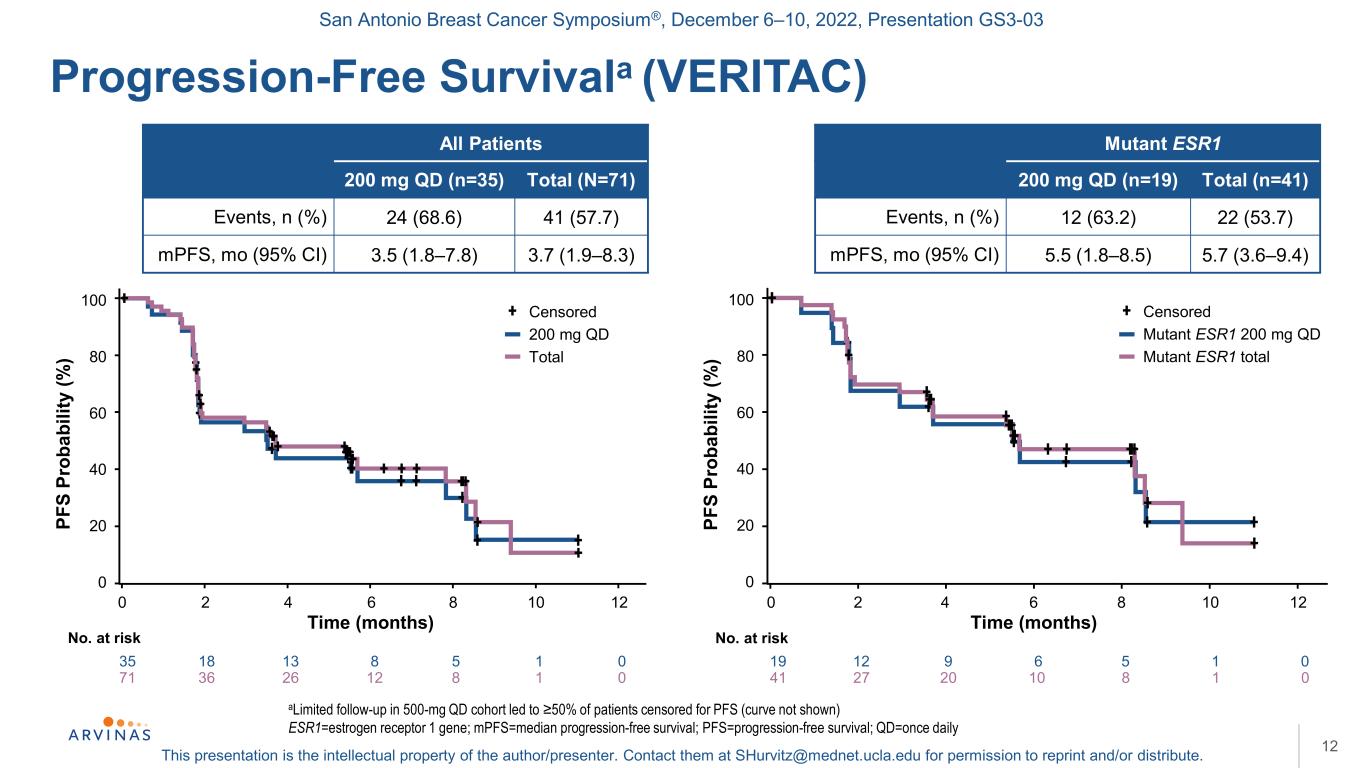
圣安东尼奥乳腺癌研讨会®,2022年12月6-10日,演示文稿GS3-03本演示文稿是作者/演讲者的知识产权。联系他们:shurvitz@mednet.ucla.edu,以获得转载和/或分发的许可。100 80 60 40 20 0无进展生存期(VERITAC)12在500mgQd队列中限定的随访导致≥50%的患者被审查PFS(曲线未显示)ESR1=雌激素受体1基因;MPFS=中位无进展生存期;PFS=无进展生存期;Qd=每天一次所有患者200 mg qd(n=35)总计(N=71)事件,n(%)24(68.6)41(57.7)mpFS,mo(95%CI)3.5(1.8-7.8)3.7(1.9-8.3)突变型ESR1 200 mg qd(n=19)总计(n=41)事件,n(%)12(63.2)22(53.7)mpFS,钼(95%CI)5.5(1.8-8.5)5.7(3.6-9.4)71 36 26 12 8 1 0 100 80 60 40 0 PF S PROAB(%)0 2 4 6 8 8 10 12次(月)否风险35 18 13 8 5 10共审查200 mg qd突变体ESR1 200 mg qd突变体ESR1总Pf S pr abilty(%)0 2 4 6 8 10 12时间(月)No.面临风险41 27 20 10 8 1 0 19 12 9 6 5 1 0
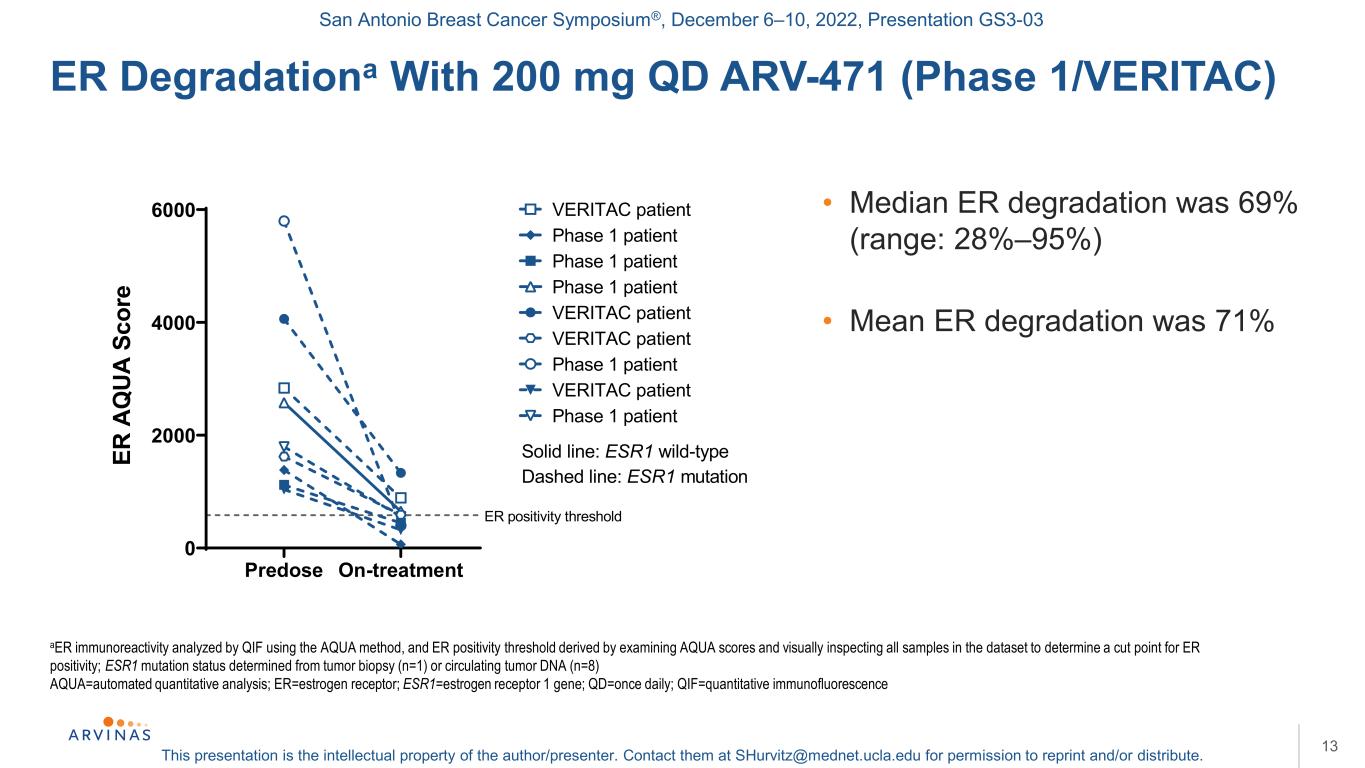
圣安东尼奥乳腺癌研讨会®,2022年12月6-10日,演示文稿GS3-03本演示文稿是作者/演讲者的知识产权。联系他们:shurvitz@mednet.ucla.edu,以获得转载和/或分发的许可。ER Degradationa含200 mg QD ARV-471(1期/VERITAC)13Aer免疫反应性由QIF使用Aqua方法分析,ER阳性阈值通过检查Aqua评分和肉眼检查数据集中的所有样本以确定ER阳性的临界点而得出;ESR1突变状态通过肿瘤活检(n=1)或循环肿瘤DNA(n=8)Aqua=自动定量分析;ER=雌激素受体;ESR1=雌激素受体1基因;QD=每天一次;QIF=定量免疫荧光·ER降解率中位数为69%(范围:28%-95%)·治疗前平均ER降解率为71%0 2000 4000 6000 ER A Q UA S COR阳性阈值VERITAC患者1期患者VERITAC患者1期VERITAC患者1期患者实线:ESR1野生型虚线:ESR1突变
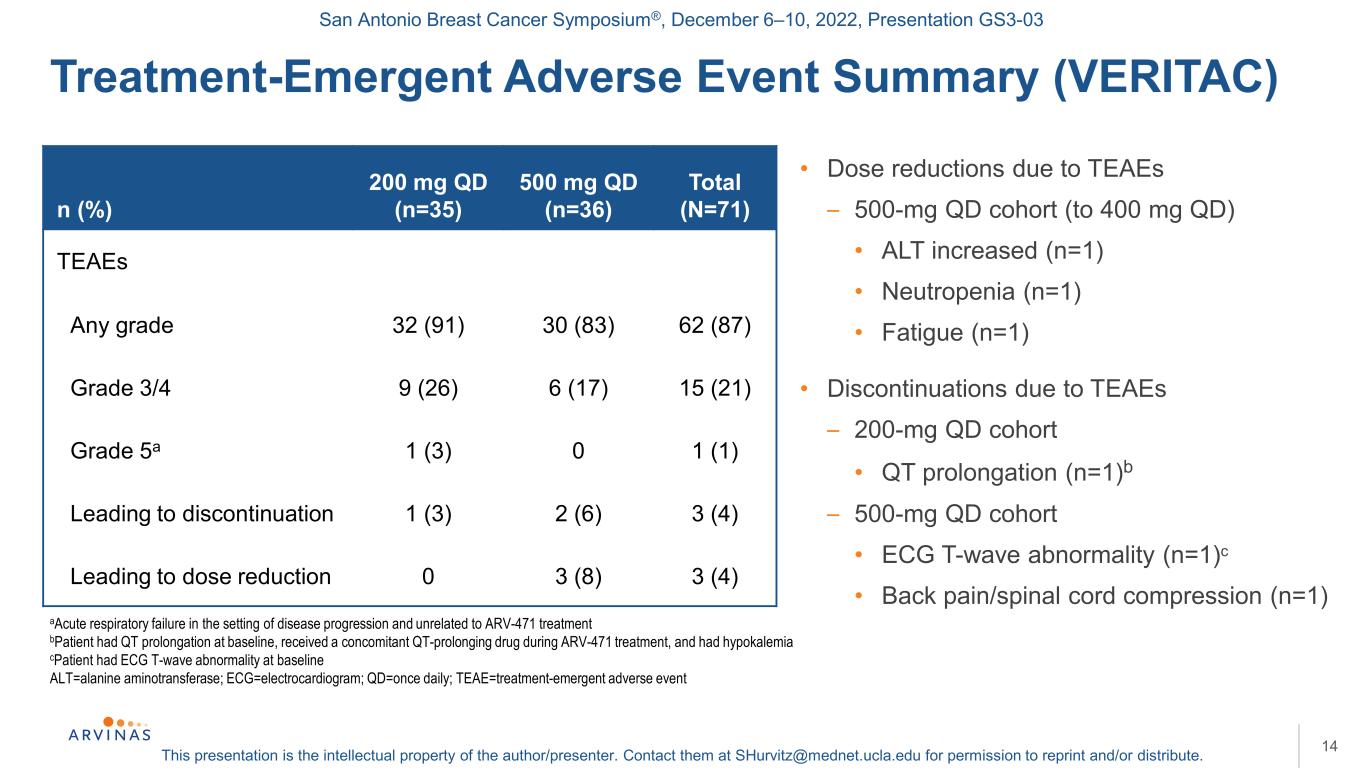
圣安东尼奥乳腺癌研讨会®,2022年12月6-10日,演示文稿GS3-03本演示文稿是作者/演讲者的知识产权。联系他们:shurvitz@mednet.ucla.edu,以获得转载和/或分发的许可。治疗-紧急不良事件总结(VERITAC)14与ARV-471治疗无关的疾病进展背景下的急性呼吸衰竭患者在基线时QT延长,在ARV-471治疗期间接受伴随的QT延长药物,并有低钾血症患者在基线时有心电图T波异常,ALT=丙氨酸氨基转移酶;ECG=心电图;QD=每日一次;TEAE=治疗-紧急不良事件·TEAE导致的剂量减少-500 mg qd队列(至400 mg qd)·ALT升高(n=1)·中性粒细胞减少(n=1)·疲劳(n=1)·因TEAEs中断-200 mg qd队列·QT延长(n=1)b-500 mg qd队列·心电图T波异常(n=1)c·背痛/脊髓压迫(n=1)n(%)200 mg qd(n=35)总计500 mg qd(n=71)TEEs Any分级32(91)30(83)(87)3/4级9(26)6(17)15(21)5a级1(3)0 1(1)导致停止1(3)2(6)3(4)导致剂量减少0 3(8)3(4)
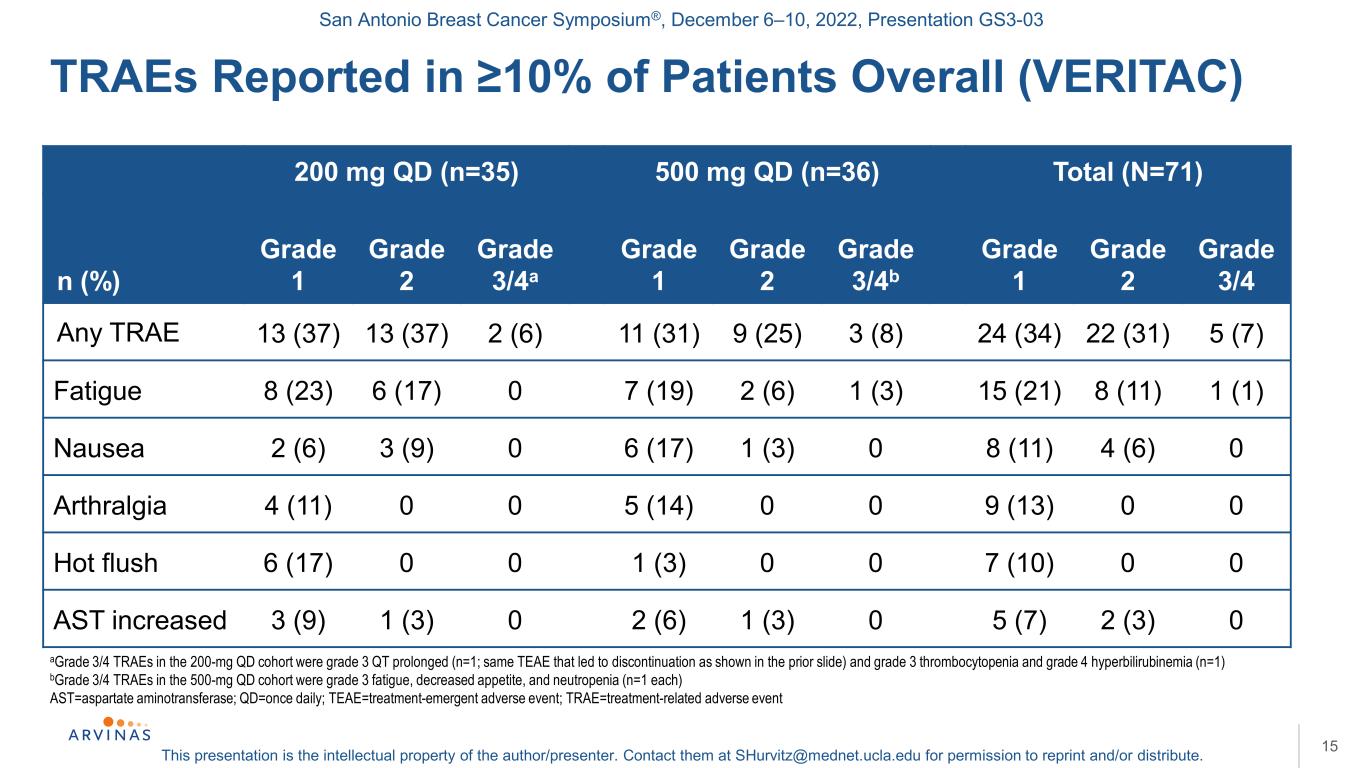
圣安东尼奥乳腺癌研讨会®,2022年12月6-10日,演示文稿GS3-03本演示文稿是作者/演讲者的知识产权。联系他们:shurvitz@mednet.ucla.edu,以获得转载和/或分发的许可。200 mg qd(n=35)500 mg qd(n=36)总计(N=71)n(%)1级2级3/4a级1级2级3/4b级1级3/4任何曲目13(37)13(37)2(6)11(31)9(25)3(8)24(34)22(31)5(7)疲劳8(23)6(17)07(19)2(6)1(3)15(21)8(11)1(1)恶心2(6)3(9)0 6(17)1(3)0 8(11)4(6)0关节痛4(11)0 0 5(14)0 0 9(13)0 0潮热6(17)0 0 1(3)0 0 7(10)0 0 AST增加3(9)1(3)0 2(6)1(3)0 5(7)2(3)0 15 A级3/4 TRAE延长(n=1);B500 mg qd队列中3/4级TRAE为3级疲乏、食欲下降和中性粒细胞减少(n=1),AST=天冬氨酸氨基转移酶;Qd=每天1次;TEAE=治疗-紧急不良事件;TRAE=治疗相关不良事件≥中报告的TRAE占患者总数的10%(VERITAC)
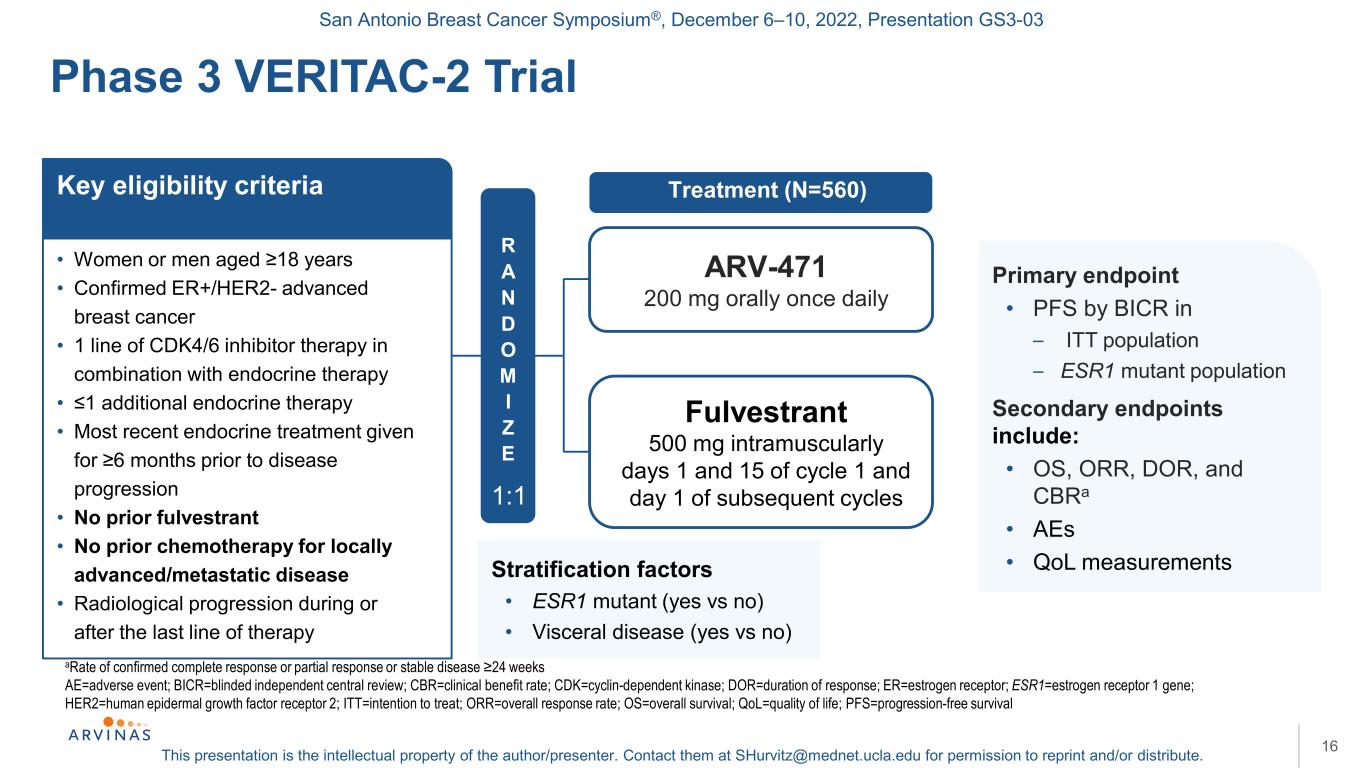
圣安东尼奥乳腺癌研讨会®,2022年12月6-10日,演示文稿GS3-03本演示文稿是作者/演讲者的知识产权。联系他们:shurvitz@mednet.ucla.edu,以获得转载和/或分发的许可。16确诊完全缓解或部分缓解或病情稳定的比率≥24周AE=不良事件;BICR=盲法独立中心综述;CBR=临床受益率;CDK=细胞周期蛋白依赖性激酶;DOR=反应持续时间;ER=雌激素受体;ESR1=雌激素受体1基因;HER2=人表皮生长因子受体2;ITT=治疗意向;ORR=总应答率;OS=总生存期;QOL=生活质量;PFS=无进展生存期3 VERITAC-2试验·年龄18岁的女性或男性·确诊的ER+/HER2-晚期乳腺癌·CDK4/6抑制剂联合内分泌治疗的1行·≤1附加内分泌治疗·在疾病进展前6个月接受最近的内分泌治疗·以前没有接受过福尔维斯特·没有接受过局部晚期/转移性疾病的化疗·最后一次治疗期间或之后的放射进展-4712万毫克,每天肌肉注射一次Fulvestrant,每天500 mg,在周期1和15天以及随后的关键资格标准主要终点的第1天和第15天,以及随后的关键资格标准主要终点的第1天和第15天·BICR In-ITT群体的PFS-ESR1突变群体次要终端包括:·OS、ORR、DOR和CBRa·AEs·QOL测量R A N D O M I Z E 1:1分层因素·ESR1突变(是与否)·内脏疾病(是与否)治疗(N=560)
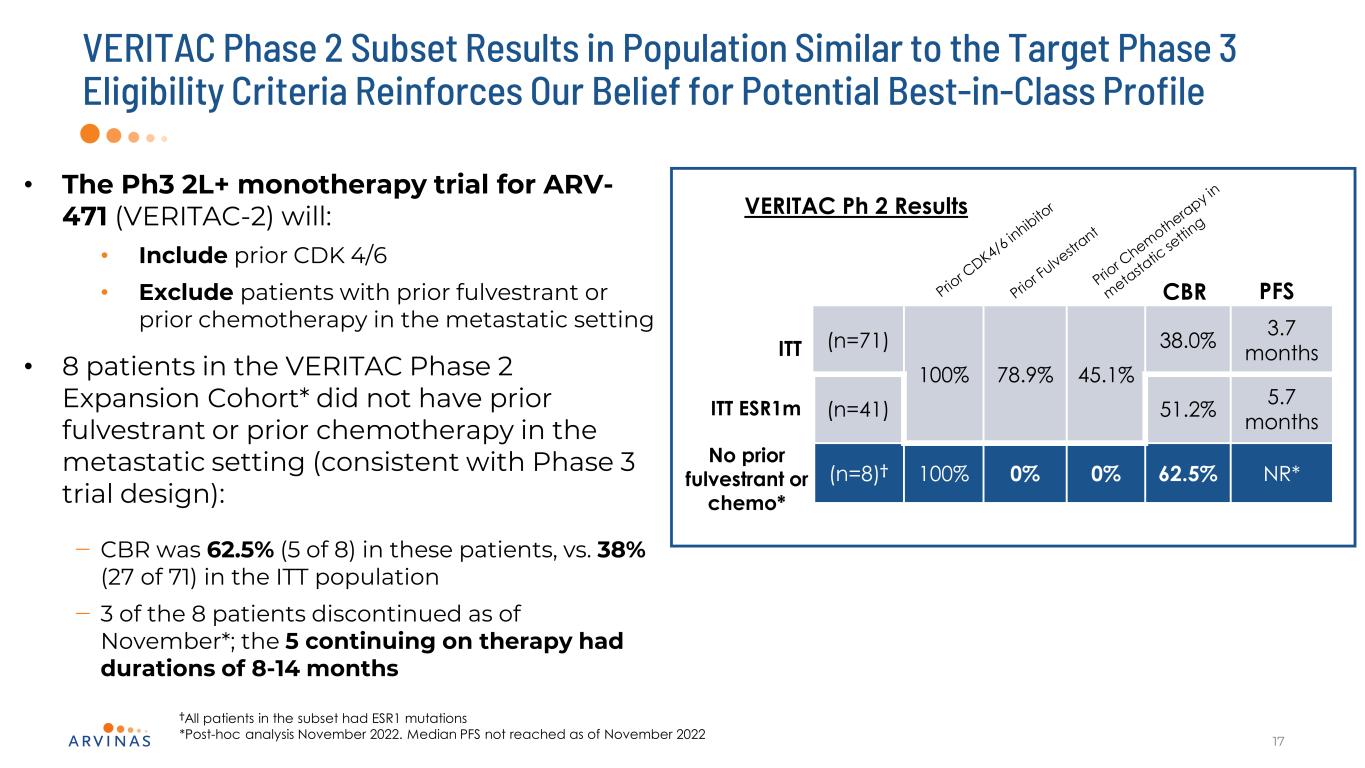
VERITAC 2期子集在人群中的结果与目标3期资格标准相似,这加强了我们对潜在的同类最佳配置文件的信念17·针对ARV-471的Ph3 2L+单一疗法试验(VERITAC-2)将:·包括先前的CDK 4/6·排除在转移环境中曾接受过全反式或先前化疗的患者·VERITAC第2期扩展队列中的8名患者*在转移环境中没有以前的全反式或先前的化疗(与第3期试验设计一致):-CBR在这些患者中为62.5%(5/8),ITT人群中38%(27/71)--截至11月,8名患者中有3名停止了治疗*;继续治疗的5名患者的持续时间为8-14个月,†亚组中的所有患者都有ESR1突变*2022年11月的事后分析。截至2022年11月未达到的中位数PFS ITT(n=71)100%78.9%45.1%38.0%3.7个月(n=41)51.2%5.7个月(n=8)†100%0%0%62.5%NR*VERITAC Ph2结果CBR PFS无之前的富尔维酮或化疗*ITT ESR1M

18个结论

持续的疗效和良好的耐受性使ARV-471走上了两项关键研究的道路,这两项研究很快将开始19·良好的耐受性,分别为200 mg qd和500 mg qd·200 mg第3阶段剂量,无剂量减少和一次停药·ARV-471的耐受性非常适合于在疾病连续过程中开发·启动Ph3试验·在治疗经验较少的患者中采用单一疗法2L Ph3(2022年第四季度)·旨在解决ESR1mut和All-comers中的作用的试验·Palbo联合1L Ph3在ER依赖肿瘤患者中的应用(2023年第一季度)·与其他联合疗法和早期乳腺癌一起启动的更广泛的开发·ARV-471在严重耐药患者中显示出强大的CBR和MPFS·在这一难以治疗的人群中的活性表明了PROTAC技术的耐受性的潜力。其安全性和有效性尚未确定:确诊完全缓解或部分缓解或病情稳定的比率≥24周CBR=临床受益率;ER=雌激素受体;ESR1=雌激素受体1基因;PFS=无进展生存期

VERITAC数据证实,ARV471有可能成为一种同类中最好的ER靶向疗法20cc 2020:阶段1 PoC 2021:阶段1读出2022:阶段2读出2022:计划启动TACTIVE-U,TACTIVE-E 2022:计划在日本患者中启动TACTIVE-N 2022:在日本患者中启动第一阶段验证的PROTAC蛋白质降解器持续疗效信号和良好的耐受性特征支持推进到日本的第三阶段注册研究第一阶段试验,以实现具有多靶向治疗的全球路径组合试验-按计划增加更多药物,以建立ARV-471作为骨干治疗的潜力,旨在评估早期乳腺癌的安全性和临床活性(例如,新佐剂)下一个里程碑:第3阶段注册研究(1L)证实了ARV-471作为转移性乳腺癌2022年潜在治疗方法的评估:VERITAC-2 Ph3试验(2L+单一疗法)第一个地点的剂量患者已经启动

谢谢你21岁