

展品99.1 3Q 2022|业务介绍神经退行性疾病和癌症的疾病修饰疗法的临床进展 Inhibikase.com:IKT

免责声明本演示文稿不应构成出售要约或征求购买任何证券的要约,也不得在任何州或司法管辖区出售此类证券,在这些州或司法管辖区,此类要约、招揽或出售在根据任何此类州或司法管辖区的证券法注册或资格之前是非法的 。本报告包含的信息可能构成证券法第27A节和修订后的1934年证券交易法第21E节所指的“前瞻性陈述”。Inhibikase Treateutics,Inc.(以下简称“公司”或“我们”)打算将前瞻性陈述纳入这些章节中前瞻性陈述的安全港条款。一般来说,我们通过使用“相信”、“预期”、“打算”、“估计”、“预期”、“项目”、“目标”、“预测”、“ ”、“目的”、“应该”、“将”、“可能”、“继续”以及类似的表述来识别此类前瞻性陈述。此类陈述受许多假设、风险和不确定因素的影响,这些假设、风险和不确定性可能会导致实际结果、业绩或成就与这些前瞻性陈述中预期的大不相同。您应该仔细阅读包含这些词语的声明,因为它们讨论了未来的预期和计划,其中包含对未来临床研究、监管批准、候选产品开发、运营结果或财务状况的预测,或陈述其他前瞻性信息。然而,没有这些词语或类似的表达并不意味着一项陈述不具有前瞻性。前瞻性陈述不是历史事实,而只是代表公司对未来事件的信念,其中许多事件的性质, 本质上是不确定的,不在公司的控制范围内。公司的实际结果和财务状况可能与这些前瞻性陈述中显示的预期结果和财务状况大不相同。管理层认为, 截至目前,这些前瞻性陈述是合理的。但是,应当注意的是,不要过度依赖任何此类前瞻性陈述,因为此类陈述只能说明发表之日的情况。除法律要求外,公司不承担公开更新或修改任何前瞻性陈述的义务,无论是由于新信息、未来事件还是其他原因。此外,前瞻性陈述会受到某些风险和不确定性的影响,这些风险和不确定性可能会导致实际结果与公司的历史经验以及我们目前的预期或预测大相径庭。可能导致实际结果与前瞻性陈述大不相同的重要因素在公司提交给美国证券交易委员会的文件中陈述,包括其10-K表格的年度报告和10-Q表格的季度报告,包括在“风险因素”标题下。我们 无意使用或展示其他实体的名称、商号、商标或服务标志,以暗示与任何其他实体之间的关系,或由任何其他实体背书或赞助我们。Inhibikase.com·:IKT 2

激酶抑制剂治疗的多治疗流水线开发治疗光谱的创新药物·专注于开发包括神经退行性变、肿瘤学和传染病在内的广泛治疗范围的新疗法。·目的通过使用该公司使用代谢保留(RAMP)药物化学平台的重新工程方法模拟人类疾病来发现新的治疗方法·IKT-148009:Lead Abelson Tyroine Kinase(c-Abl)抑制剂计划有可能成为 帕金森氏病(PD)和相关疾病的疾病修正治疗方法。2a期“201”课程开放招生。·IKT-001Pro:第一个肿瘤学产品是一种bcr-abl抑制剂,与治疗白血病和胃肠道癌症的标准甲磺酸伊马替尼相比,其安全性可能有所改善。提交慢性髓系白血病的IND申请。·强大的专利组合,保护到2033年(肿瘤学)和2036年(神经退行性变)。·来自美国国立卫生研究院、美国国防部、迈克尔·J·福克斯基金会和佐治亚州研究联盟的2080万美元赠款和合同,均经同行审查;2021年投资者资本毛收入6300万美元·经验丰富的管理团队、顾问、董事会和科学顾问委员会Inhibikase.com·:IKT 3
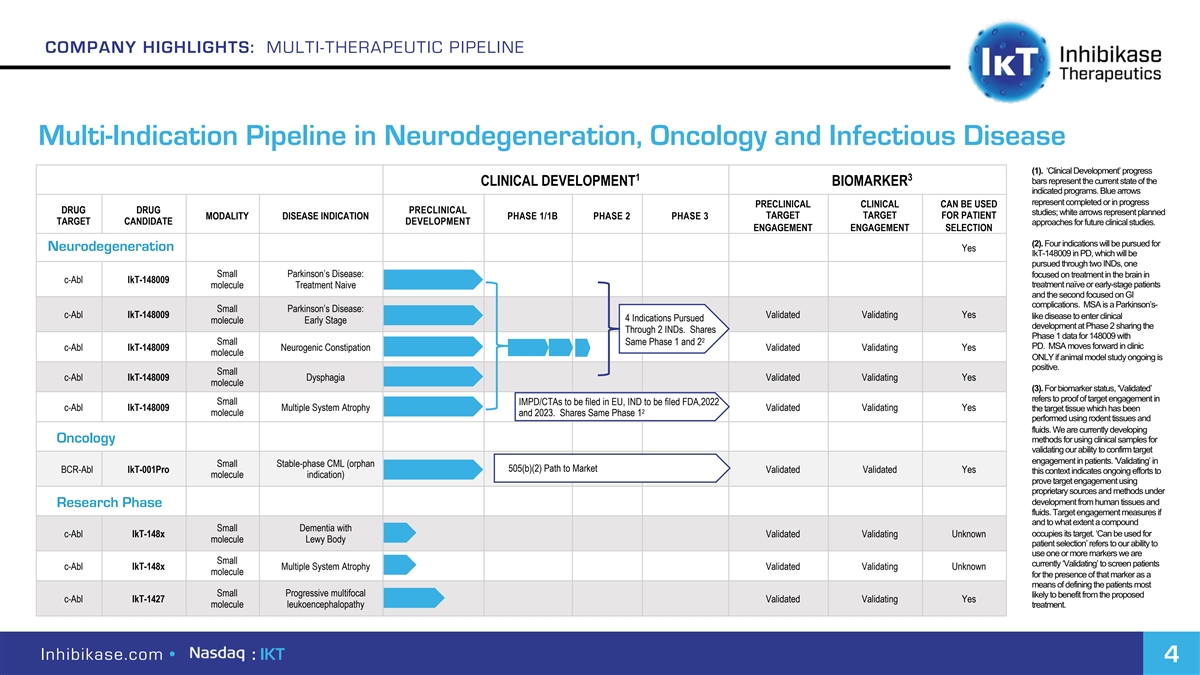
公司亮点:神经退行性疾病、肿瘤和传染病的多治疗流水线多适应症流水线(1)。‘临床开发’进展1-3条代表了临床开发生物标记物所指示的项目的当前状态。蓝色箭头表示已完成或正在进行的 临床前药物可用于药物临床前研究;白色箭头表示患者形态疾病适应症阶段1/1B阶段2阶段3目标候选开发方法的计划目标。 参与选择(2)。神经退行性变将寻求四种适应症是IKT-148009治疗帕金森氏症,将通过两种IND来进行,一种是小型帕金森氏症:专注于大脑中的治疗,c-Abl IKT-148009 治疗幼稚或早期患者的分子治疗朴素,第二种侧重于胃肠道并发症。MSA是一种帕金森氏症-小型帕金森氏症:C-Abl IKT-148009验证验证是样病进入临床4 共享通过2个IND的第二阶段分子早期开发。与2个相同的小1期和2个PD共享148009的1期数据。MSA在临床上取得了进展,c-Abl IKT-148009神经源性便秘验证验证 只有在正在进行的动物模型研究呈阳性的情况下才验证是分子。小c-Abl IKT-148009吞咽困难验证是分子(3)。对于生物标记物状态,“有效”是指目标参与小型IMPD/CTA的证明将提交给欧盟,IND提交给FDA, 2022年c-Abl IKT-148009多系统萎缩验证是的,验证的目标组织已经是2个分子和2023年。共享使用啮齿动物组织和液体执行的相同阶段1。我们目前正在开发肿瘤学 方法,使用临床样本来验证我们确认患者目标参与的能力。在小型稳定相CML(孤儿505(B)(2)上市之路BCR-ABL IKT-001Pro验证是此上下文 指示正在进行的分子适应症的努力)使用来自人体组织和研究相液的专有来源和方法证明靶向参与。目标参与度衡量复合小规模痴呆症是否以及在多大程度上占据目标。‘可用于c-Abl IKT-148x验证未知分子路易体患者选择’指的是我们使用一个或多个我们目前较小的标志物的能力,以筛查c-Abl IKT-148x多系统萎缩验证的患者c-Abl IKT-148x多系统萎缩验证未知分子的存在,以此作为定义最小进展性多焦点可能从拟议的c-Abl IKT-1427 验证白质脑病治疗中受益的患者的一种手段。Inhibikase.com·:IKT 4

帕金森病市场和帕金森病市场 &战略战略Inhibikase.com·:IKT 5
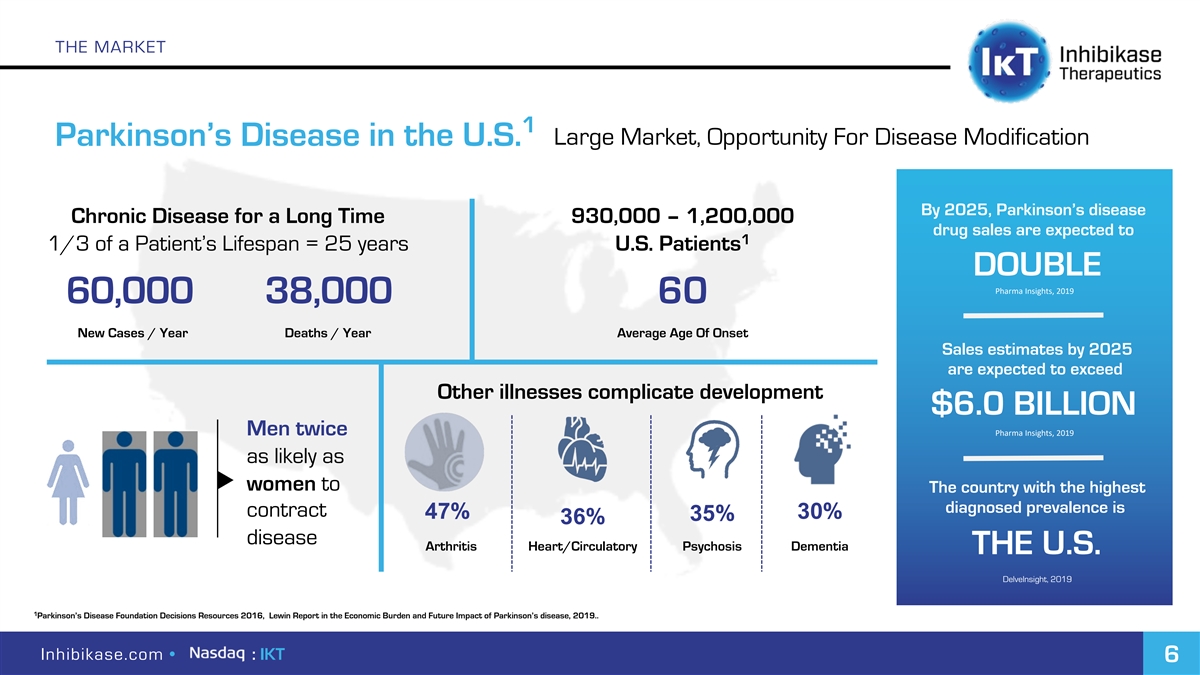
市场1大市场,疾病改良的机会 帕金森氏症在美国。到2025年,帕金森氏症慢性疾病长期存在93,000-1,200,000种药物的销售量预计将达到患者寿命的1/3=25年。美国患者加倍Pharma Insights,2019年 60,000 38,000新病例/年60例/年60例/年平均发病年龄销售估计到2025年将超过其他疾病复杂化发展60亿美元男性Pharma Insights,2019年与女性一样,确诊患病率最高的国家是合同47%30%35%36%疾病关节炎心脏/循环性精神病痴呆美国DelveInsight,2019年1帕金森氏病基金会决定资源2016,勒文在经济负担和 帕金森病的未来影响,2019年。Inhibikase.com·:IKT 6
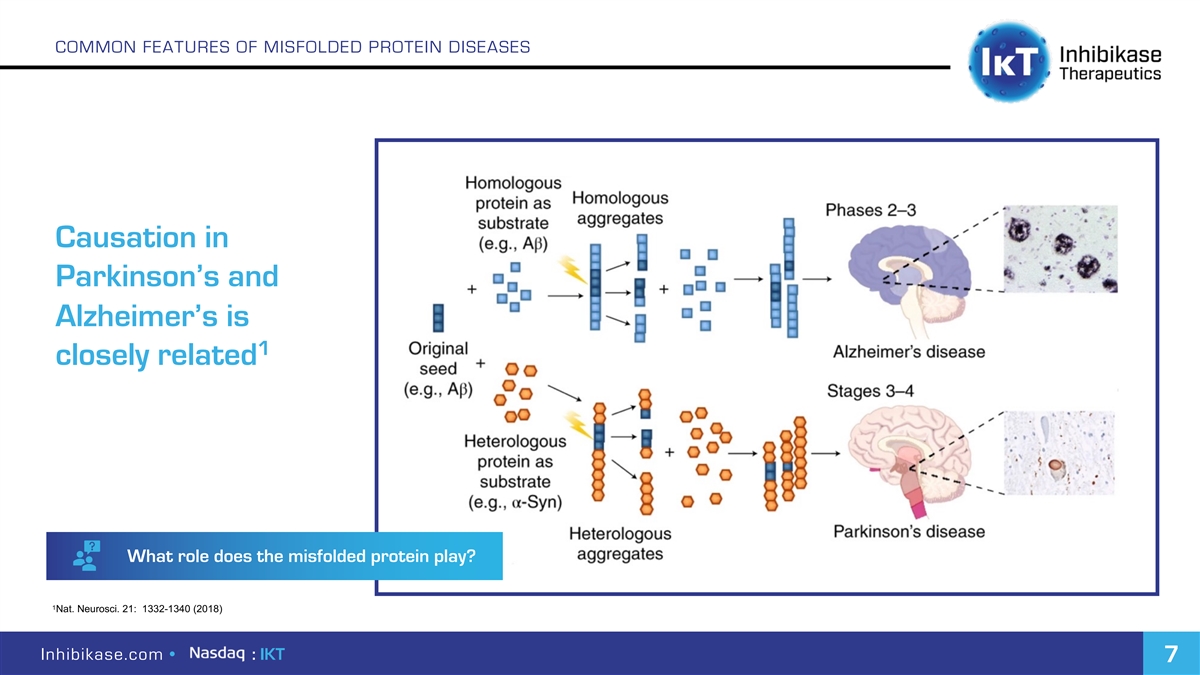
错误折叠的蛋白质疾病的共同特征在帕金森氏症和阿尔茨海默病的病因中密切相关,错误折叠的蛋白质扮演什么角色?神经科。21:1332-1340(2018)Inhibikase.com·:IKT 7
帕金森氏症c-Abl中错误折叠的‘种子’蛋白导致神经变性的原因评估视频>Inhibikase.com·:ikt 8
抑制酶将如何改变帕金森病:用IKT-148009抑制C-Abl激酶 :iKT 9
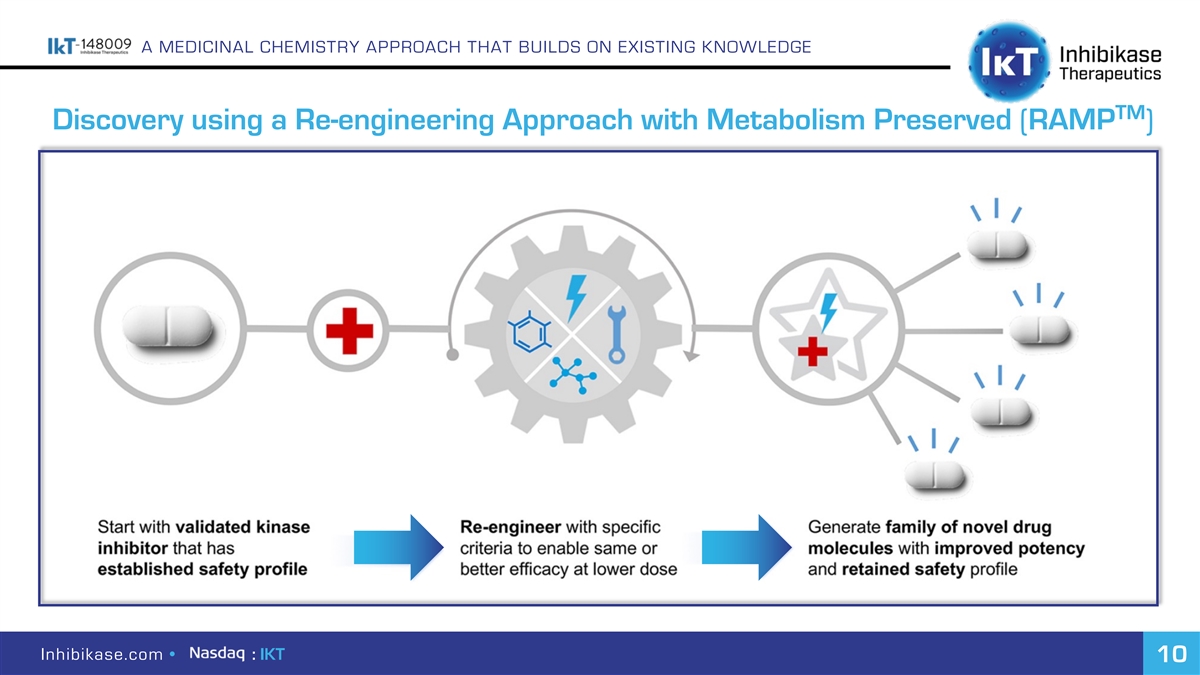
建立在现有知识基础上的药物化学方法TM 使用代谢保留(RAMP)Inhibikase.com·:IKT 10的重新工程方法发现

是一种小分子c-abl抑制剂IKT-148009,毒性低,选择性强,脑渗透剂1c-Abl抑制剂在临床开发中的毒理学人类等量剂量伊马替尼达沙替尼IKT-148009心血管无120肾无肝无100骨髓无· 选择性80胸骨抑制剂无c-abl和载脂蛋白2/Arg血液无60个PBMCs略有增加·设计抑制中性粒细胞对癌症的毒性40种正常限量药物对原代20或成熟细胞无细胞毒性在当前持续脑内低或无明显器官毒性>1微摩尔0知识水平c-ab1 c-abl/Arg c-Kit PDGFRb1第13周和第39周的毒理学数据显示,IKT-148009·高脑外显率 抑制这些酶导致的毒性随着剂量的延长具有更有利的毒性分布:IKT 11 IC(Nm)50 0.6 48 33 1 41 14 31 5 100 28 72 100 28 72 28 72
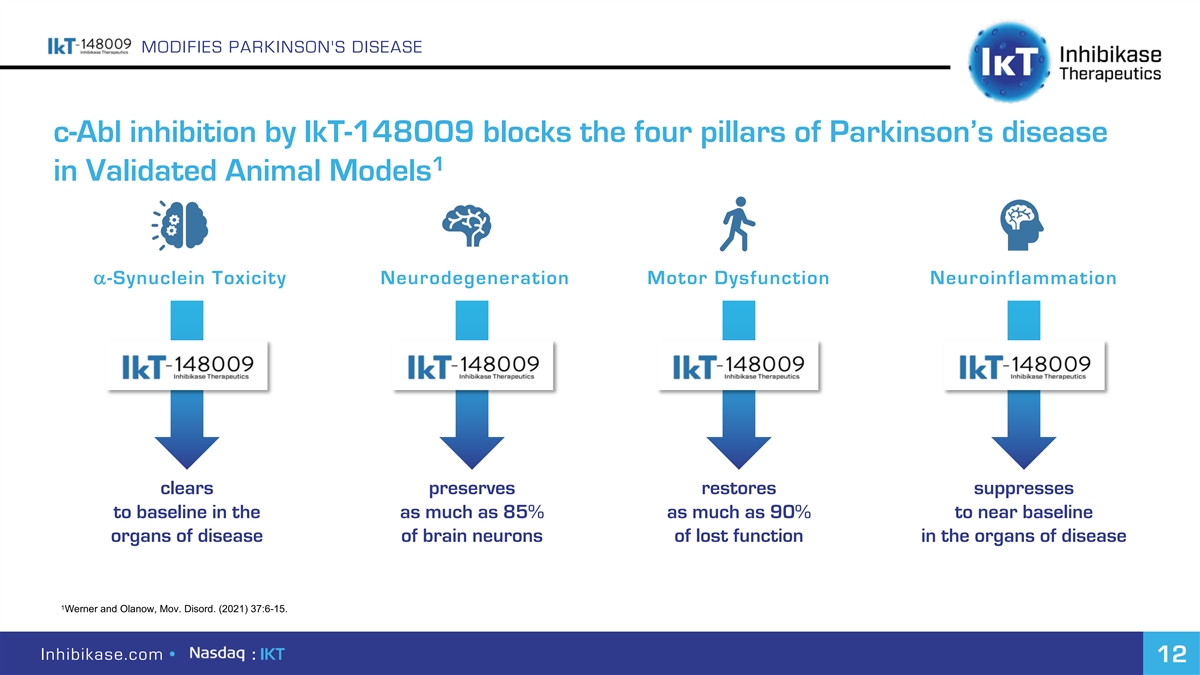
通过IKT-148009修饰帕金森病c-Abl抑制在经过验证的动物模型中阻断帕金森病1的四大支柱a-突触核蛋白毒性神经变性运动功能障碍神经炎症清除保留恢复抑制到基线高达85%到接近基线 疾病器官中丧失功能的脑神经元在沃纳和奥兰诺,Mov的器官中。迪诺德。(2021)37:6-15。Inhibikase.com·:IKT 12

IKT-148009 Inhibikase.com·:iKT的临床开发 13

安全和剂量1/1B阶段的第一阶段试验:剂量比例 临床药代动力学和无临床显著不良事件健康受试者评估帕金森患者价值类别人口学(占总数的百分比N=88)(占总数的百分比,N=13)性别女性34(38.6)6(42.8)男性54(61.4)7(57.2)平均年龄 (SD)57.9(5.72)62.5中位数58.0 62 IKT-148009不在45,69,57,70导致典型的c-Abl种族拉美裔或拉丁裔13(14.8)3(23.1)抑制剂不良事件:非西班牙裔或拉丁裔75(85.2)10(76.9)无GI种族黑人或非洲人 美国人54(61.4)2(15.4)无心血管白种33(37.5)11(84.6)无血液学其他1(1.1)0(0)不良反应7(7.9),所有临床意义不大5(38.5)Inhibikase.com

安全性和剂量方面的第一阶段试验第一阶段:剂量比例临床 药代动力学和没有临床显著不良事件IKT-148009-SAD Cmax AUC线性(Cmax)线性(Auc)200000 R²=0.9977 6000 180000 R²=0.9905 160000 5,000 140000临床4000药代动力学120000 100000 3000低剂量口服剂量120000 100000 3000高暴露剂量;线性剂量2000年比例高达175 mg。60000次暴露于75 mg IKT-40000 148009相当于1000 1 20000 500 mg伊马替尼治疗剂量范围1 00 FDA摘要 批准数据21-335 0 20 40 60 100 120 140 160 180口服剂量(Mg)Inhibikase.com·:IKT 15平均Cmax(Ng)平均AUC0-∞(ng-h/mL

评估帕金森氏症患者安全性的1B期试验:1B期:与具有相似T和1/2暴露(C和AUC)的老年健康受试者相似的患者的药物动力学。最大0-inf§PD评估未显示疾病恶化Inhibikase.com·:IKT 16
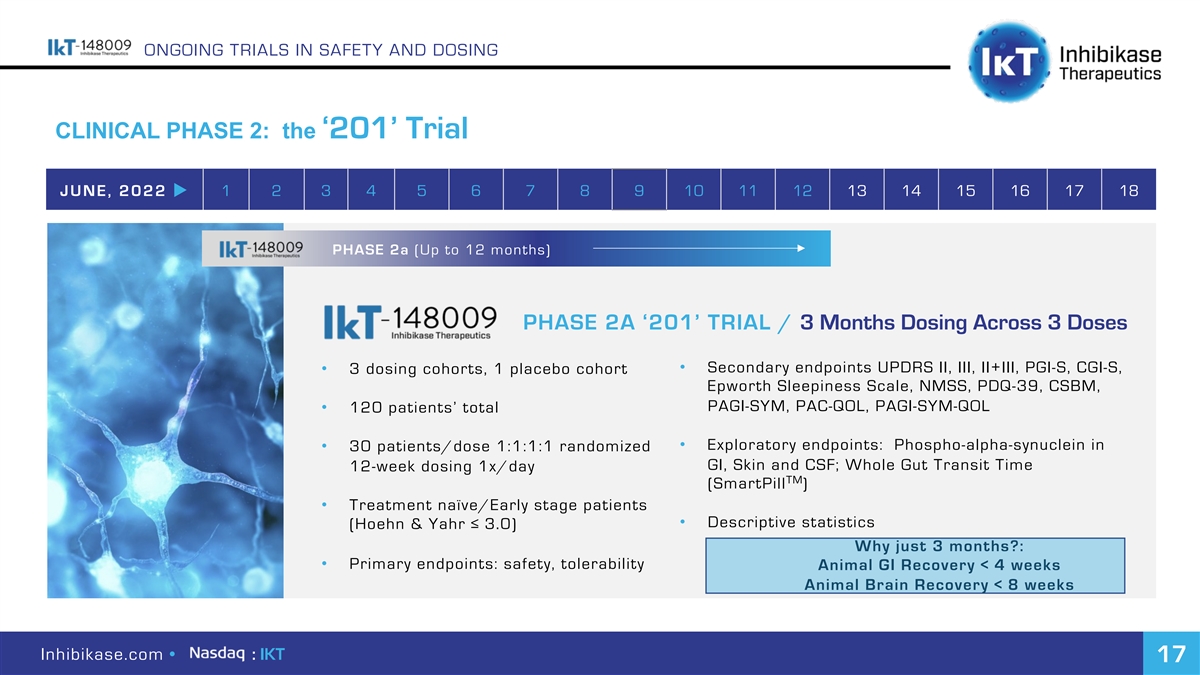
正在进行的安全性和剂量临床试验第二阶段:2022年6月1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18阶段2a(长达12个月)进行中的‘201’试验/3个月剂量·次级终点UPDR II、III、II+III、PGI-S、CGI-S、·3个剂量队列、1个安慰剂队列、Epworth嗜睡量表、NMSS、PDQ-39、CSBM、PAGI-SYM、PAC-QOL、PAGI-SYM-QOL·120例患者的总·探索终点:30例·磷酸-α-突触核蛋白/剂量1:1:1:1随机分为胃肠道、皮肤和脑脊液;全肠道转运时间12周1次/天TM(智能避孕药)·治疗幼稚/早期患者·描述性统计(Hoehn&Yahr≤3.0)为什么只有3个月?:·主要终点:安全, 耐受性动物GI恢复
稳定期慢性粒细胞白血病市场及策略 Inhibikase.com·:IKT 18
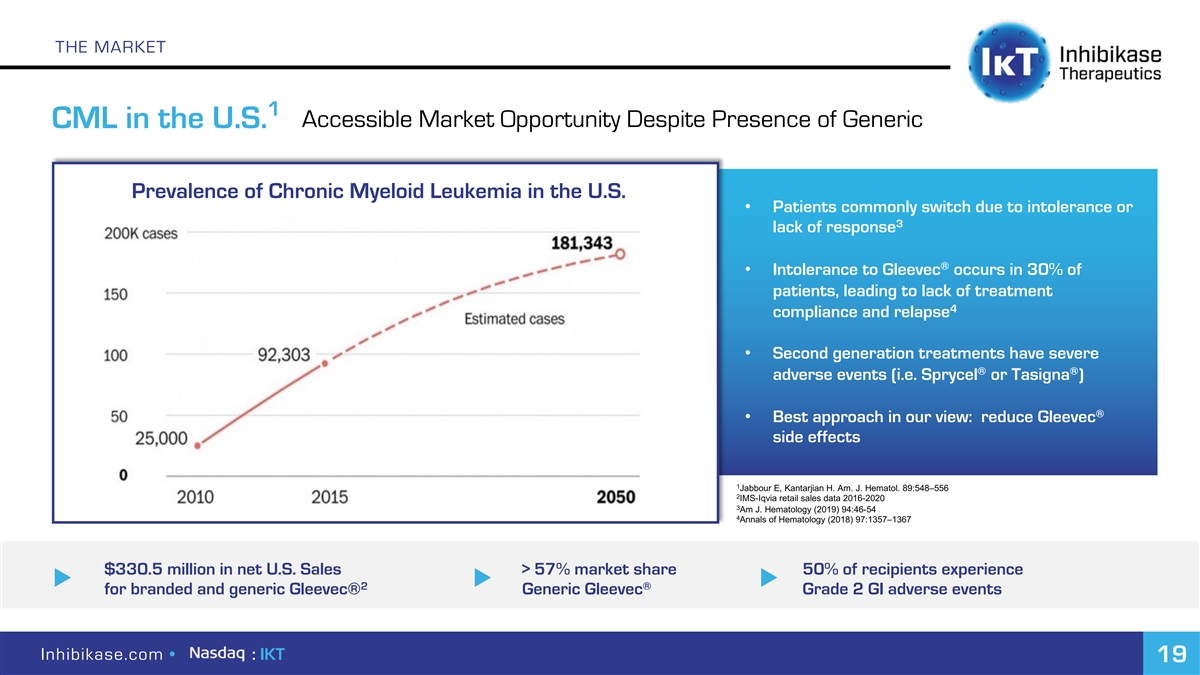
市场1可进入的市场机会,尽管美国存在非专利CML 慢性粒细胞白血病在美国的流行率·患者通常由于不耐受或3缺乏反应而转而使用®·30%的患者对格列卫不耐受,导致缺乏治疗依从性 并复发·第二代治疗有严重的®®不良事件(即Sprycel或Tasigna)®·我们认为的最佳方法:减少格列卫副作用1 Jabbour E,Kantarkin H.AmJ.血醇。血液学年鉴(2019)94:46-54 4美国血液学年鉴(2018)97:13 57-13 67美国净销售额3.305亿美元>57%市场份额50%的接受者经历了品牌和仿制药的u 2® 格列卫®通用Gleevec 2级GI不良事件Inhibikase.com
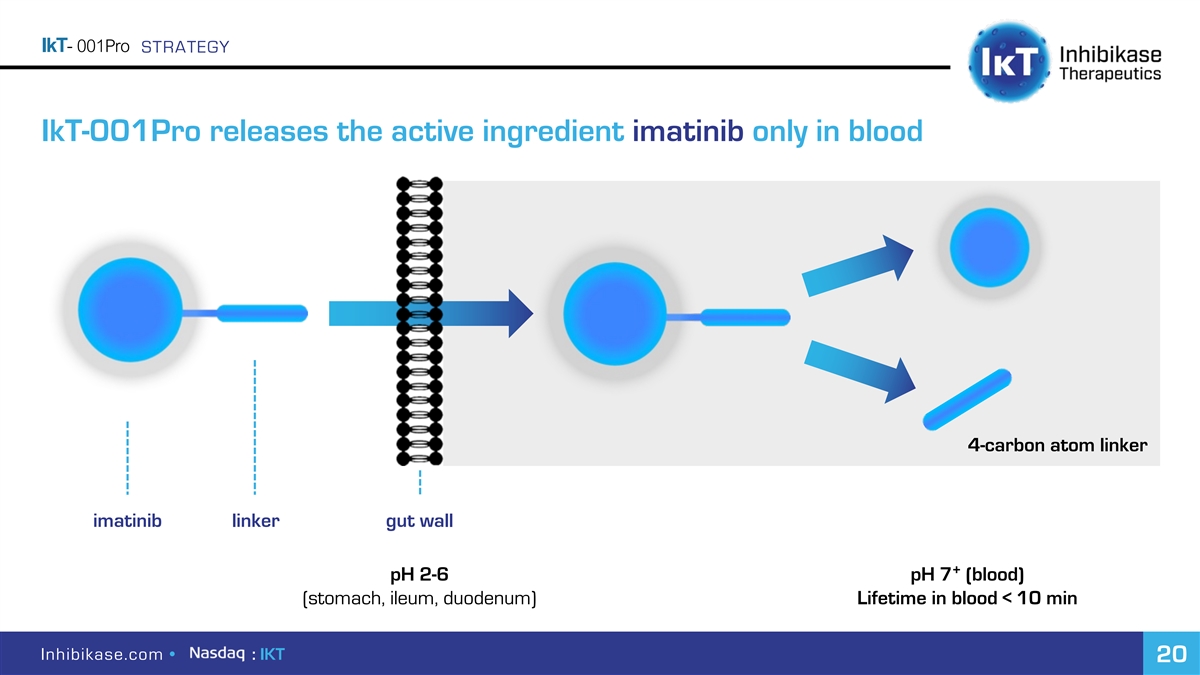
IKT-001Pro策略IKT-001Pro仅在血液中释放活性成分伊马替尼 4碳原子接头伊马替尼接头肠壁+pH 2-6 pH 7(血液)(胃、回肠、十二指肠)在血液中的寿命

IKT-001Pro是一种小分子bcr-abl抑制剂IKT-001Pro:® 替代普通格列卫的胃肠道毒性较低的IKT-001Pro在非人类灵长类动物中的测试结果表明:没有不良事件水平Cmax Tmax AUC0-T(mg/kg)ü实现剂量弹性,(Mean,ng/mL)(Mean,h)(Mean,h)Ng-h/mL)NOAEL 包括由于AEs较低而使用较高剂量的Imatinib 176/206 4/3 1540/1960 15 1(第91天)(男/女)(男/女)ü抑制胃肠道感染和其他与依从性相关的不良反应IKT-001Pro 400/318 5.3/3.75220/3890 75事件(第28天)(男/女)1 FDA 供批准的汇总数据21-335▲▲无不良事件3倍3倍增加暴露剂量更高剂量的伊马替尼作为001Pro Inhibikase.com·:IKT 21

IKT-001Pro的生物等效性和优越性临床开发试验2022年6月1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18生物等效性IKT-001Pro(最长3个月)单剂两部分生物等效性试验·第1部分:3个剂量队列,10名受试者每人发现剂量相当于400毫克甲磺酸伊马替尼IKT-001Pro,测量96小时药代动力学生物等效性·第2部分:在32名受试者中进行验证性单剂量测量,证实96小时药代动力学‘501’试验·将根据 505(B)(2)法规在NDA路径上与FDA磋商,遵循CML IKT-001Pro中501试验优于护理标准的501试验优势·等待名单交叉设计,比较001Pro和400 mg伊马替尼6个月·98名患者服用1x/天计划·主要 终点是患者报告的胃肠道紊乱和腹泻频率的结果衡量指标。·计划根据505(B)(2)法规Inhibikase.com. :IKT 22进行与追求保密协议同时进行的‘502’审判

Inh Hiib BIIK ka中的精选股票和财务数据作为Se E.C.co om m·::IKT 23 23

表2022年6月30日未偿还普通股25,227,051流动资产:期权(WAEP:2.25)4,238,056现金$32,212,276认股权证(WAEP:5.21)1,561,913应收赠款$6,552完全稀释 未偿还的30,622,020股研究和开发$919,053美元IPO前的非稀释授予收入(NIH,DoD,州政府)预付费用和其他811,482美元流动资产总流动资产33,949,363总流动负债$4,490,305营运资金29,459,058美国财政部持有的账户中可用的主动赠款资金314,228美元营运资本总额29,773,286 Inhibikase.com

公司重点介绍即将到来的里程碑:2022年第三季度IKT-001Pro· 第一个在IKT-148009 2a期研究中的随机患者·开始生物等效性临床研究·在治疗朴素帕金森患者后开始生物等效性临床研究·FDA对IND的审查或研究的接收可能继续进行·设计PK桥研究以 评估字母IKT-148009的药片配方和食物对PD患者PK的影响·设计和开发优势研究·完成IKT-001Pro相对于CML的两个动物模型验证研究中的第一个·IKT-148009在MSA中完成商业开发工作·在美国为MSA的IKT-148009文件IND;在美国寻求孤儿合作药物指定·开始表征新化合物作为 IKT-148009 Inhibikase.com·:IKT 25的后续产品

关于在药物开发和商业化方面拥有丰富经验的美国高管管理团队 米尔顿·沃纳、约瑟夫·弗拉塔罗利博士、注册会计师C.沃伦·奥兰诺医学博士、总裁&首席财务官、CLINTREX临时首席医疗官兼首席执行官。此前,沃纳博士曾担任弗拉塔罗利先生的董事 凯尔塔罗利先生是Celaxsys认证的公共研究人员。从1996年9月至2007年6月担任Henry P.and Georgette Goldschmidt教授和2007年6月董事长之前,Werner博士一直担任Henry P.and Georgette Goldschmidt教授和2007年6月董事长一职,在处理上市公司文件和西奈山医学院神经病学系方面具有丰富的经验。在加入西奈山分子生物学实验室之前,他曾在麦吉尔大学、杜克大学和纽约市洛克菲勒大学分子生物物理系任职。在整个公司中。此前,他向南佛罗里达州首席执行官提供了。他是运动障碍协会的前总裁,国际运动障碍协会的前总裁,美国运动障碍协会的前财务主管。他的科学生涯,一直是神经病学协会的财务主管和咨询服务。他曾在Michael J.Fox的创新者执行委员会任职,该委员会整合了化学、物理和生物学几个新兴的生物制药和基金会科学顾问委员会,他是科学委员会的前主席,并与巴赫曼-施特劳斯·帕金森基金会和Dystonia in Medicine的顾问委员会一起,致力于全面解决医疗器械公司的问题。沃纳博士是《责任包括资本基金会》一书的作者或合著者。奥兰诺博士是《运动障碍》杂志的前联合主编。70多篇研究文章、评论, Olanow博士在多伦多大学获得医学学位,完成了他的章节,并在哥伦比亚长老会医疗工作的纽约神经学研究所向神经学培训过渡的私人公司的研究中发表了演讲。成为公开交易的美国证券交易委员会注册商。 哥伦比亚大学中心,并在哥伦比亚大学进行神经解剖学研究生学习,撰写了600多篇神经退行性疾病领域的文章。Inhibikase.com·:IKT 26
关于美国/董事会丹尼斯·伯曼先生罗伊·弗里曼博士,医学博士保罗·格林特,医学博士伊丽莎白·奥法雷尔·联合创始人、董事会成员和/或·哈佛大学神经病学教授·20年以上生物制药经验和·25年在礼来公司工作,是许多私立 医学院和小分子研究与公司董事的种子投资者,最后担任自主和外围设备开发的首席生物技术和技术中心,包括成功的公司采购官和领导者,在公共共享服务全球负责人的审批和商业化部门中,已有5人神经紊乱。贝丝以色列女执事神经学,·曾在礼来公司担任高级管理人员 ·目前担任医学中心免疫学和肿瘤治疗学总裁,包括高级副总裁,政策莫利诺风险投资公司董事会·前世界地区主席。和金融;高级副总裁,咨询和风险投资公司,神经学研究联合会·董事,安培制药金融;首席财务官,礼来公司,自主神经和Synedgen联合创始人兼执行副总裁。美国;企业发展系统首席财务官礼来公司总裁,曾在加拿大担任高级管理职务的·总裁;以及总审计师。在托卡根之前。美国自主学会和Cerexa,森林实验室, 加入礼来公司,·种子投资人,辉瑞公司的种子投资人,联合创始人和/或前董事长,PDL BioPharma的IDEC·董事,Intervu的Geron董事会成员,Kintera,美国药物学会分部,以及先灵公司和LENSAR Inc.,gensia, 卡拉布里亚神经科。犁公司。·会计学学士,荣誉和·Autonomic主编·皇家学院MBA管理信息研究员 神经科学:印第安纳大学的基础、临床和病理学家以及医学学位体系。在圣巴塞洛缪医院疼痛杂志:伦敦大学临床学院的《临床》的编辑委员会上。 更新,和临床自主研究。·在疼痛和神经退行性疾病领域的几家公司的连续创始人,并是许多大小制药和生物技术公司的科学顾问委员会成员。Inhibikase.com ·:IKT 27

美国/业界领先的顾问瓦琳娜·道森博士,医学博士卡尔·基伯茨,公共卫生硕士罗伯特·豪泽,医学博士神经变性和干细胞计划,细胞研究所罗伯特·J·乔因特神经病学教授,工程大学神经病学系神经病学高级副院长和生理学临床研究,董事,南佛罗里达大学医学院临床与翻译科学学院,约翰霍普金斯大学医学院研究所,人类实验治疗中心创始人董事美国帕金森氏症和(CHET)-罗切斯特大学医学中心运动障碍研究中心总裁博士,医学博士,医学博士FRCPC Henry P.和Georgette Goldschmidt教授兼主席Jeffrey Kordower,西奈山医学院荣誉博士Jay Pasricha,MBBS,MD荣休,创建董事ASU-Banner神经退行性疾病首席执行官,Clintrex研究公司董事,约翰霍普金斯大学神经胃肠病研究中心(NDRC)医学教授Charlene和J.Orin Edson在生命科学生物设计研究所授予董事杰出教授,亚利桑那州立大学神经退行性疾病研究所教授Ken Marek总裁和高级科学家Ted Dawson博士,MD,神经退行性疾病和干细胞方案博士,细胞工程研究所神经、生理、药理学、干细胞系和分子科学-约翰霍普金斯大学医学院Inhibikase.com·:IKT 28

乔治亚州Riverwood Parkway Suite1900 Atlanta,GA 30339,Massachusetts Office 1 Cranberry Hill Suite 200 Lexington,MA 02421 Inhibikase.com