附件99.1
Adverum BioTechnologies报告2021年第四季度和全年财务业绩
加利福尼亚州雷德伍德城,2022年3月29日-Adverum BioTechnologies,Inc.(纳斯达克股票代码:ADVM),一家针对眼科和罕见疾病未得到满足的医疗需求的临床阶段基因治疗公司,今天公布了截至2021年12月31日的第四季度和全年的财务业绩,并提供了最新业务情况。
Adverum生物技术公司总裁兼首席执行官Laurent Fischer医学博士说:“2022年对Adverum来说将是重要的一年,因为我们计划启动一项第二阶段试验,评估两剂ADVM-022对湿性老年性黄斑变性患者的疗效。鉴于我们对使用ADVM-022治疗的所有55名患者进行了强有力的安全性审查,以及我们在湿性老年性黄斑变性和进入2024年的现金跑道的光学研究中产生的有希望的临床疗效数据,我们能够满怀信心地启动ADVM-022的第二阶段试验。我们期待着在2022年第三季度给第一名患者开药。
此外,我们继续通过聘用多名高级管理层和任命董事会成员来加强我们的领导团队,所有这些人都是各自领域的资深人士,并拥护Adverum的愿景,“Fischer继续说,”我们共同致力于推进ADVM-022的开发及其潜力,提供旨在防止湿性老年性黄斑变性患者视力丧失的一次性办公室治疗,并提供一种替代当今需要频繁注射抗血管内皮生长因子的治疗标准的方法。“
ADVM-022用于湿性老年性黄斑变性(Wet AMD)
Adverum计划启动一项第二阶段试验,以评估两种剂量水平的ADVM-022,2×10^11 Vg/眼(2E11)和新的较低剂量6 X 10^10 Vg/眼(6E10),以及新的增强型预防性类固醇疗法,预计将包括局部类固醇和局部和全身类固醇的组合。Adverum预计,这项研究将评估类似于湿性AMD第一阶段光学试验的终点。该公司预计将在2022年第三季度为第二阶段试验中的第一名患者提供剂量。
Adverum在2021年10月举行的视网膜学会第54届年度科学会议上公布了其在湿性AMD患者中进行的ADVM-022第一阶段光学试验的两年随访数据。提供的数据显示,在2E11 VG/EY ADVM-022玻璃体内注射(IVT)后,每年的抗VEGF注射减少了80%以上。此外,在湿性AMD患者中,ADVM-022耐受性良好,眼部炎症轻微,对类固醇滴眼液有反应。
其他近期亮点
·Adverum被FDA授予ADVM-062(AAV/7M8-L-opsin)孤儿药物称号(ODD),这是一种新的基因治疗候选产品,通过提供OPN1LW基因的功能副本,被开发为潜在的单一IVT用药,用于治疗蓝色锥体单色症。
·主要高管领导层成员包括首席财务官鲁珀特·德苏扎(Rupert D‘Souza)博士、医学博士斯塔·塞德卡泽米(Star Seyedkazemi)和首席医疗官理查德·贝克曼(Richard Beckman)。2021年8月加入该公司的吉姆·王(Jim Wang)博士、工商管理硕士,最近被提升为首席监管官。
·董事会增加了两名成员,任命了医学博士Rabia Gurses Ozden和M.B.A.Soo J.Hong。奥兹登博士在眼科、临床开发和手术、药物警戒、监管事务和基因治疗方面拥有20年的经验。洪女士在人力资本管理、高管和领导力发展以及高管和董事会薪酬设计和治理方面拥有深厚的专业知识,在转型期间为快速增长的组织提供服务。
预计2022年的里程碑
·2022年第2季度--于2022年5月1日在科罗拉多州丹佛市举行的视觉与眼科研究协会(ARVO)年会上发表题为“ADVM-022玻璃体内(IVT)基因治疗新生血管性AMD的第1阶段研究(光学试验):中和抗体(NAB)的作用”
·2022年第二季度-打算提供非人类灵长类蛋白质表达数据,支持人类相当剂量的ADVM-022 6 X 10^10 Vg/眼(6E10)
·2022年年中-完成IND修订程序,以启动ADVM-022在湿性AMD中的第二阶段试验
·2022年第三季度-计划在湿性AMD的ADVM-022第二阶段试验中为第一名患者提供剂量
截至2021年12月31日的三个月的财务业绩
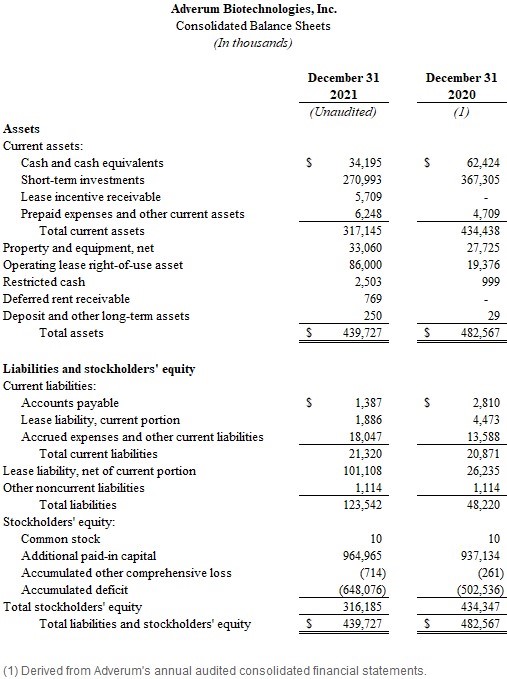
·截至2021年12月31日,现金、现金等价物和短期投资为3.052亿美元,而截至2021年9月30日为3.327亿美元,截至2020年12月31日为4.297亿美元。Adverum预计,年底的现金状况将为2024年的运营提供资金。
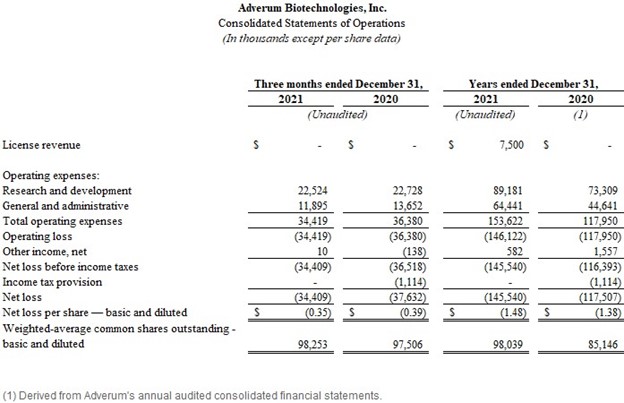
·截至2021年12月31日的三个月,研发支出为2250万美元,而2020年同期为2270万美元。研究和开发费用相对持平,主要是由于临床试验成本较低,但实验室和咨询费用略有上升。2021年第四季度,包括在研发费用中的股票薪酬支出为180万美元。
·截至2021年12月31日的三个月,一般和行政费用为1190万美元,而2020年同期为1370万美元。一般和行政费用减少的主要原因是与人员相关的和专业服务费用下降,但被Adverum新总部的保险和租赁费用增加部分抵消。2021年第四季度,包括在一般和行政费用中的基于股票的薪酬支出为270万美元。
·截至2021年12月31日的三个月,净亏损为3440万美元,或每股基本摊薄亏损0.35美元,而2020年同期为3760万美元,或每股基本摊薄亏损0.39美元。
关于Adverum生物技术公司
Adverum生物技术公司(纳斯达克代码:ADVM)是一家临床阶段的基因治疗公司,目标是治疗严重的眼科和罕见疾病,满足未得到满足的医疗需求。Adverum正在评估其新的基因治疗候选药物ADVM-022,作为一次性玻璃体内注射,用于治疗新生血管或湿性老年性黄斑变性患者。ADVM-062是一种基因治疗候选药物,专门为患有蓝色锥体单色症的患者设计。ADVM-062利用Adverum的适当载体衣壳AAV.7m8。欲了解更多信息,请访问www.Adverum.com。
前瞻性陈述
本新闻稿中包含的有关未来可能发生的事件或结果的陈述属于“1995年私人证券诉讼改革法”所指的“前瞻性陈述”。这些陈述包括但不限于关于2024年的预期当前现金跑道的陈述,以及标题为“预期的2022年里程碑”和标题为“ADVM-022用于湿性老年性黄斑变性(Wet AMD)”的陈述。由于各种风险和不确定性,实际结果可能与前瞻性声明中预期的结果有实质性差异,这些风险和不确定性包括但不限于:Adverum的新技术使其难以预测候选产品开发和获得监管批准的时间和成本;早期临床试验的结果并不总是能预测未来的结果;以及与使用ADVM-022相关的任何未来并发症或副作用,以推迟或阻止ADVM-022的监管推进或批准。Adverum面临的其他风险和不确定因素在Adverum公司提交给美国证券交易委员会的文件和报告中以“风险因素”为标题列出,这些文件和报告包括Adverum公司截至2021年9月30日的10-Q表格季度报告,以及Adverum公司未来的文件和报告,包括Adverum公司截至2021年12月31日的10-K表格年度报告。本新闻稿中包含的所有前瞻性陈述仅在发表之日发表。Adverum没有义务更新这些声明,以反映在声明发表之日之后发生的事件或存在的情况。
问询
阿南德·雷迪
副总裁,公司战略和对外事务及接洽负责人
Adverum生物技术公司
T: 650-649-1358
或
投资者:
劳伦斯·瓦茨
吉尔马丁集团
T: 619-916-7620
电子邮件:laurence@gilmartinir.com
媒体:
詹妮弗·阿库尔运河通信公司
T: 917-603-0681
电子邮件:jennifer.Arure@canalecomm.com
来源:Adverum BioTechnologies,Inc.