1.60。?GSP?是指所有适用的良好供应实践标准,包括FDA颁布或认可的当时的良好供应实践标准(如适用),该标准在《药品许可产品良好供应规范》中定义,或许可地区内同等适用的法律,每项法律均可不时修订和适用。
1.61。?HGR批准是指在中华人民共和国人类遗传资源管理局或任何其他中国政府机构进行开发活动(包括临床试验)以及根据本协议与
就在中国的领域开发许可产品进行数据传输和共享所需的任何和所有必要的记录备案和批准、许可证、
和/或许可证。
1.62。国际商会规则具有第14.4(A)节规定的含义。
1.63。国际财务报告准则是指一贯适用的国际财务报告准则。
1.64。?IND?是指
新药研究申请,或类似的申请,如在许可地区向适用的监管机构提交的临床试验申请(a?CTA?),该申请需要
在许可地区开始临床试验。
1.65。?赔偿方具有第11.3节中给出的含义。
1.66。?受偿人具有第11.3节中给出的含义。
1.67。?适应症?是指一种单独且独特的疾病或状况,或疾病或医疗状况的征兆或症状。为清楚起见,同一疾病或医疗状况的不同治疗路线或不同阶段或不同形式或不同人群(例如成人与儿童)的治疗不应构成单独的适应症。
1.68。?初始MAH?具有第5.1(E)节中规定的含义。
1.69。?发明是指在履行本协议的过程中创造、构思、开发或作出的任何和所有发明、发现和发展,无论是否可申请专利,也无论是由卡鲁纳、扎伊、双方共同或与第三方或其任何附属公司共同或代表卡鲁纳、扎伊或其任何附属公司创造、构思、开发或制造的。
1.70.?全球联合研究具有4.4(B)节中规定的含义。
1.71。?JSC?具有第3.1(A)节中规定的
含义。
1.72。?《卡鲁纳协议》具有本协议序言中所述的含义。
1.73。?卡鲁纳赔偿人具有第11.1节中规定的含义。
1.74。?卡鲁纳产品标志具有第7.5节中给出的含义。
1.75。?卡鲁纳赞助的监管和商业活动具有第5.1(E)(Ii)节所述的
含义。
1.76。?卡鲁纳赞助的研究具有第5.1(D)节规定的
含义。
1.77。?专有技术是指任何类型、任何有形或无形形式的任何专有科学或技术信息、结果和数据,包括数据库、安全信息、实践、方法、技术、规格、配方、配方、知识、专有技术、技能、经验、测试数据,包括药理、药物化学、生物、化学、生化、毒理和临床测试数据、分析和质量控制数据、稳定性数据、研究和程序,以及制造过程和开发信息、结果和数据。
6
[***] = C某件事 C非正式的 I信息 O已提交
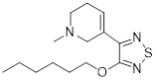 。三氯托普铵的IUPAC名称为[(1R,5S)-斯皮罗[8-偶氮双环[3.2.1]辛烷-8,1-氮唑烷-1-离子]-3-乙基] 2-羟基-2,2-二苯乙酸酯氯和
的结构
。三氯托普铵的IUPAC名称为[(1R,5S)-斯皮罗[8-偶氮双环[3.2.1]辛烷-8,1-氮唑烷-1-离子]-3-乙基] 2-羟基-2,2-二苯乙酸酯氯和
的结构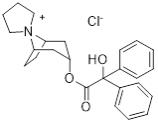 .
.