

恢复肠屏障健康企业演示文稿|2022年2月巴利(纳斯达克)|palisadeBio.com

前瞻性陈述本演示文稿中非历史事实陈述属于前瞻性陈述。这些前瞻性陈述包括但不限于有关我们的研究和临床开发计划、战略、监管事项、市场规模和机会以及我们完成某些里程碑的能力的陈述。诸如“相信”、“预期”、“可能”、“估计”、“目标”、“目标”、“计划”、“预期”、“打算”、“将会”、“可能”、“目标”、“潜在”等词汇以及类似的表述旨在识别前瞻性表述,尽管并非所有前瞻性表述都一定包含这些标识性词汇。这些前瞻性陈述是基于公司管理层的信念以及可能永远不会实现或被证明是不正确的假设。此类陈述反映了公司对未来事件的当前看法,会受到已知和未知风险的影响,包括但不限于,有关公司的商业、监管、经济和竞争风险、不确定因素、意外情况和假设,包括但不限于药品开发过程中固有的风险、公司正在进行和计划中的临床试验的未来结果、公司获得足够资金为计划中的临床试验和其他费用提供资金的能力、行业趋势、竞争格局的变化、新冠肺炎疫情造成的延误或中断。该行业和未来支出的法律和监管框架。鉴于这些风险和不确定性, 前瞻性陈述中提到的事件或情况可能不会发生。实际结果可能与预期结果不同,变化可能是实质性的。可能导致公司实际结果与当前预期不同的其他因素在公司提交给证券交易委员会的文件中进行了讨论,其中包括文件中题为“风险因素”的章节。这些前瞻性陈述不应被视为预测或承诺,也不应被视为暗示、保证或保证作出此类前瞻性陈述所依据的假设是正确或详尽的,或者就假设而言,是在本演示文稿中充分陈述的。告诫您不要过度依赖这些前瞻性陈述,这些陈述仅反映了本报告发表之日的情况。除非法律要求,否则Palisade Bio没有义务更新本文中包含的任何前瞻性陈述,以反映预期的任何变化,即使有新的信息可用。本演示讨论正在进行临床研究的候选产品,以及尚未获得美国食品和药物管理局(FDA)批准上市的候选产品。没有关于这些候选产品的安全性或有效性的陈述。当解释涉及不同候选产品的不同试验结果时,应谨慎行事。试验设计和受试者人口统计学之间存在差异,这限制了从不同试验的比较中得出的结论。本演示文稿包括我们从行业出版物、第三方研究、调查和研究中获得的统计数据和其他行业和市场数据。这些信息是从据信可靠的来源获得的。, 尽管不能保证此类信息的准确性或完整性。本文中包含的商标是其所有者的财产,仅供参考。

Palisade Bio公司开发有针对性的消化酶抑制剂Palisade Bio公司开发治疗消化酶泄漏引起的疾病的药物,这些疾病会产生炎症和组织损伤科学平台技术LB1148是一种口服液体蛋白酶抑制剂,在家中用于大手术的肠道准备,并在两个大的适应症上显示了积极的临床效果:加速术后肠功能的恢复,以及减少手术后粘连,使候选药物进入第三阶段

主药:LB1148

主要候选药物LB1148-手术患者商业化的潜在途径的要点口服消化酶抑制剂已在多项外科研究中显示出临床益处临床安全性和有效性事先批准为关键试验设计和监管审查提供了先例;LB1148进入关键研究LB1148可以在手术前在家里进行;非常大的手术市场(20%的市场份额可能带来超过15亿美元的收入)商业化的理想报销方案批准巨大的商业机会

未得到满足的需求-术后胃肠功能恢复的时间通常是出院的限制性决定因素患者通常直到排便后才出院缺乏胃肠功能恢复:引起疼痛和腹胀引起重大不适延长住院时间增加医疗成本如果我们节省一天的住院时间,我们每年将实现2000万美元的额外利润。大手术心血管、胃肠、腹部、妇科LB1148显示住院时间缩短1.1至1.3天。每个住院日的平均住院费用=2400美元

未得到满足的需求减少手术后粘连是一个普遍且潜在的严重问题:高达93%的腹部手术导致手术后粘连头号原因继发性女性不孕头号原因肠梗阻(高达75%)第十大最常见原因紧急手术死亡80%美国每年40万例粘连溶解手术美国每年23亿美元医疗费用来源:J Chir Incerale2012年;149(2):114-126。DOI:10.1016/j.jviscSurg.2011.11.006女性不孕的原因,2020年至今,K.阿尔..。结肠切除术后粘连相关并发症对医疗服务利用的影响。克莱恩。结果结果10,761-771(2018)非粘连并发症粘连并发症差异住院时间5.2天7.2天38%再住院费用22,500美元29,800美元7,326美元/分。

术后粘连限制:仅批准用于腹部手术的产品仅批准用于开腹手术,不能用于腹腔镜手术,这些产品的市场份额越来越大,只减少腹壁和潜在内脏之间的粘连,扰乱手术过程,延长麻醉药的持续时间每个适应症只有一个竞争对手;竞争对手展示了FDA批准的先例肠道功能限制的恢复:住院治疗仅限短期使用限制性REMS计划黑匣子警告:心肌梗死发病率增加只能通过限制性计划-REMS
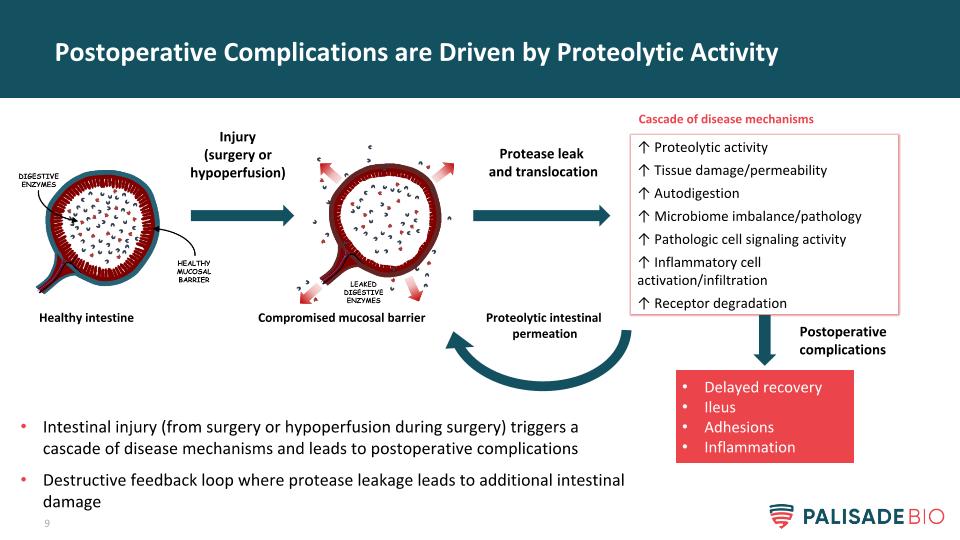
术后并发症的驱动因素是蛋白水解活性损伤(手术或低灌注)损害粘膜屏障健康肠道蛋白酶泄漏和移位↑蛋白水解活性↑组织损伤/通透性↑自体消化↑微生物群失衡/病理↑病理细胞信号活性↑炎性细胞活化/浸润↑受体降解延迟恢复肠梗阻粘连炎症级联疾病机制蛋白溶解性肠渗透损伤(手术或术中低灌注)触发一系列疾病机制并导致术后并发症破坏反馈环
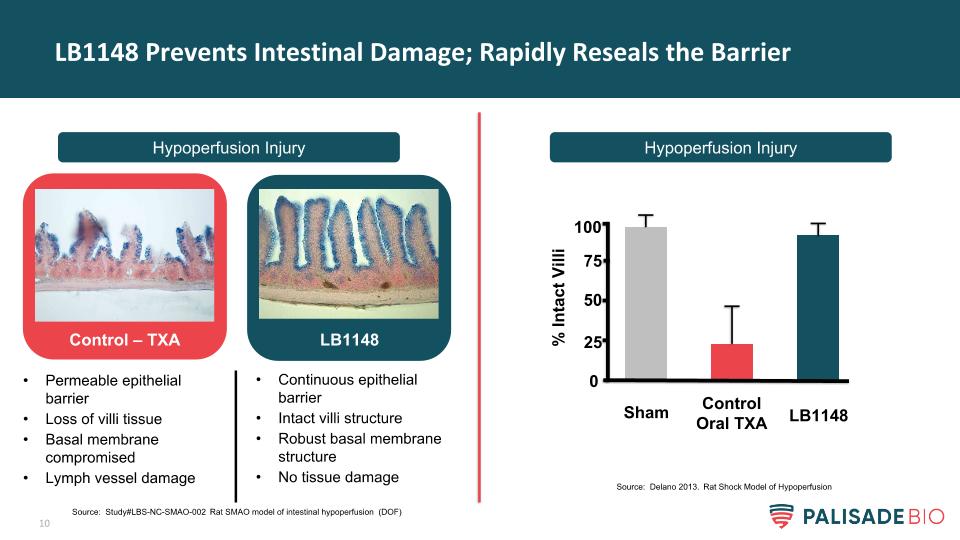
LB1148防止肠道损伤;快速修复屏障低灌注损伤对照-TXA LB1148通透性上皮屏障丢失绒毛组织基底膜受损淋巴管受损持续上皮屏障完整的绒毛结构坚固的基底膜结构无组织损伤%完好率绒毛假对照口服TXA LB1148 0 50 75 100 25来源:研究#LBS-NC-SMAO-002大鼠SMAO小肠低灌注模型(DOF)来源:Delano 2013。低灌注休克大鼠模型的建立

LB1148概述:产品中的流水线-多适应症LB1148计划临床前阶段1阶段2阶段3下一个里程碑术后肠功能恢复阶段3协议许可1H 2022;研究启动2H 2022*CV计划跟踪GI研究2022年3月16日手术后腹部粘连的预防SAGES数据介绍2022年3月16日第二阶段登记完成2H 2022*GI外科第二阶段:已完成的GI手术第二阶段:正在进行的LB1148在大中华区(不包括台湾)的商业权已被授予Newsoara心血管外科第二阶段:完成美国食品和药物管理局批准LB1148的两个临床适应症的快速通道称号:减少腹部或盆腔手术治疗术后GI的粘连

加速肠功能恢复
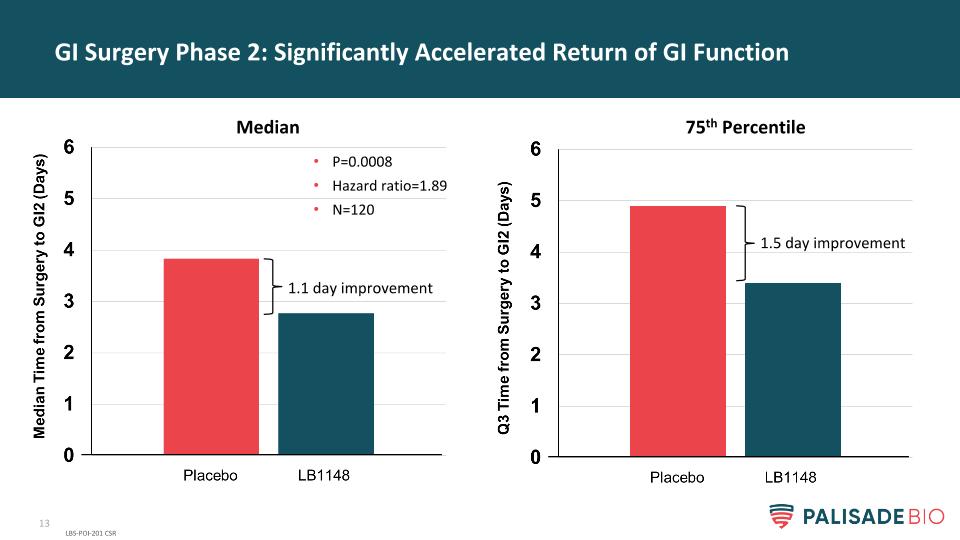
GI手术阶段2:显著加速GI功能恢复LBS-POI-201CSR P=0.0008风险比=1.89N=1201.1天改善1.5天改善中位数第75百分位数

LB1148加速胃肠道功能的恢复--在三项已完成的临床研究中,其临床疗效均达到3期一致,在统计学上具有显着性意义。在第1期胃肠道手术后,肠功能恢复的时间缩短了48%(与Enterig研究中的安慰剂相比314*)。与入院时的预期肠道功能相比,住院时间缩短了1.3天(p )

预防术后粘连
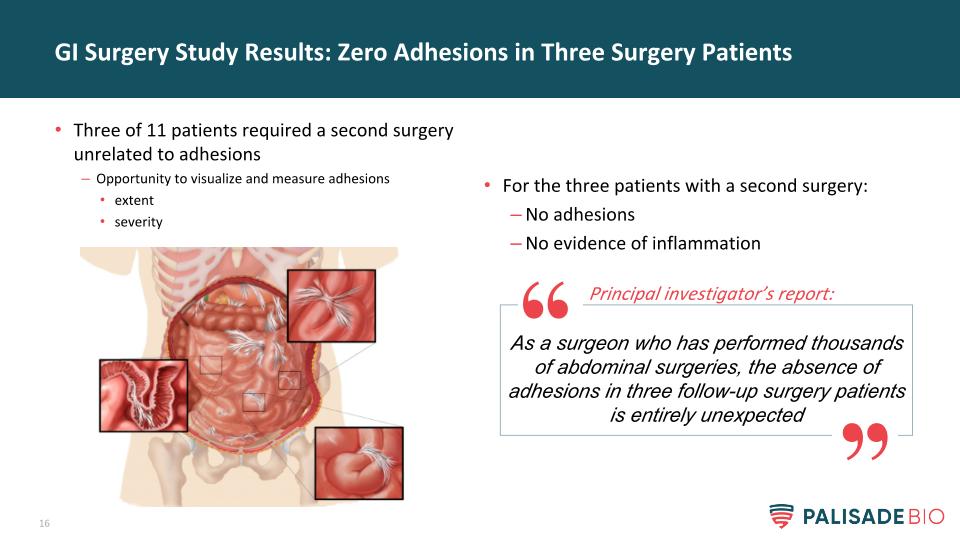
对于三名接受第二次手术的患者:没有粘连没有炎症证据的胃肠道手术研究结果:三名手术患者为零粘连11名患者中有三名需要进行与粘连无关的第二次手术机会观察和测量粘连的严重程度作为一名做过数千次腹部手术的外科医生,三名随访的手术患者没有粘连是完全出乎意料的首席调查员的报告:

LB1148商机
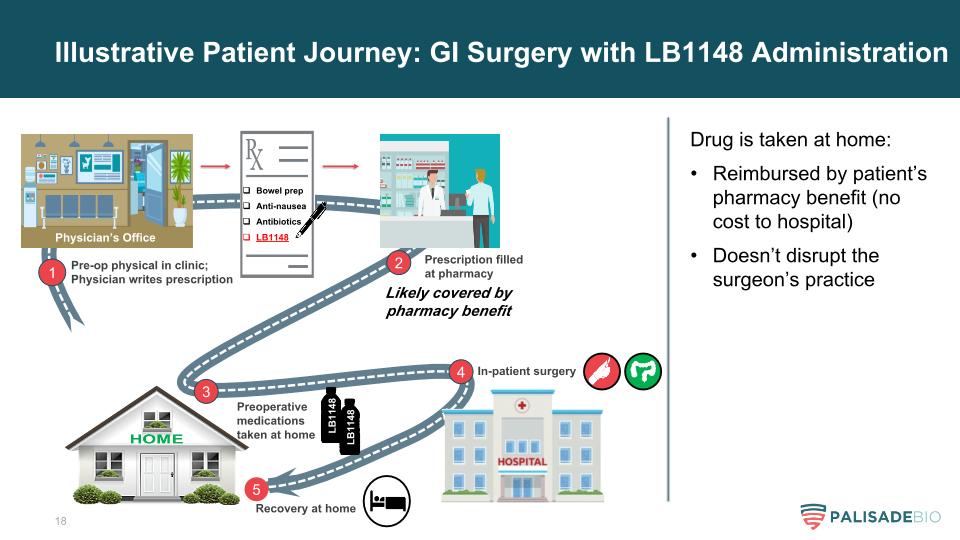
说明性患者之旅:GI手术使用LB1148管理1术前临床体检;医生写处方肠道准备抗恶心抗生素LB1148可能由药房福利覆盖2处方在药房配药3术前药物在家服用LB1148 4住院手术5在家康复药物在家服用:由患者的药房福利报销(不支付医院费用)不会扰乱外科医生的执业LB1148医生办公室

LB1148拥有巨大的全球市场机会美国市场110万例心内直视手术560万例腹部手术20-40%的市场渗透率可转化为超过20亿美元的收入与中国合作:W/Newsoara EU和ROW机会潜在地与美国的权利或独立合作美国战略通过向5000家医院营销进行商业化并购-显示粘合市场的价值巴克斯特在2020年以3.5亿美元从赛诺菲手中收购了医疗器械SepraFilm,销售额是3.5倍

加利福尼亚州卡尔斯巴德210卡尔斯巴德套房5800ARMADA DR,邮编:92008858-704-4900IR@palisadeBio.comPALI(纳斯达克)www.palisadeBio.com

附录幻灯片

由FDA批准的成分组成的新型口服制剂广谱丝氨酸蛋白酶抑制剂(氨甲环酸)已知的安全性简介计划利用505(B)(2)途径获得批准用于减少手术粘连的快速通道指定用于减少接受心内直视手术的儿童患者术后胃肠道功能障碍为药品颁发专利自2008年以来,没有批准用于术后肠梗阻的新药Enterig具有严格的黑盒警告、繁琐的REMS方案和有限的使用LB1148--快速调节途径;有限竞争

Enteregg:只有被批准用于加速胃肠道功能恢复的药物提供了FDA批准的先例途径,该药物由GSK/Adolor/Cubist开发,现为默克公司所有,表明可改善术后肠功能恢复第三阶段*:肠功能恢复17小时改善住院时间7小时Enterig MOA存在安全风险ENTEG MOA LB1148具有完全不同的MOA限制包括*:住院管理仅限短期使用,仅限限制性REMS计划,针对少数医院使用的严重副作用的黑匣子警告Program-REMS Enterig的FDA批准提供了监管路线图LB1148临床试验设计

LB1148计划概述产品中的流水线-多适应症加速术后胃肠功能恢复,减少术后粘连心血管手术、胃肠手术、腹部手术

心血管外科(低灌注损伤)

CV手术完成阶段2:研究设计*研究第0天是手术日。筛查期CV手术术后/出院LB1148天-42至-1天0天*随访1-14天30天安慰剂心血管手术需要体外循环的心内直视手术随机、双盲、安慰剂对照,在接受CABG和/或心脏瓣膜置换手术的受试者中,在0、1和2天随机选择1:1 7.5克,每日1次。研究设计120名接受择期心脏手术的患者,单中心CRO:IQVIA,2020年公布的数据范围和时间表ICO:IQVIA
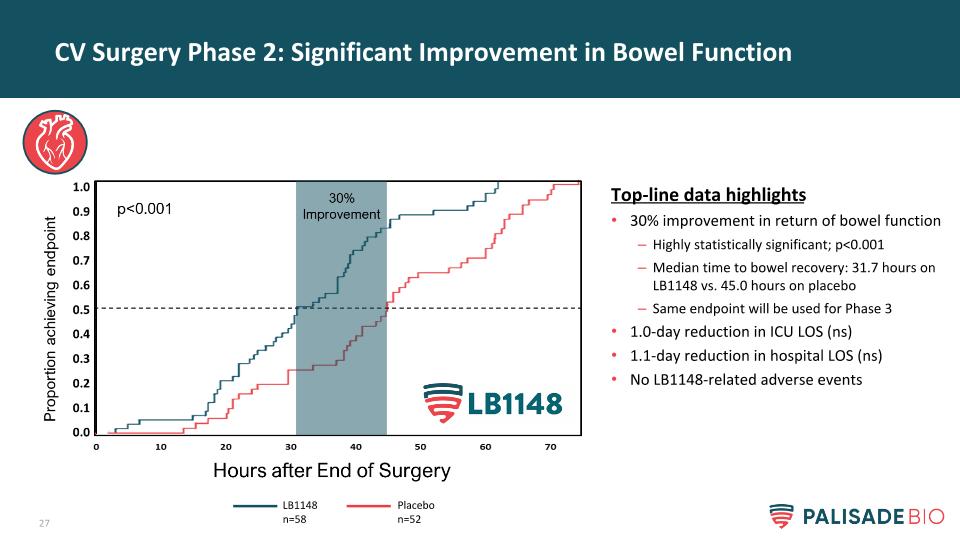
CV手术阶段2:肠功能的显著改善顶线数据突出显示肠功能恢复30%的改善具有高度统计学意义;p

胃肠道手术:肠功能恢复(身体损伤)
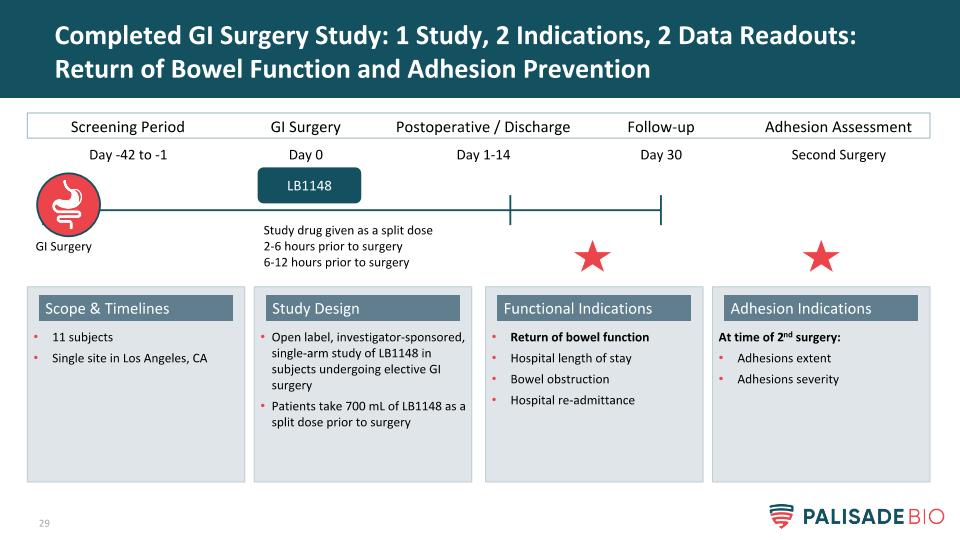
完成胃肠道手术研究:1项研究,2个适应症,2个数据读数:肠功能恢复和粘连预防开放标签,研究人员赞助的单臂LB1148研究在接受择期胃肠道手术的受试者中,患者在手术前服用700毫升LB1148作为分次剂量设计11名受试者在洛杉矶的单一地点,第二次手术时的CA范围和时间表:粘连程度粘连严重粘连指征肠功能恢复住院时间肠梗阻医院再入院功能指征筛查期GI手术术后/出院LB1148天-42至-1天0天1-14随访第30天30天研究药物在手术前2-6小时分次给药手术前6-12小时手术前6-12小时粘连评估第二次手术GI手术
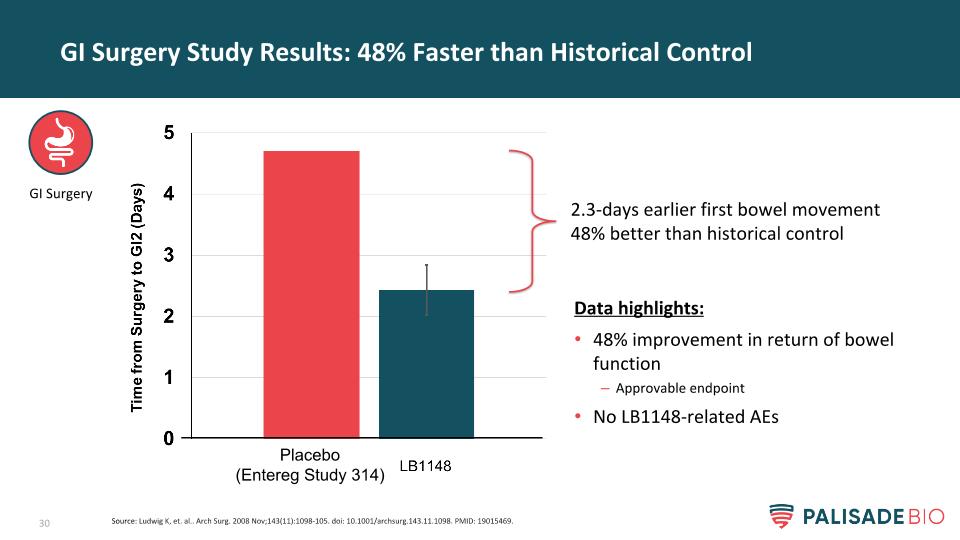
GI手术研究结果:比历史控制数据突出48%:肠功能恢复48%可批准终点No LB1148相关AEs 2.3天第一次排便比历史控制GI手术好48%来源:Ludwig K,et。阿尔..。“拱门外科”,2008年11月;143(11):1098-105。DOI:10.1001/archSurg.143.11.1098.19015469。安慰剂(肠道研究314)

GI外科研究结果:与预期的LOS GI手术相比,住院时间有显著改善患者从手术到出院的实际住院时间(LOS)与从入院时的账单代码(GMLOS)确定的预期LOS进行了比较,LOS减少了1.3天,LOS减少了20%,p=0.03

GI手术(Profile)阶段2-伙伴研究GI手术随机、双盲、安慰剂对照、多部位第二阶段试验评估LB1148在接受择期肠道切除(采用剖腹手术或计划拆除造口的微创入路)受试者的GI功能和粘连恢复情况研究设计120名患者第二次手术时在中国6个地点范围:粘连的存在粘连对肠功能和疼痛粘连指征的影响主要终点:恢复GI功能的时间GI2:(第一次排便)次要终点:医院对解决POI功能指征的损失时间筛查期GI手术时的范围:粘连的存在对肠功能和疼痛粘连指征的影响GI2:(第一次排便)次要终点:解决POI功能指征的住院损失时间筛查期GI手术术前2-6小时分次给药,术前6-10小时进行粘连评估,首次手术后最多7个月服用安慰剂

胃肠道手术第二阶段:安全和耐受性良好的LB1148是耐受性良好的药物相关不良事件LB1148=10.9%安慰剂=4.8%最常见的与药物相关的不良反应是胃肠道疾病LB1148 4.7%安慰剂3.2%在试验中没有发生与药物相关的严重不良事件

胃肠道手术:减少粘连(身体损伤)
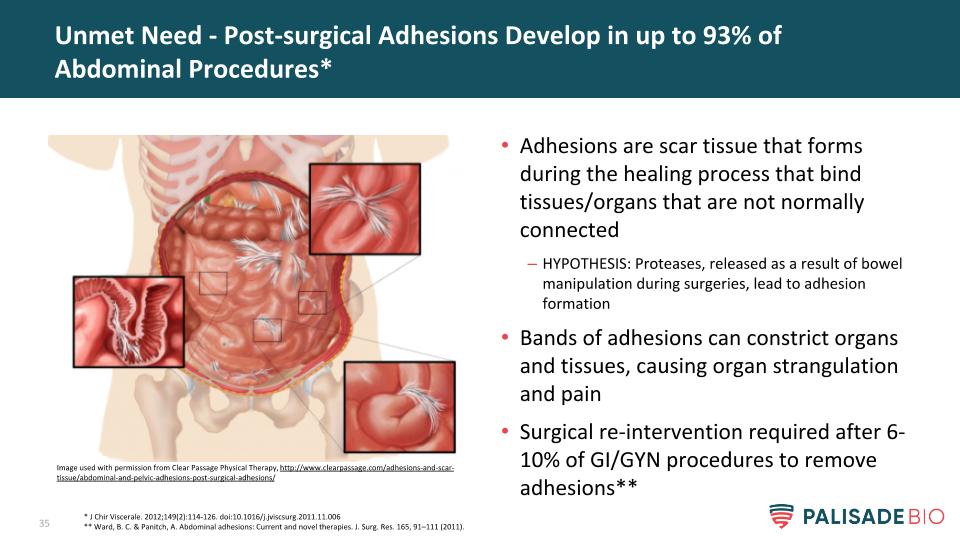
粘连是愈合过程中形成的疤痕组织,它绑定了未正常连接的组织/器官假设:手术中操作肠道时释放的蛋白酶会导致器官和组织发生粘连,粘连的条带会收缩器官和组织,造成器官窒息和疼痛,6-10%的GI/GYN手术后需要再次干预以解除粘连**未得到满足的需求-高达93%的腹部手术后会发生粘连**J Chir内脏。2012年;149(2):114-126。DOI:10.1016/j.jviscSurg.2011.11.006**Ward,B.C.&Panitch,A.腹部粘连:当前和新的治疗方法。“外科学报”165,91-111(2011)。经http://www.clearpassage.com/adhesions-and-scar-tissue/abdominal-and-pelvic-adhesions-post-surgical-adhesions/透明通道理疗中心许可使用的图像
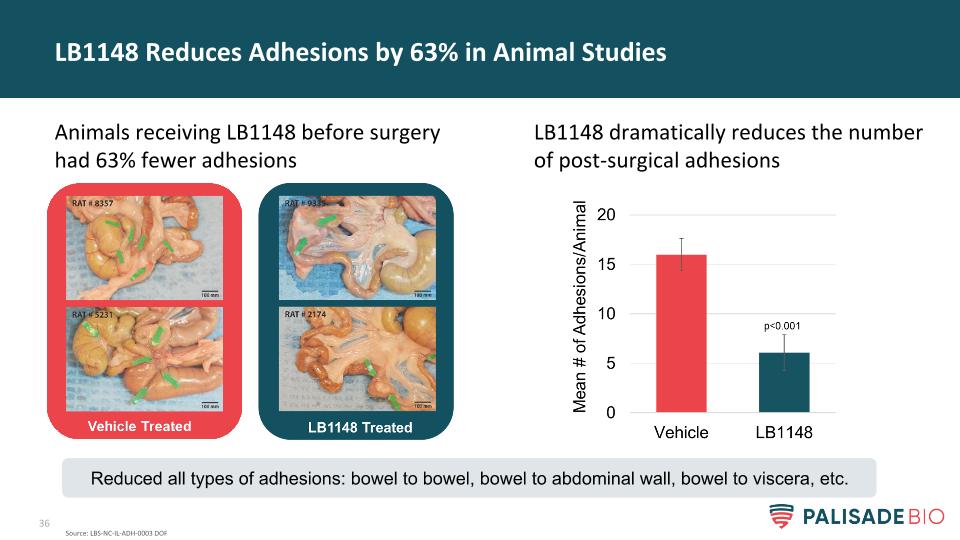
LB1148大大减少了手术后粘连的数量LB1148在动物研究中减少了63%的粘连在手术前接受LB1148的动物粘连减少了63%来源:LBS-NC-IL-ADH-0003 DOF减少了所有类型的粘连:肠与肠、肠与腹壁、肠与内脏等。

美国食品和药物管理局批准ADEPT用于盆腔手术,粘连仅减少10%来源:ADEPT(4%二十碳糊精)包装插入;2006年3月www.accessdata.fda.gov/cdrh_docs/pdf5/P050011B.pdf FDA批准ADEPT仅基于10%的患者获得“成功”(定义为减少≥3个部位的粘连)

加利福尼亚州卡尔斯巴德210卡尔斯巴德套房5800ARMADA DR,邮编:92008858-704-4900IR@palisadeBio.comPALI(纳斯达克)www.palisadeBio.com