①諾和諾德公佈司美格魯肽2.4毫克對肝纖維化和MASH顯著改善的Ⅲ期試驗第一階段結果;②試驗顯示,司美格魯肽組37.0%的患者肝纖維化改善且無脂肪性肝炎惡化,安慰劑組爲22.5%;③諾和諾德預計2025年上半年向美國和歐盟提交監管批准,MASH影響美國約5%的成年人。
財聯社11月2日訊(編輯 趙昊)當地時間週五(11月1日),諾和諾德在官網公佈了正在進行的一項Ⅲ期試驗第一階段的結果,司美格魯肽2.4毫克顯示出對肝纖維化和MASH消退的顯著改善。

代謝功能障礙相關脂肪性肝炎(MASH,曾稱爲NASH)由代謝功能障礙相關脂肪性肝病(MASLD)進一步發展而來。MASH患者常常伴隨着脂肪變性、炎症和肝纖維化,並可進一步發展爲肝硬化。
如果不及時治療,肝硬化風險將增加,誘導患者出現肝衰竭和肝癌,最終導致死亡。因此在MASH藥物的臨床試驗中患者纖維化改善程度是常用的主要終點。
由於發病機理複雜,其很長一段時間都是醫藥行業的研發黑洞,不少藥企屢屢失敗。
諾和諾德的「ESSENCE」是一項關鍵的Ⅲ期、爲期240周的雙盲試驗,參與者爲1,200名患有MASH和中度至晚期肝纖維化的成年人,在標準治療基礎上按2:1的比例分爲2.4mg司美格魯肽組和安慰劑組。
試驗實現了主要終點:第72周時,司美格魯肽組37.0%的患者肝纖維化改善且無脂肪性肝炎惡化,安慰劑組這一比例爲22.5%;司美格魯肽組62.9%患者脂肪性肝炎緩解且肝纖維化無惡化,安慰劑組爲34.1%。
司美格魯肽還顯示出安全性和良好的耐受性,諾和諾德研發執行副總裁Martin Holst Lange寫道,「我們對ESSENCE臨床試驗結果以及司美格魯肽幫助MASH患者的潛力感到非常高興。」
諾和諾德預計將於2025年上半年向美國和歐盟提交監管批准。Lange補充道,「在超重或肥胖人群中,三分之一患有MASH。這對他們的健康產生了嚴重影響,代表着一項尚未得到滿足的重大需求。」
數據公佈後,在美股交易的諾和諾德股價變化不大;而Madrigal Pharmaceuticals漲超19%,漲幅最大時接近24%,因其藥物Rezdiffra是美國首款,也是當前唯一的MASH藥物。
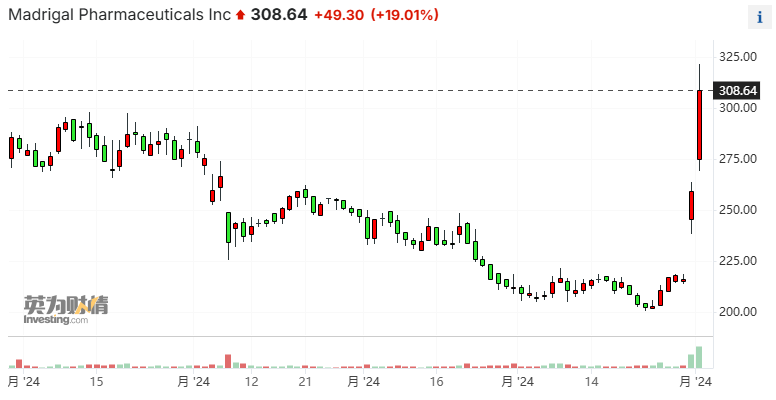
Rezdiffra是40年來首款獲FDA批准上市的MASH藥物。Piper Sandler分析師Yasmeen Rahimi看好Madrigal的長期前景,「因爲大型製藥公司有資源大幅擴大這個市場,爲Rezdiffra創造更大的機會。」
根據美國肝臟基金會的數據,MASH影響了美國約5%的成年人,因此患者群體十分龐大。今年6月時,禮來也公佈了tirzepatide治療MASH二期臨床試驗的積極結果。

 如果不及时治疗,肝硬化风险将增加,诱导患者出现肝衰竭和肝癌,最终导致死亡。因此在MASH药物的临床试验中患者纤维化改善程度是常用的主要终点。
如果不及时治疗,肝硬化风险将增加,诱导患者出现肝衰竭和肝癌,最终导致死亡。因此在MASH药物的临床试验中患者纤维化改善程度是常用的主要终点。