憑藉其獨有的Trimer-Tag技術平台,三葉草生物的RSV候選疫苗SCB-1019有望成爲潛在同類最佳,重塑RSV疫苗的市場格局~
當前正是第三季度業績期,中國疫苗行業在當前經濟週期波動下業績承壓,以往熱賣的疫苗大品種也在面臨國內市場進一步降價競爭的挑戰。作爲生物醫藥細分賽道的國產創新疫苗行業,如何尋找到一條破局企穩,撥雲見日的路徑,是決定各國產疫苗廠家未來商業生死的核心戰略考量。
與此同時,近期創新生物藥其他細分賽道,例如雙抗,創新小分子藥,核藥等領域,均有國產企業自主研發的潛在同類最佳(Best-in-Class)生物資產,被國際大藥企(MNC)以數千萬甚至數億美金購買其海外權益。這表明在2018年至2021年受到資本熱潮孵化的中國生物創新藥賽道上,真正有自主研發創新實力的國產生物創新藥企業代表,正在引領中國創新生物資產「出海」。在這樣的行業大趨勢下,我們期待具備自研創新疫苗出海能力的國產創新疫苗企業也儘快趁浪揚帆。以實力過硬的自研創新疫苗產品「出海」廣袤的國際市場,很有可能是國產疫苗行業破局當前國內運營挑戰的唯一可行性路徑。在這個思路下,2021年底港股上市的三葉草生物(02197)進入我們的視野。
 三葉草生物擁有自研的Trimer-Tag (蛋白質三聚體化)疫苗開發技術平台,且該技術平台已得到全面驗證: 基於該技術平台自研的新冠疫苗 (SCB-2019) 在全球八個國家、五大洲有近4萬人入組多項III期臨床試驗,後在中國獲得緊急使用授權(EUA)。從2023年中開始,三葉草生物以其自研新冠疫苗所累積的豐富經驗和資源,結合自身技術平台特點,以潛在商業價值最大化爲導向佈局管線研發,開始集中快速推進自研的呼吸道合胞病毒(RSV)候選疫苗SCB-1019。2023年12月初,三葉草生物宣佈啓動RSV候選疫苗I期臨床試驗,成爲中國首家開發 RSV PreF (基於融合前構象的F蛋白) 疫苗並進入人體臨床試驗階段的疫苗公司,這堅定了三葉草生物在中國RSV領域的領跑地位。
三葉草生物擁有自研的Trimer-Tag (蛋白質三聚體化)疫苗開發技術平台,且該技術平台已得到全面驗證: 基於該技術平台自研的新冠疫苗 (SCB-2019) 在全球八個國家、五大洲有近4萬人入組多項III期臨床試驗,後在中國獲得緊急使用授權(EUA)。從2023年中開始,三葉草生物以其自研新冠疫苗所累積的豐富經驗和資源,結合自身技術平台特點,以潛在商業價值最大化爲導向佈局管線研發,開始集中快速推進自研的呼吸道合胞病毒(RSV)候選疫苗SCB-1019。2023年12月初,三葉草生物宣佈啓動RSV候選疫苗I期臨床試驗,成爲中國首家開發 RSV PreF (基於融合前構象的F蛋白) 疫苗並進入人體臨床試驗階段的疫苗公司,這堅定了三葉草生物在中國RSV領域的領跑地位。
很快,2024年4月和6月三葉草生物分別披露其二價RSV候選疫苗SCB-1019 Ⅰ期臨床試驗在年輕成年人和老年人群組獲得積極初步數據。短短四個月後,三葉草生物又成爲全球首家公佈其RSV候選疫苗與已獲批商業化的國際龍頭RSV疫苗產品頭對頭臨床試驗結果的廠家,引來全球同行及資本市場的高度關注。當下全球已經有三家大藥企巨頭擁有已獲批的針對老年人的RSV疫苗產品,三葉草生物自研的RSV候選疫苗又有何高度差異化的優勢能夠實現彎道超車,從而達到最終出海的戰略目的,值得深究和關注!
潛在同類最佳,SCB-1019嶄露頭角
10月29日,三葉草生物發佈公告稱,其在I期臨床試驗中評估未使用佐劑的二價RSV PreF-三聚體亞單位候選疫苗SCB-1019與GSK使用AS01E佐劑的RSV疫苗AREXVY進行頭對頭比較後,在老年人受試者中獲得了更多積極的免疫原性和安全性數據。
免疫原性方面,在第28天,未使用佐劑的SCB-1019誘導的RSV-A和RSV-B中和抗體幾何平均滴度(GMTs)分別約爲30500IU/mL及32000IU/mL;而AREXVY誘導的RSV-A和RSV-B中和抗體幾何平均滴度(GMTs)分別約爲26700IU/mL及37700IU/mL;安慰劑組分別約爲3300IU/mL及2900IU/mL。
安全性方面,與GSK使用AS01E佐劑的RSV疫苗AREXVY(76.7%)相比,未使用佐劑的SCB-1019(16.7%)的局部不良事件(AEs)發生率明顯較低。
表明,SCB-1019的耐受性總體良好,且SCB-1019的局部和全身不良事件(AEs)總體較輕,與生理鹽水安慰劑組相當。
值得一提的是,在全球已經商業化上市的RSV疫苗中,從銷售數據來看,GSK的AREXVY可以說是RSV疫苗屆的扛把子,因此三葉草生物公佈其未使用佐劑的RSV候選疫苗SCB-1019與GSK使用AS01E佐劑的AREXVY頭對頭臨床試驗結果,且數據相當積極:效價相當的同時安全性更優,足見三葉草生物的SCB-1019有成爲同類最佳的潛力。
據智通財經APP了解,RSV是一種常見的呼吸道病毒,目前市面上並沒有特效藥,只能針對RSV感染引發的併發症進行對症治療,因此接種疫苗進行主動預防是當下避免RSV重症感染和減少死亡的關鍵有效措施。
事實上,自20世紀60年代以來,開發RSV疫苗一直是WHO的一個優先事項。由於RSV病原體致病機理複雜,因此多年來很多大藥企都在RSV疫苗開發上折戟。
直到去年,也就是2023年,GSK宣佈其呼吸道合胞病毒(RSV)疫苗Arexvy獲美國食品藥品監督管理局(FDA)批准上市,用於老年人群體預防RSV感染導致的下呼吸道疾病,才成功實現了RSV感染零預防的突破。
目前,全球範圍內有四款RSV疫苗、預防藥物獲批上市,分別是葛蘭素史克(GSK)研發的Arexvy、輝瑞(Pfizer)研發的ABRYSVO、賽諾菲和阿斯利康研發的Nirsevimab(尼塞韋單抗)以及Moderna研發的mRNA-1345。
從技術路徑和保護效力上看,GSK和輝瑞的RSV疫苗都屬於重組蛋白路線。GSK的AREXVY是單價RSV疫苗,使用了佐劑,保護力比其他RSV疫苗高,達到82.6%,預防嚴重RSV相關下呼吸道疾病的保護效力達到94.1%;輝瑞二價的RSV疫苗保護力則在60%上下;Moderna的單價RSV疫苗今年5月才上市,技術路線是mRNA,保護效力也在80%以上,然而今年年中CDC披露該單價RSV疫苗有效保護效力不足以覆蓋一個完整流行季節,在接種8個月後就會下降到不足50%的保護效力。mRNA技術路線的RSV疫苗商業化前景堪憂,Moderna的股價也從6月底至今跌去近50%。而同期公佈的以重組蛋白路線爲主的GSK和輝瑞的RSV疫苗,其保護效力持久性在2年左右。因此當下從保護效力和保護持久性角度而言,重組蛋白路線的RSV疫苗優於mRNA路線的RSV疫苗。
從目前商業銷售結果上看,GSK的RSV疫苗佔據優勢。2023年,GSK的RSV疫苗銷售額爲15.64億美元,輝瑞的則實現8.9億美元的銷售額,只有GSK的一半。GSK公司CEO艾瑪·沃姆斯利曾表示,其RSV疫苗已佔據美國三分之二的市場。
儘管RSV疫苗的首次銷售在一個季度就創下近13億美金的行業記錄,全球RSV疫苗能否成爲下一個百億美金大單品取決於未來重複接種的市場機會。而兩款已獲批商業化的重組蛋白路線的RSV疫苗,根據其之前和最新的臨床數據顯示,均面臨有效重複接種的問題。因爲不管是GSK還是輝瑞,各自III期臨床數據均顯示在接種首針後的12個月或者24個月後,再接種疫苗所誘導的中和抗體滴度水平都只能回到首針峯值水平的約45-60%。其中GSK有披露過一個III期臨床保護效力數據,顯示首針間隔12個月後的重複接種,其不及首針中和抗體滴度峯值55%所對應的保護效力,對照安慰劑組等同於沒有保護效力。從科學角度推斷,這兩家企業的RSV疫苗抗原不同,但在三聚體標籤上都是用了T4-Foldon技術。考慮到該技術本身就是一個抗原,有可能進入人體後引起免疫干擾,因此可能導致了重複接種效果不佳的問題。
當下GSK和輝瑞宣佈正在進行間隔3年和4年重複接種的III期臨床試驗,但兩家RSV疫苗的保護效力持久性數據顯示,大約每2年就需要重複接種一次。那麼誰能補缺?
國際大藥企三款針對老年人的已獲批商業化的RSV疫苗產品,其中兩款面臨有效重複接種的挑戰,另外一款的保護效力甚至不能覆蓋一個完整的疾病流行季。當前國際巨頭的產品缺陷,對於三葉草生物及全球各家生物創新疫苗企業就意味着潛在彎道超車的機會。
看回三葉草生物,其未使用佐劑的二價重組蛋白RSV候選疫苗SCB-1019基於其自研的Trimer-Tag技術平台所開發。Trimer-Tag是全球唯一一個利用人源共價三聚體化標籤的重組蛋白疫苗技術,共價的結合可保持穩定天然三聚體抗原的結構,因此可誘導強烈和精準的中和免疫應答,且根據過往的臨床試驗經驗,未觀察到免疫干擾和預存免疫。在當前開展的澳洲I期臨床上,SCB-1019通過頭對頭比較GSK的AREXVY所展現出來的積極數據,使得SCB-1019在RSV疫苗中潛在同類最佳的保護效力得到有力保障。據悉,三葉草生物計劃在2025年啓動臨床試驗評估SCB-1019在RSV疫苗重複接種的應用,值得期待和關注。
基於Trimer-Tag平台,RSV疫苗及其他呼吸道聯苗有望被快速開發
在呼吸道疫苗領域,開發高效的聯合疫苗是整個行業的發展趨勢。同樣,對於RSV疫苗市場而言,各家企業長遠的管線規劃也是開發相關的呼吸道聯合疫苗,切入更大的商業化市場機會。值得一提的是,流感病毒、呼吸道合胞病毒(RSV)以及SARS-CoV-2病毒,已成爲重大的全球公共衛生挑戰。季節性流感每年影響全球5%至10%的成年人和20%至30%的兒童,導致300萬至500萬重症病例,並造成約29萬至65萬人死亡。
2019年,由SARS-CoV-2引發的冠狀病毒病(COVID-19)大流行更是雪上加霜,全球報告至少7.75億例病例,約700萬人因此喪生。
在COVID-19之後,流感和SARS-CoV-2等病毒的共同感染現象已被多項研究證實,其患病率範圍從0.2%至48%不等。此類合併感染通常導致病情加劇及病程延長。
因此,研發聯合呼吸道疫苗也逐漸成爲疫苗研發的新焦點,這一趨勢的核心在於通過單一疫苗提供針對多種呼吸道病毒的保護,從而減少接種次數,提高接種率,並擴大免疫覆蓋範圍。
三葉草生物的Trimer-Tag(蛋白質三聚體化)疫苗研發技術平台,特別適合結合多個具有類似結構的呼吸道病毒抗原。這一平台能夠促進疫苗抗原的穩定性和免疫原性,爲開發多價或聯合疫苗提供了堅實的基礎。尤爲重要的是,三葉草生物基於該平台在RSV疫苗研發方面積累的寶貴經驗也爲呼吸道聯合疫苗的開發鋪平道路。
目前三葉草的RSV候選疫苗SCB-1019正被用於開發單正黏病毒目病毒的呼吸道聯合疫苗(RSV+hMPV±PIV3),並計劃於2025年啓動臨床試驗評估SCB-1019在呼吸道聯合疫苗的應用。如果其呼吸道聯苗的有效性得到臨床驗證其候選疫苗產品出海的實力則更上一層樓。
全球RSV疫苗商業化前景及市場競爭
由於RSV疫苗2023年下半年開始銷售就錄得近25億美金,GSK和輝瑞的成功進一步驗證了RSV市場的巨大潛在需求,也給後續研發企業吃了一顆定心丸。根據灼識諮詢研究數據,RSV藥物全球整體市場規模(包括治療藥物及預防藥物),預計將從2020年的18億美元增長至2030年的128億美元,年均複合增長率達到21.4%。
而根據ClinicalTrials數據庫,截至2023年9月,全球已有超過20款不同技術路徑的RSV疫苗與抗體藥物研發管線陸續進入臨床研究階段。
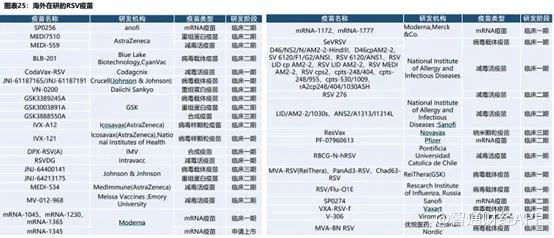
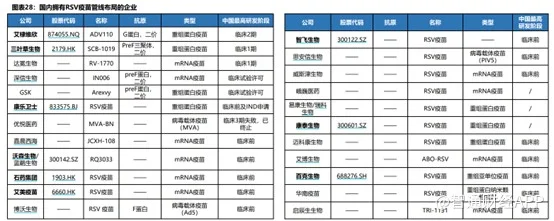
儘管參與RSV疫苗開發的企業衆多,但是RSV疫苗研發壁壘極高,成功開發安全有效的RSV疫苗道阻且長。而憑藉獨創且成熟的Trimer-Tag技術平台,三葉草生物的RSV候選疫苗SCB-1019有望成爲潛在行業最佳,並在國產RSV疫苗開發中處於領先梯隊,非常有機會成爲國產生物創新疫苗成功出海的代表。
結語
隨着RSV疫苗市場的迅速發展,三葉草生物憑藉其獨有的Trimer-Tag技術平台和RSV候選疫苗SCB-1019展現了在這一領域的巨大潛力。根據臨床試驗數據,三葉草生物的二價RSV PreF-三聚體亞單位候選疫苗不僅在免疫原性和安全性方面表現優異,還有望解決現有商業化的RSV疫苗重複接種效果不佳的問題,且評估其在呼吸道聯合疫苗中應用的臨床也值得期待。
儘管RSV疫苗市場目前由GSK等國際製藥巨頭主導,但三葉草生物憑藉其獨特優勢,正逐步確立其在國內乃至全球RSV疫苗研發中的領先地位。未來,隨着更多臨床試驗的推進及潛在呼吸道聯合疫苗的開發,三葉草生物有望爲抵禦RSV感染提供更加有效、持久的解決方案,並進一步擴大其在全球生物健康領域的影響。

 三叶草生物拥有自研的Trimer-Tag (蛋白质三聚体化)疫苗开发技术平台,且该技术平台已得到全面验证: 基于该技术平台自研的新冠疫苗 (SCB-2019) 在全球八个国家、五大洲有近4万人入组多项III期临床试验,后在中国获得紧急使用授权(EUA)。从2023年中开始,三叶草生物以其自研新冠疫苗所累积的丰富经验和资源,结合自身技术平台特点,以潜在商业价值最大化为导向布局管线研发,开始集中快速推进自研的呼吸道合胞病毒(RSV)候选疫苗SCB-1019。2023年12月初,三叶草生物宣布启动RSV候选疫苗I期临床试验,成为中国首家开发 RSV PreF (基于融合前构象的F蛋白) 疫苗并进入人体临床试验阶段的疫苗公司,这坚定了三叶草生物在中国RSV领域的领跑地位。
三叶草生物拥有自研的Trimer-Tag (蛋白质三聚体化)疫苗开发技术平台,且该技术平台已得到全面验证: 基于该技术平台自研的新冠疫苗 (SCB-2019) 在全球八个国家、五大洲有近4万人入组多项III期临床试验,后在中国获得紧急使用授权(EUA)。从2023年中开始,三叶草生物以其自研新冠疫苗所累积的丰富经验和资源,结合自身技术平台特点,以潜在商业价值最大化为导向布局管线研发,开始集中快速推进自研的呼吸道合胞病毒(RSV)候选疫苗SCB-1019。2023年12月初,三叶草生物宣布启动RSV候选疫苗I期临床试验,成为中国首家开发 RSV PreF (基于融合前构象的F蛋白) 疫苗并进入人体临床试验阶段的疫苗公司,这坚定了三叶草生物在中国RSV领域的领跑地位。








評論(0)
請選擇舉報原因