①針對網傳裁員消息,榮昌生物董秘稱,從去年即開始對公司的業務進行梳理,崗位與人員優化只是根據工作需要,沒有硬性的比例;②對方透露,靶向藥物泰它西普的重症肌無力適應症近期將申報上市。但在市場上,泰它西普正面臨多重競爭。
《科創板日報》9月20日訊(記者 鄭炳巽) 近日,在網絡上逐漸發酵的一則裁員傳聞,再次讓榮昌生物(688331.SH)成爲輿論的焦點。
正在網上流傳的圖片顯示,關於榮昌生物裁員的說法其實不止一種。其中,有說法稱公司將有兩輪裁員,預計裁員比例70%,也有說法是裁員人數將近1000人,還有說法是裁員已經從今年8月開始。當然,其他裁員版本也在流傳。
 針對此事,《科創板日報》記者向榮昌生物董秘溫慶凱求證真僞,以及裁員比例。對方回覆稱,「其實公司從去年即開始對公司的業務進行了梳理,並根據梳理情況進行崗位、人員優化。優化只是根據工作需要,沒有硬性的比例。」
針對此事,《科創板日報》記者向榮昌生物董秘溫慶凱求證真僞,以及裁員比例。對方回覆稱,「其實公司從去年即開始對公司的業務進行了梳理,並根據梳理情況進行崗位、人員優化。優化只是根據工作需要,沒有硬性的比例。」
▌開啓崗位與人員優化
事實上,在今年之前,榮昌生物的職工人數仍處於增加狀態,2022年總數爲3332人,2023年增加至3615人,增幅爲8.49%。但在進入2024年後,這一情況開始改變。
截至2024年上半年,榮昌生物研發人員數量1216人,較去年同期1271人減少4.33%。今年上半年研發人員佔公司總人數比例爲34.77%,以此計算,公司總人數約爲3497人,較2023年年底減少118人。
不過,榮昌生物今年上半年研發人員雖然在減少,但研發投入卻還在增加,其中,研發人員薪酬合計2.36億元,同比增長14.21%,研發費用合計8.06億元,同比增長49.18%。同時,銷售費用也同比增長11.28%至3.90億元。
榮昌生物表示,由於報告期內不斷拓展在研產品管線,推進現有臨床項目的開展,導致研發費用增長,同時,隨着泰它西普和維迪西妥單抗的准入醫院數量及覆蓋藥房數量大幅度增加,一線銷售人員擴充導致銷售費用增加。
受此影響,報告期內,榮昌生物實現營收7.42億元,同比增長75.59%,歸母淨虧損7.80億元,較去年期淨虧損7.03億元進一步擴大。
截至2024年上半年,榮昌生物除了泰它西普(RC18)的系統性紅斑狼瘡、類風溼關節炎,以及維迪西妥單抗(RC48)的HER2表達胃癌、HER2表達尿路上皮癌4個適應症在中國獲批上市之外,其餘合計擁有超過20個適應症處於臨床研究之中,且在全球範圍內有超過10條管線處於關鍵/III期臨床。
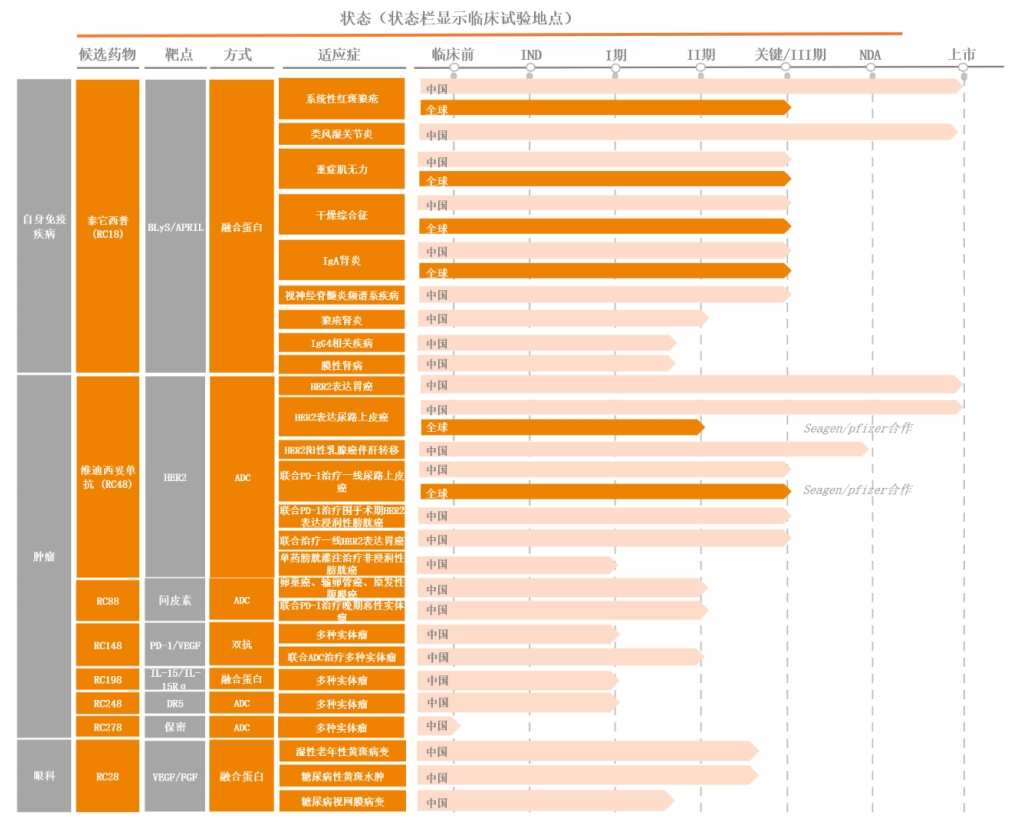
榮昌生物在研管線(截至2024年上半年)
衆多管線同步推進,快速消耗榮昌生物賬上資金,公司期末現金及現金等價物餘額由2022年底的20.69億元減少至2023年上半年的11.20億元,2023年年底減少至7.27億元,到2024年上半年進一步減少至6.73億元。
有感於日益增長的資金壓力,榮昌生物在今年3月底對外披露了一份定增預案,擬向特定對象發行最高7076.32萬股股票,募集資金25.5億元投入「新藥研發項目」,具體用於包括「臨床前研究及RC18、RC48、RC28、RC88、RC148及RC198等產品的臨床研究」,項目投資總額約29.46億元。
然而,今年7月底,榮昌生物針對定增預案發行了一版新的修訂稿,擬募資總金額減少爲19.53億元,用途的表述也變更爲用於「包括RC18、RC48、RC28、RC88、RC148及RC198等產品的臨床研究」,相比於第一個版本,去除了「臨床前研究」的表述,而項目投資總額同樣也下調至19.53億元。
或許,正是長期以來的入不敷出,加之定增目標的縮減,使得榮昌生物開啓崗位和人員的優化工作。
這一變動,似乎也指向了高層人員。今年8月上旬,榮昌生物對外宣佈,任命何如意爲公司首席戰略官,何如意不再擔任公司首席醫學官及高級管理人員,但將繼續擔任公司董事且爲核心技術人員。
▌gMG適應症面臨多方競爭
對於榮昌生物而言,近期的積極消息,或許應屬於泰它西普用於治療全身型重症肌無力(gMG)的III期臨床研究,達到方案設計的臨床試驗主要研究終點。
榮昌生物表示,對於重症肌無力,目前尚無滿意治療措施,有效、精準、安全的靶向生物製劑成爲重症肌無力藥物研發的熱點。而泰它西普可同時靶向BLyS和APRIL,直擊致病性抗體產生的源頭——B細胞及漿細胞,從而減少致病性抗體的產生,發揮治療作用。
溫慶凱向《科創板日報》記者透露,「公司近期將會申報泰它西普重症肌無力適應症的上市。」
根據弗若斯特沙利文報告,全球重症肌無力患者人數預計2025年達到114.60萬,中國患者人數約爲21.67萬。
另據頭豹研究院,2018-2023年,重症肌無力藥物(MG)行業市場規模由11.25億人民幣元增長至12.33億人民幣元。預計2024-2028年,這一市場規模由12.51億人民幣元增長至13.42億人民幣元。
但是,《2022中國重症肌無力患者健康報告》顯示,針對重症肌無力的治療,預測採用激素、膽鹼酯酶抑制劑及免疫製劑的患者比例分別爲50%、60%、31%,而較爲昂貴的靶向藥物應用比例低,預計僅在1.3-1.5%。
不僅如此,在靶向藥物賽道上,泰它西普也面臨不少競爭對手。
根據頭豹研究院的統計,首先,2023年,阿斯利康的依庫珠單抗獲批上市,用於治療抗乙酰膽鹼受體(AChR)抗體陽性的難治性gMG成人患者,成爲中國首個獲批用於治療gMG的補體抑制劑。其次,在原研廠商羅氏的利妥昔單抗專利到期後,截至2024年6月,已有4家企業的利妥昔單抗獲批上市。
《科創板日報》記者亦發現,今年7月,再鼎醫藥的「艾加莫德α注射液(皮下注射)」獲NMPA批准上市,用於治療乙酰膽鹼受體(AChR)抗體陽性的成人gMG。在此之前,艾加莫德α注射液(靜脈輸注)先於2023年6月獲批上市。
2024年上半年,靜脈輸注型艾加莫德α注射液實現產品收入3640萬美元,再鼎醫藥預計產品全年收入超過8000萬美元。
此外,在新藥上市申請方面,泰它西普也有競爭對手。其中,和鉑醫藥的巴託利單抗(HBM9161)已於2024年6月重新提交針對gMG的BLA,次月獲得NMPA受理。和鉑醫藥預測,巴託利單抗有望在2025年獲批。

 针对此事,《科创板日报》记者向荣昌生物董秘温庆凯求证真伪,以及裁员比例。对方回复称,
针对此事,《科创板日报》记者向荣昌生物董秘温庆凯求证真伪,以及裁员比例。对方回复称,