来源:锦缎
作者:青栎
世人皆知“药物”$礼来 (LLY.US)$是以GLP-1起家,但却鲜有人知晓,礼来8000亿美元市值背后,其阿尔兹海默症(简称AD)的研究也贡献了不低的市场估值。
礼来之所以能够在市值上领先于诺和诺德,除减肥神药替尔泊肽的加速放量外,更核心的原因在于长久以来在AD领域的持续钻研。实际上,在过去五年中,每当礼来在AD领域有所突破后,都会提振公司股价的上涨。
7月2日,礼来研发的Kisunla(Donanemab)获FDA批准用于治疗早期症状性阿尔茨海默病,正式踏入了AD这个千亿美元潜力市场的大门,并将与渤健展开正面交锋。礼来终于挥出了手中的“第二把剑”。
01 挑战风车的骑士
礼来布局AD,这曾被视为是一个“唐吉坷德”式的行为。
尽管AD已经被发现百余年,但人类却始终无法找到攻克它的方式。目前,全球约有5000万AD患者,随着全球人口老龄化的加剧,预计到2050年时,这个数字将会达到1.3亿。随着年纪的增长,罹患AD的概率越高,85岁老人患AD的概率超过30%。可以说,AD是一个与我们每一个人都息息相关的疾病。
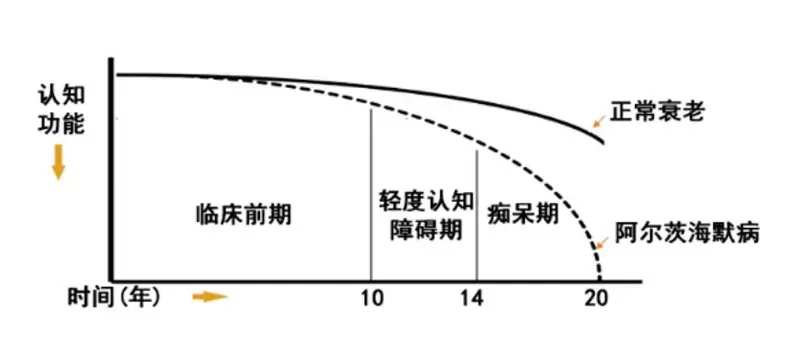 图:衰老与阿尔茨海默病,来源:西部证券
图:衰老与阿尔茨海默病,来源:西部证券在2021年之前,美国FDA仅批准过6种治疗AD的药物,且这些药物都只能改善患者的症状,不能减轻AD的病理性变化,更不能逆转或减缓已经发生的疾病进程,此外这些药物还存在诸多的副作用。
庞大的用户基数,神秘的发病机制,激发了无数科学家的好胜心,因此攻克AD也成为医药产业极为重要的一个课题。为了找到问题的答案,无数药企投入大量的时间与金钱,但最终却始终没有收获,甚至连其发病理论都难以摸清,因此AD一度被称为药企“研发黑洞”。
在这一众药企中,礼来可谓是最执着的一个。早在上世纪90年代,礼来就开始投身于AD药物研发。
1992年,英国科学家约翰·哈迪在《科学》杂志上发表了“Aβ级联假说”。这种假说认为Aβ沉积是一系列分子事件的主要触发因素,这些事件导致产生过度磷酸化tau蛋白寡聚体,从而导致神经元凋亡机制的激活,最终导致AD发生。在这套理论体系下,“Aβ是杀手,tau是吸烟枪,神经元是受害者”。
“Aβ级联假说”给AD药物研发提供了新的思路,礼来科学家根据这一假说,设计了一种针对可溶性β-淀粉样蛋白的单克隆抗体——Solanezumab,并在2002年于《Nature Neuroscience》中公开了他们的研究成果。然而,在经历十年的漫长临床研究后,这款药物还是在2012年被证实无效,最终倒在III期临床试验中。
面对失败,礼来并未完全丧失信心,他们认为Solanezumab的机制没有问题,虽然无法治疗轻中度AD患者,但可能对处于疾病早期阶段的AD患者有效。于是礼来启动了新的临床研究,在那些大脑中已出现β-淀粉样蛋白斑块但尚未出现症状的早期AD病患者身上测试Solanezumab,共1100名患者接受Solanezumab或安慰剂治疗4.5年。
现实总是残酷的。2016年11月,礼来公布临床试验结果:Solanezumab并没能达到预期的理想效果,最终试验失败。到此时为止,礼来已经合计为Solanezumab投入了超30亿美元,然而却换来了个寂寞,消息传出后礼来股价当日重挫16%。再加上当时礼来核心药物胰岛素销量下降,市场中甚至传出礼来将被其他巨头吞并的传闻。
Solanezumab只是无数AD药物研发失败的一个缩影。根据美国药物生产与研发协会发布的研究报告,2000-2017年,全球累计投入在AD上的研发费用投入超过6000亿美元,失败的临床药物超过300种,失败率高达99.6%,其中不乏默沙东、辉瑞、罗氏等跨国大药企的惨败。
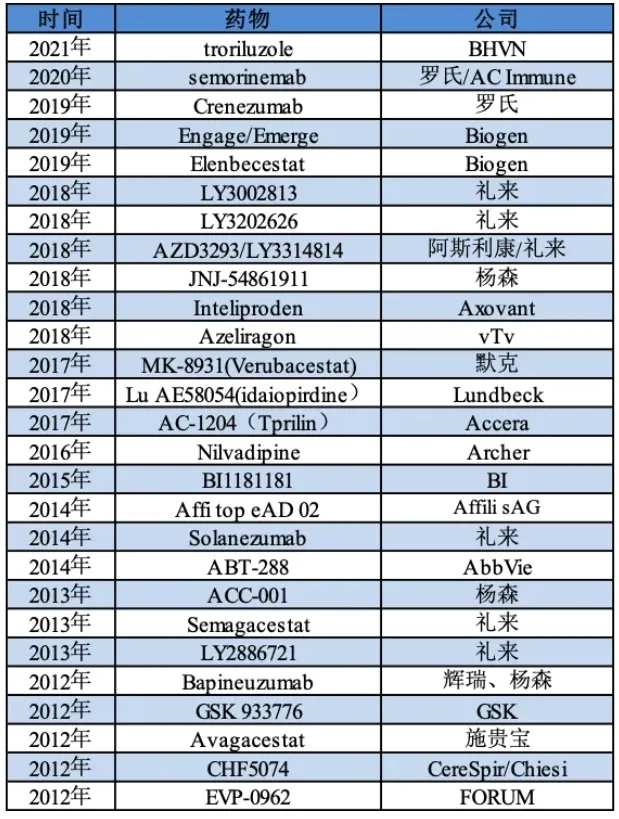 近十年全球部分失败的AD药物,来源:凯莱英
近十年全球部分失败的AD药物,来源:凯莱英面对AD这个“研发黑洞”,礼来坦然接受了Solanezumab的失败,但却并没有放弃对于这一疾病的研发。在Donanemab获批之前,礼来已经在AD适应症上投入超过80亿美元的研发费用。
02 礼来AD策略:管线“赛马”
礼来深知AD领域的困难,因此它并没有将全部资源梭哈在Solanezumab之上,而是采取了产品“赛马”的矩阵布局方式。
除了Solanezumab,礼来还同时布局了Donanemab、Semagacestat、Lanabecestat和Remternetug等几款AD药物。虽然其中的Semagacestat和Lanabecestat分别于2010年和2018年宣告失败,让礼来公司内部对是否要坚持“Aβ级联假说”路线产生动摇,但最终礼来还是选择了坚持。在汲取失败经验后,礼来将研发重点转向清除沉积斑块的抗体,而Donanemab就是这样一款产品。
在礼来AD研发体系中,Ronald DeMattos博士是关键人物。他于2002年加入公司,投身于Solanezumab的研发工作。在研发Solanezumab的同时,DeMattos博士就着手开始研究Solanezumab的“升级版本”。在研究的过程中,DeMattos博士在淀粉样斑块中发现了一种特定的环状结构N3pG,这为药物靶向递送提供了关键的靶点,新的抗体Donanemab就此诞生。
尽管礼来找到了最终的目标,但验证Donanemab的过程还是充满坎坷。
临床前阶段还算顺利,DeMattos花费了4年时间,培育出斑块水平与患病人群相似的小鼠,Donanemab成功使小鼠大脑中的淀粉样斑块水平急剧下降。
可到了2011年,Donanemab开始进入临床I期,但来自第一阶段的数据却让这个项目险些流产。数据显示,超过90%的患者都对Donanemab产生了抗药抗体,研究人员担心这种免疫反应会阻碍药物进入大脑。
好在礼来通过放射性分子结合PET扫描的方法检测沉积斑块,发现该药物并没有受到免疫反应的影响,单次输注Donanemab 即可减少患者脑部的沉积斑块,多次给药的许多患者脑部斑块完全被清除。这一结果让礼来的研发人员无比振奋,开始全力推动Donanemab上市。
2021年1月,礼来宣布顺利地完成II期临床试验,结果显示,Donanemab在18个月内将某些早期阿尔茨海默病患者的认知和功能下降速度减缓了35%。但由于其二期临床试验入组患者仅有94人,而FDA特别要求礼来提供至少100名接受过12个月持续治疗的患者数据,因此Donanemab被拒绝提前批准。
然而,此时卫材和渤健联合开发的AD新药仑卡奈单抗(Leqembi)于2023年1月获得FDA加速批准,7月获FDA完全批准,成为全球首个能延缓AD进程的药物。虽然礼来未能在“FIC”竞争中取胜,但“后发先至”却是其一贯的战略。
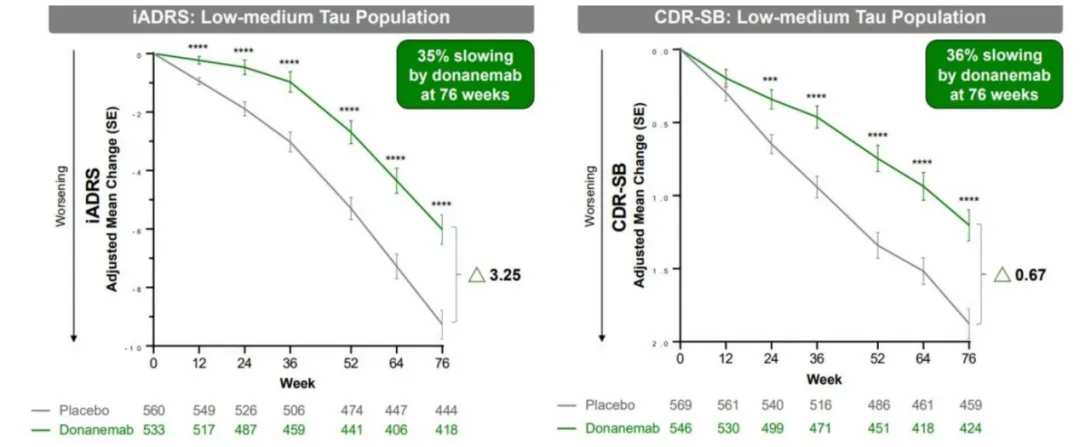
2023年7月,礼来宣布了Donanemab的最新完整III期临床数据。与安慰剂相比,接受Donanemab治疗18个月内,早期患者的认知与功能下降速度减缓了35%。在轻度认知功能障碍的患者中效果更加明显,减缓幅度超过了50%,并且72%的患者在使用该药物一年左右就可以基本清除所有斑块。
![图:Donanemab的III期临床数据 来源:太平洋证券]() 图:Donanemab的III期临床数据 来源:太平洋证券
图:Donanemab的III期临床数据 来源:太平洋证券从临床研究数据来看,Donanemab的疗效更优于Leqembi。Leqembi在18个月内使阿尔茨海默病患者的认知和功能下降速度减缓了27%。且Leqembi是每两周给药一次,Donanemab每四周给药一次。
与其说Donanemab是在疗效上胜过了Leqembi,倒不如说礼来在AD领域的准备更加充分。
03 AD新王登基?
基于优异的III期临床数据,礼来于2023年第二季度再次向FDA递交了Donanemab的上市申请。
FDA本应在今年第一季度对该申请作出审批决定,但在今年3月8日,FDA决定推迟Donanemab药物的上市批准,并将组织外部专家会议讨论该药物的安全性和有效性,为该药上市蒙上了阴影,当天礼来股价跌了2.31%。III期临床数据显示,31.4%受治疗者出现了大脑微出血,明显高于安慰剂组的13.6%,另外有3名实验患者的死亡与治疗有关。
直至今年6月10日,FDA 独立科学顾问委员会进行审查,根据II期和III 期临床试验的结果,委员会就两个具体问题进行了投票。最终,委员会以11:0的票数一致赞同该药物的有效性,并一致赞同其获益大于风险。至此,礼来守得云开见月明。
7月2日,礼来宣布新药Donanemab获FDA批准,用于治疗早期症状性AD,包括轻度认知障碍(MCI)患者及患有轻度痴呆阶段的AD患者。Donanemab的成功获批为AD患者提供了一种新的治疗选择,再次验证了Aβ假说的有效性,鼓舞了正在研究的AD治疗药物项目,为未来基于β淀粉样蛋白的药物研发指明了方向。
同时,Donanemab获批意味着礼来三十余年来在AD领域的持续投入初次获得回报。与Leqembi相比,Donanemab是首个且唯一有限疗程的淀粉样斑块靶向疗法,当患者达到一定的淀粉样斑块清除率,即可停止用药,Leqembi则没有相关停药方案。目前Donanemab美国售价为695.65美元/瓶,单年治疗费用为3.2万美元;相比之下,Leqembi年治疗费用为2.65万美元。
今年一季度,Leqembi实现营收1900万美元,远高于分析师平均预期的 700 万美元,这款药物或将成为渤健未来的营收支柱。数据更好的Donanemab无疑潜力更大,甚至有机会成为一款药王级产品,极有可能成为下一个类似减肥药(GLP-1)的热点。
更为关键的是,Donanemab还只是礼来迈向AD领域的第一步,后续礼来仍有多款矩阵产品正在推进中,礼来不会满足于阶段性的胜利,它会继续不断对产品进行升级迭代。
Remternetug就是礼来开发的另一款AD药物,即下一代N3pG淀粉样蛋白抗体,该药物采用静脉注射、皮下给药等灵活给药方式。I期临床试验结果显示,Remternetug可快速清除斑块,给药169天后,24例受试者中有18例淀粉样蛋白实现了清除,预计2025年10月完成III期试验。
如今的“药王”礼来手中已经握着两把剑,一把是“GLP-1”药物,在糖尿病领域和减肥领域大杀四方,让后来者难以望其项背;另一把就是AD治疗药物,艰难打磨三十余年,在利剑出鞘的那一刻,短期内恐难有人撼动礼来医药王者之位。
编辑/Somer
來源:錦緞
作者:青櫟
世人皆知「藥物」$禮來 (LLY.US)$是以GLP-1起家,但卻鮮有人知曉,禮來8000億美元市值背後,其阿爾茲海默症(簡稱AD)的研究也貢獻了不低的市場估值。
禮來之所以能夠在市值上領先於諾和諾德,除減肥神藥替爾泊肽的加速放量外,更核心的原因在於長久以來在AD領域的持續鑽研。實際上,在過去五年中,每當禮來在AD領域有所突破後,都會提振公司股價的上漲。
7月2日,禮來研發的Kisunla(Donanemab)獲FDA批准用於治療早期症狀性阿爾茨海默病,正式踏入了AD這個千億美元潛力市場的大門,並將與渤健展開正面交鋒。禮來終於揮出了手中的「第二把劍」。
01 挑戰風車的騎士
禮來佈局AD,這曾被視爲是一個「唐吉坷德」式的行爲。
儘管AD已經被發現百餘年,但人類卻始終無法找到攻克它的方式。目前,全球約有5000萬AD患者,隨着全球人口老齡化的加劇,預計到2050年時,這個數字將會達到1.3億。隨着年紀的增長,罹患AD的概率越高,85歲老人患AD的概率超過30%。可以說,AD是一個與我們每一個人都息息相關的疾病。
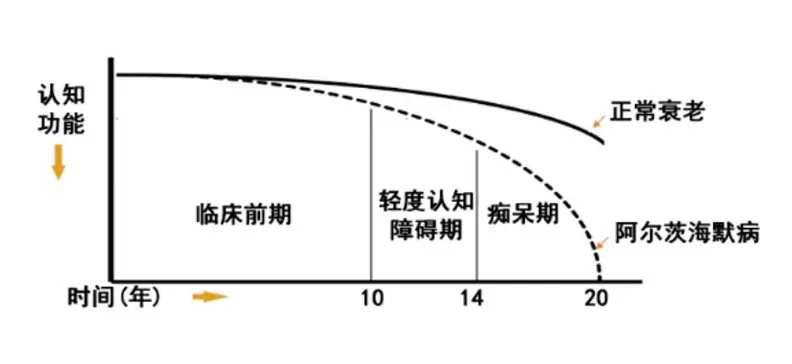 圖:衰老與阿爾茨海默病,來源:西部證券
圖:衰老與阿爾茨海默病,來源:西部證券在2021年之前,美國FDA僅批准過6種治療AD的藥物,且這些藥物都只能改善患者的症狀,不能減輕AD的病理性變化,更不能逆轉或減緩已經發生的疾病進程,此外這些藥物還存在諸多的副作用。
龐大的用戶基數,神祕的發病機制,激發了無數科學家的好勝心,因此攻克AD也成爲醫藥產業極爲重要的一個課題。爲了找到問題的答案,無數藥企投入大量的時間與金錢,但最終卻始終沒有收穫,甚至連其發病理論都難以摸清,因此AD一度被稱爲藥企「研發黑洞」。
在這一衆藥企中,禮來可謂是最執着的一個。早在上世紀90年代,禮來就開始投身於AD藥物研發。
1992年,英國科學家約翰·哈迪在《科學》雜誌上發表了「Aβ級聯假說」。這種假說認爲Aβ沉積是一系列分子事件的主要觸發因素,這些事件導致產生過度磷酸化tau蛋白寡聚體,從而導致神經元凋亡機制的激活,最終導致AD發生。在這套理論體系下,「Aβ是殺手,tau是吸菸槍,神經元是受害者」。
「Aβ級聯假說」給AD藥物研發提供了新的思路,禮來科學家根據這一假說,設計了一種針對可溶性β-澱粉樣蛋白的單克隆抗體——Solanezumab,並在2002年於《Nature Neuroscience》中公開了他們的研究成果。然而,在經歷十年的漫長臨床研究後,這款藥物還是在2012年被證實無效,最終倒在III期臨床試驗中。
面對失敗,禮來並未完全喪失信心,他們認爲Solanezumab的機制沒有問題,雖然無法治療輕中度AD患者,但可能對處於疾病早期階段的AD患者有效。於是禮來啓動了新的臨床研究,在那些大腦中已出現β-澱粉樣蛋白斑塊但尚未出現症狀的早期AD病患者身上測試Solanezumab,共1100名患者接受Solanezumab或安慰劑治療4.5年。
現實總是殘酷的。2016年11月,禮來公佈臨床試驗結果:Solanezumab並沒能達到預期的理想效果,最終試驗失敗。到此時爲止,禮來已經合計爲Solanezumab投入了超30億美元,然而卻換來了個寂寞,消息傳出後禮來股價當日重挫16%。再加上當時禮來核心藥物胰島素銷量下降,市場中甚至傳出禮來將被其他巨頭吞併的傳聞。
Solanezumab只是無數AD藥物研發失敗的一個縮影。根據美國藥物生產與研發協會發布的研究報告,2000-2017年,全球累計投入在AD上的研發費用投入超過6000億美元,失敗的臨床藥物超過300種,失敗率高達99.6%,其中不乏默沙東、輝瑞、羅氏等跨國大藥企的慘敗。
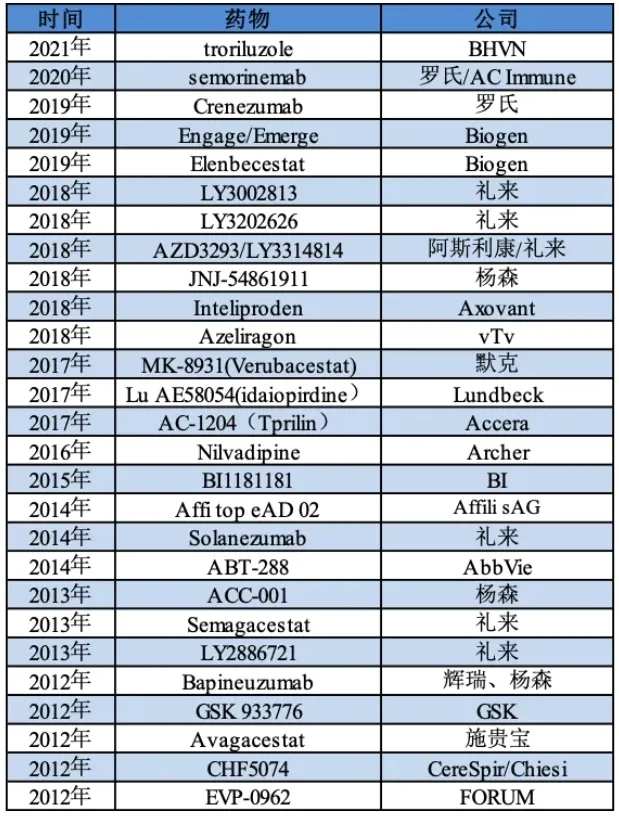 近十年全球部分失敗的AD藥物,來源:凱萊英
近十年全球部分失敗的AD藥物,來源:凱萊英面對AD這個「研發黑洞」,禮來坦然接受了Solanezumab的失敗,但卻並沒有放棄對於這一疾病的研發。在Donanemab獲批之前,禮來已經在AD適應症上投入超過80億美元的研發費用。
02 禮來AD策略:管線「賽馬」
禮來深知AD領域的困難,因此它並沒有將全部資源梭哈在Solanezumab之上,而是採取了產品「賽馬」的矩陣佈局方式。
除了Solanezumab,禮來還同時佈局了Donanemab、Semagacestat、Lanabecestat和Remternetug等幾款AD藥物。雖然其中的Semagacestat和Lanabecestat分別於2010年和2018年宣告失敗,讓禮來公司內部對是否要堅持「Aβ級聯假說」路線產生動搖,但最終禮來還是選擇了堅持。在汲取失敗經驗後,禮來將研發重點轉向清除沉積斑塊的抗體,而Donanemab就是這樣一款產品。
在禮來AD研發體系中,Ronald DeMattos博士是關鍵人物。他於2002年加入公司,投身於Solanezumab的研發工作。在研發Solanezumab的同時,DeMattos博士就着手開始研究Solanezumab的「升級版本」。在研究的過程中,DeMattos博士在澱粉樣斑塊中發現了一種特定的環狀結構N3pG,這爲藥物靶向遞送提供了關鍵的靶點,新的抗體Donanemab就此誕生。
儘管禮來找到了最終的目標,但驗證Donanemab的過程還是充滿坎坷。
臨床前階段還算順利,DeMattos花費了4年時間,培育出斑塊水平與患病人群相似的小鼠,Donanemab成功使小鼠大腦中的澱粉樣斑塊水平急劇下降。
可到了2011年,Donanemab開始進入臨床I期,但來自第一階段的數據卻讓這個項目險些流產。數據顯示,超過90%的患者都對Donanemab產生了抗藥抗體,研究人員擔心這種免疫反應會阻礙藥物進入大腦。
好在禮來通過放射性分子結合PET掃描的方法檢測沉積斑塊,發現該藥物並沒有受到免疫反應的影響,單次輸注Donanemab 即可減少患者腦部的沉積斑塊,多次給藥的許多患者腦部斑塊完全被清除。這一結果讓禮來的研發人員無比振奮,開始全力推動Donanemab上市。
2021年1月,禮來宣佈順利地完成II期臨床試驗,結果顯示,Donanemab在18個月內將某些早期阿爾茨海默病患者的認知和功能下降速度減緩了35%。但由於其二期臨床試驗入組患者僅有94人,而FDA特別要求禮來提供至少100名接受過12個月持續治療的患者數據,因此Donanemab被拒絕提前批准。
然而,此時衛材和渤健聯合開發的AD新藥侖卡奈單抗(Leqembi)於2023年1月獲得FDA加速批准,7月獲FDA完全批准,成爲全球首個能延緩AD進程的藥物。雖然禮來未能在「FIC」競爭中取勝,但「後發先至」卻是其一貫的戰略。
2023年7月,禮來宣佈了Donanemab的最新完整III期臨床數據。與安慰劑相比,接受Donanemab治療18個月內,早期患者的認知與功能下降速度減緩了35%。在輕度認知功能障礙的患者中效果更加明顯,減緩幅度超過了50%,並且72%的患者在使用該藥物一年左右就可以基本清除所有斑塊。
![圖:Donanemab的III期臨床數據 來源:太平洋證券]() 圖:Donanemab的III期臨床數據 來源:太平洋證券
圖:Donanemab的III期臨床數據 來源:太平洋證券從臨床研究數據來看,Donanemab的療效更優於Leqembi。Leqembi在18個月內使阿爾茨海默病患者的認知和功能下降速度減緩了27%。且Leqembi是每兩週給藥一次,Donanemab每四周給藥一次。
與其說Donanemab是在療效上勝過了Leqembi,倒不如說禮來在AD領域的準備更加充分。
03 AD新王登基?
基於優異的III期臨床數據,禮來於2023年第二季度再次向FDA遞交了Donanemab的上市申請。
FDA本應在今年第一季度對該申請作出審批決定,但在今年3月8日,FDA決定推遲Donanemab藥物的上市批准,並將組織外部專家會議討論該藥物的安全性和有效性,爲該藥上市蒙上了陰影,當天禮來股價跌了2.31%。III期臨床數據顯示,31.4%受治療者出現了大腦微出血,明顯高於安慰劑組的13.6%,另外有3名實驗患者的死亡與治療有關。
直至今年6月10日,FDA 獨立科學顧問委員會進行審查,根據II期和III 期臨床試驗的結果,委員會就兩個具體問題進行了投票。最終,委員會以11:0的票數一致贊同該藥物的有效性,並一致贊同其獲益大於風險。至此,禮來守得雲開見月明。
7月2日,禮來宣佈新藥Donanemab獲FDA批准,用於治療早期症狀性AD,包括輕度認知障礙(MCI)患者及患有輕度癡呆階段的AD患者。Donanemab的成功獲批爲AD患者提供了一種新的治療選擇,再次驗證了Aβ假說的有效性,鼓舞了正在研究的AD治療藥物項目,爲未來基於β澱粉樣蛋白的藥物研發指明瞭方向。
同時,Donanemab獲批意味着禮來三十餘年來在AD領域的持續投入初次獲得回報。與Leqembi相比,Donanemab是首個且唯一有限療程的澱粉樣斑塊靶向療法,當患者達到一定的澱粉樣斑塊清除率,即可停止用藥,Leqembi則沒有相關停藥方案。目前Donanemab美國售價爲695.65美元/瓶,單年治療費用爲3.2萬美元;相比之下,Leqembi年治療費用爲2.65萬美元。
今年一季度,Leqembi實現營收1900萬美元,遠高於分析師平均預期的 700 萬美元,這款藥物或將成爲渤健未來的營收支柱。數據更好的Donanemab無疑潛力更大,甚至有機會成爲一款藥王級產品,極有可能成爲下一個類似減肥藥(GLP-1)的熱點。
更爲關鍵的是,Donanemab還只是禮來邁向AD領域的第一步,後續禮來仍有多款矩陣產品正在推進中,禮來不會滿足於階段性的勝利,它會繼續不斷對產品進行升級迭代。
Remternetug就是禮來開發的另一款AD藥物,即下一代N3pG澱粉樣蛋白抗體,該藥物採用靜脈注射、皮下給藥等靈活給藥方式。I期臨床試驗結果顯示,Remternetug可快速清除斑塊,給藥169天后,24例受試者中有18例澱粉樣蛋白實現了清除,預計2025年10月完成III期試驗。
如今的「藥王」禮來手中已經握着兩把劍,一把是「GLP-1」藥物,在糖尿病領域和減肥領域大殺四方,讓後來者難以望其項背;另一把就是AD治療藥物,艱難打磨三十餘年,在利劍出鞘的那一刻,短期內恐難有人撼動禮來醫藥王者之位。
編輯/Somer