德邦證券股份有限公司李霽陽近期對邁威生物進行研究併發布了研究報告《ADC多個數據發佈,國內類似藥商業化順利推進》,本報告對邁威生物給出買入評級,當前股價爲31.28元。
邁威生物(688062)
投資要點
業績:公司2024年4月9日發佈年報,2023年度營業收入1.28億元,技術服務收入8559.53萬元,藥品銷售收入4209萬元,研發投入爲8.36億元,歸母淨虧損爲10.53億元,主要原因是君邁康與邁利舒上市時間較短,且公司一直保持較高的研發投入。公司擁有10個創新藥,4個生物類似藥在臨床,已上市品種3個,NDA階段1個,III期階段品種3個。公司具備抗體、ADC及重組蛋白藥物的研發和產業化能力。截至23年底公司在職員工1491人,其中技術研發人員398名。
ADC多個數據發表,平台價值凸顯。
9MW2821(Nectin-4ADC)已進入三期,發表多個適應症數據;
a)UC尿路上皮癌單藥二三線ORR:62.2%,DCR:91.9%,中位PFS爲6.7個月,已完成三期臨床首例患者入組;聯合PD-1治療晚期或轉移性尿路上皮癌患者已完成一期臨床首例患者入組。
b)CC宮頸癌:37例既往接受過含鉑雙藥化療聯合或不聯合貝伐珠單抗治療的可評估療效患者ORR:40.54%,DCR:89.19%,其中26例Nectin-43+患者ORR:50%,DCR:92.31%;
c)EC食管癌:30例單藥治療既往接受過含鉑化療和PD-(L)1抑制劑治療的可評估療效的患者ORR:30%,DCR:73.3%。
9MW2921(新型Trop-2ADC)、7MW3711(新型B7-H3ADC)2023年7月開展臨床試驗,進度處於I/II期臨床研究入組階段。
創新藥管線豐富,多個差異化品種中美雙報。IL-33、IL-11、TMPRSS6等多箇中美雙報創新品種處於臨床階段。其中TMPRSS6抗體(9MW3011)於2023年1月將大中華區和東南亞以外權益授予DISC MEDICINE,總交易總額最高可達4.125億美元。後期管線中,三代長效G-CSF8MW0511已申報上市;
商業化持續持續推進,9MW0321獲批。君邁康?於2023年一季度末全面恢復商業供貨,2023年發貨166921支;准入醫院173家,覆蓋藥店1316家。根據2024年4月簽署的補充協議,君實康將不再作爲君邁康?的MAH,由君實生物直接將君邁康?藥品上市許可持有人轉讓給邁威生物。邁利舒?於2023年3月底獲批上市,4月25日完成首批商業發貨,2023年完成發貨84474支;完成28省招標掛網,29省完成省級醫保對接;准入醫院605家,覆蓋藥店2061家。9MW0321地舒單抗(120mg)(安加維?的生物類似藥)2024年3月29日上市申請獲得CDE批准,適應症骨鉅細胞瘤。
盈利預測。我們認爲公司ADC平台能力已充分驗證,隨着適應症的持續開發和海外臨床推進價值將進一步凸顯。我們預計公司24-26年收入爲2.44、10.42、22.44億元。維持“買入”評級。
風險提示:銷售不及預期、臨床開發進度不及預期、政策變化風險等
證券之星數據中心根據近三年發佈的研報數據計算,華金證券趙寧達研究員團隊對該股研究較爲深入,近三年預測準確度均值爲79.97%,其預測2024年度歸屬淨利潤爲虧損9.7億。
最新盈利預測明細如下:
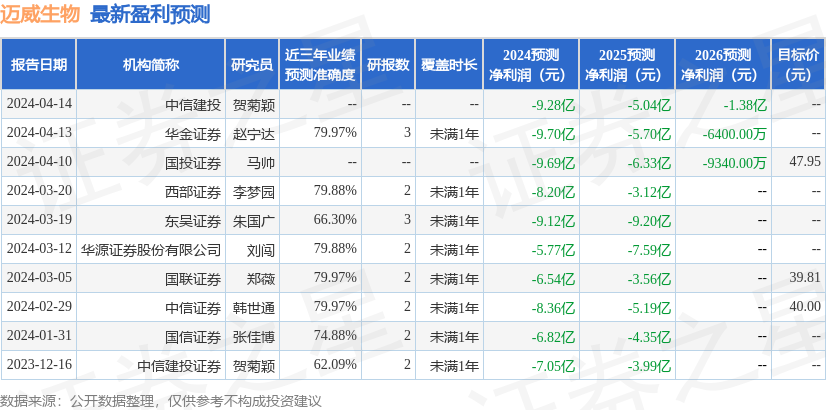
該股最近90天內共有10家機構給出評級,買入評級8家,增持評級2家;過去90天內機構目標均價爲44.56。
以上內容由證券之星根據公開信息整理,由算法生成(網信算備310104345710301240019號),與本站立場無關,如數據存在問題請聯繫我們。本文爲數據整理,不對您構成任何投資建議,投資有風險,請謹慎決策。
